Toepassingen van lood
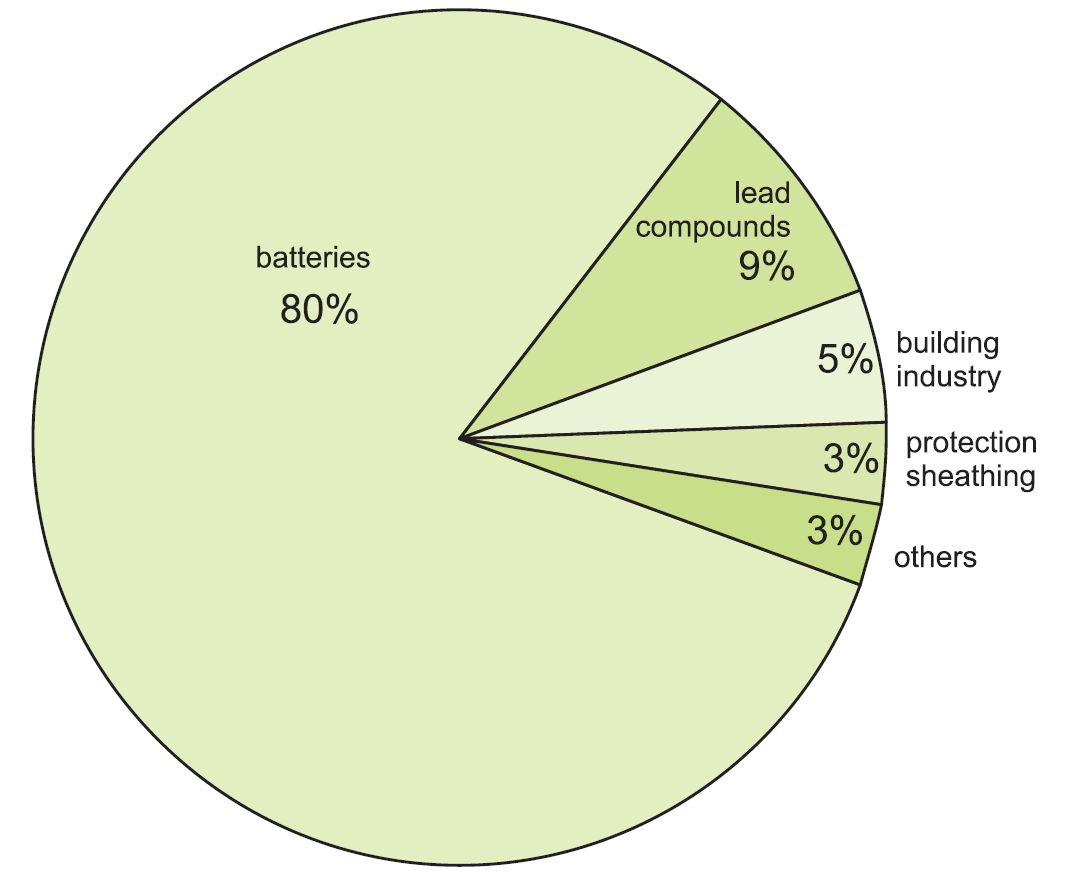
Meer dan 80% van al het geproduceerde lood komt terecht in lood-zuur batterijen, met loodmetaal als kathode en lood(IV)oxide als anode. Naast startaccu’s voor wegvoertuigen worden deze ook gebruikt voor nulemissie- en hybride voertuigen, noodstroomvoorziening (bijvoorbeeld voor computers en telefoonsystemen) en energieopslag in afgelegen stroomtoepassingen.
Figuur 1 Gebruik van lood.
De rest wordt gebruikt in een breed scala van toepassingen:
- stralingsschermen, hetzij als metaalplaat (bij gebruik van röntgen- en andere krachtige stralingsapparatuur), hetzij als loodverbindingen in glas ter bescherming tegen straling (zoals in televisiebuizen en in medische apparatuur)
- als loodverbindingen toegevoegd aan poly(chlooretheen) (PVC) als stabilisator (wanneer duurzaamheid van belang is)
- in dakbedekking (bijv, voor gootstukken op daken)
- pijpen en bekleding van vaten in chemische fabrieken (lood wordt niet meer gebruikt voor waterleidingen voor huishoudelijk gebruik)
- bescherming van ondergrondse of onderzeese stroomkabels
Lood wordt ook gebruikt in een verscheidenheid van legeringen met staal, messing en aluminium (om de bewerkbaarheid te verbeteren) en met tin voor solderen.
Jaarlijkse productie (primair lood)
Deze cijfers betreffen de primaire productie uit het erts en niet de secundaire productie uit gerecycleerd materiaal.
| Wereld | 4,7 miljoen ton |
| China | 2,3 miljoen ton |
| Australië | 633 000 ton |
| V.S. | 385 000 ton |
| Peru | 300 000 ton |
| Mexico | 240 000 ton |
| India | 130 000 ton |
Gegevens van:
U.S. Geological Survey, Mineral Commodity Summaries, 2016.
Vervaardiging van lood
Bijna de helft van het geraffineerde lood in de wereld is afkomstig van looderts, de andere helft van secundaire (schroot) loodbronnen. China en Australië hebben de grootste hoeveelheden looderts en zijn ook de grootste primaire producenten van het metaal. Canada, de VS en Peru hebben kleinere maar significante hoeveelheden van de ertsen.
|
Het belangrijkste looderts is galena (PbS). Andere belangrijke ertsen, zoals cerrusiet (PbCO3) en anglesiet (PbSO4), kunnen worden beschouwd als verweerde producten van galena en worden gewoonlijk dichter bij de oppervlakte gevonden.
De primaire produktie van lood omvat drie fasen:
a) ertsconcentratie
b) smelten
c) raffinage
a) ertsconcentratie
Lood- en zinkertsen (gewoonlijk sfaleriet, ZnS) komen vaak samen voor en kunnen ook zilver, koper en goud bevatten. Het erts moet eerst worden gescheiden van klei en andere silicaten (“ganggesteente”), waarna het looderts en het zinkerts worden gescheiden.
Het gebruikte proces is schuimflotatie, een opeenvolging van stappen die elk een grotere concentratie van het looderts opleveren. Het erts, dat ganggesteente bevat (gewoonlijk 3-8% lood), wordt met water vermalen tot een deeltjesgrootte vergelijkbaar met die van fijn zand (<0,25 mm). Dit wordt vervolgens gemengd met water en een schuimmiddel (een detergent) en heftig door lucht geroerd om een fijne suspensie te vormen met een schuim van belletjes aan de bovenkant. Het proces wordt uitgevoerd in een reeks tanks. Aangezien de lood- en zinkmineralen minder gemakkelijk worden bevochtigd dan het ganggesteente, hechten zij zich aan de luchtbellen die naar het oppervlak worden gevoerd. De rotsdeeltjes zinken en de lood- en zinkertsen worden afgeroomd.
Daarna wordt het looderts gescheiden van het zinkerts. Men voegt een in water oplosbare chemische stof toe, zinksulfaat genaamd, die het zinkerts doet zinken en het looderts doet afschuimen. Later wordt een chemische stof zoals koper(II)sulfaat toegevoegd en het zinkerts blijft nu drijven en wordt afgeroomd.
Het loodertsconcentraat uit de flotatietanks bevat nu ongeveer 50% lood en ca 0,1% zilver, een relatief kleine maar waardevolle hoeveelheid.
(b) Smelten
Smelten is gewoonlijk een tweefasenproces zoals hier beschreven, hoewel er ook eenfasige methoden worden gebruikt met een lager energieverbruik en lagere emissies.
Na menging met kalksteen wordt het gefilterde geconcentreerde erts geroosterd in lucht of met zuurstof verrijkte lucht op een bewegende band. Het grootste deel van de sulfide wordt omgezet in lood(II)oxide:
Zwaveldioxidegas kan dan worden gereinigd en gebruikt om zwavelzuur te maken.
Het lood(II)oxide wordt verhit en tot brokken gemaakt, een proces dat sinteren wordt genoemd. De brokken (de sinter) worden gebroken en gesorteerd tot een geschikte grootte voor latere behandeling in een hoogoven, die qua constructie vergelijkbaar is met die voor het maken van ijzer, maar dan kleiner.
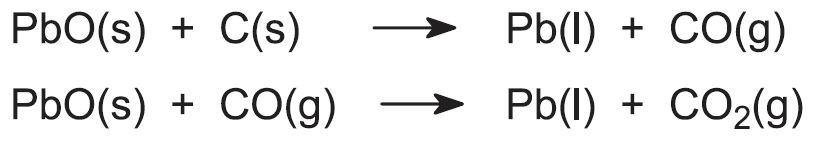
De gesorteerde sinter (elke klomp ongeveer zo groot als een vuist) wordt gemengd met ongeveer 7% van zijn massa in cokes en kalksteen. De cokes wordt toegevoegd voor twee doeleinden, enerzijds als reductiemiddel en anderzijds als warmtebron wanneer zij reageert met de lucht die, zoals bij de vervaardiging van ijzer, in de oven wordt gepompt. De kalksteen levert materiaal voor het smeltmiddel dat de onzuiverheden, de slakken, bevat. Het mengsel wordt boven in de hoogoven gebracht, en het lood(II)oxide wordt gereduceerd tot gesmolten lood. Koolstof en koolmonoxide, afkomstig van de cokes, zijn de reductiemiddelen:
Het gesmolten lood wordt onderaan de oven afgetapt en ofwel in blokken van 4 ton gegoten, ofwel in een ‘voorraadketel’ gedaan, die het metaal gesmolten houdt voor het raffinageproces.
Het product bevat ongeveer 99,5% lood, de resterende 0,5% bestaat hoofdzakelijk uit antimoon en zilver met kleinere hoeveelheden andere metalen, waaronder goud. Omdat het in dit stadium zilver en goud bevat, wordt het lood ongemunt lood genoemd.
De smeltmiddelen vormen een gesmolten slak van metaaloxiden en silicaten die bovenop blijft drijven. De slak bevat veel van het zink dat in het erts is achtergebleven en wordt later behandeld om metallisch zink te produceren.
Smelten kan ook worden gedaan met behulp van een lans waar olie en met zuurstof verrijkte lucht met hoge snelheid doorheen gaan en turbulente omstandigheden vormen. Er bestaan verschillende van dergelijke processen onder namen als Isasmelt, Ausmelt en Sirosmelt. Het éénstapsproces, Isasmelt, wordt aan het eind van dit hoofdstuk besproken.
(c) Raffineren
Het edelmetaal wordt verhit tot net boven het smeltpunt. Vast koper en kopersulfide komen aan de oppervlakte en worden afgeschuimd.
Arseen wordt vervolgens verwijderd door het lood met een luchtstroom om te roeren en de resulterende slak, die arseenoxiden bevat, af te schuimen.
Zilver wordt verwijderd met een techniek die bekend staat als het Parkes-proces. Ongeveer 2% zink wordt aan het lood toegevoegd en een zilverrijke zinkkorst vormt zich en wordt verwijderd. Vervolgens wordt meer zink toegevoegd bij 740 K (het mp is 693 K) en het bad wordt afgekoeld tot net boven het smeltpunt. Tijdens het afkoelen scheidt zich een vaste zilver/zinkkorst af, die naar de oppervlakte stijgt en voortdurend wordt verwijderd.
Het Parkes-proces hangt af van het volgende:
- lood en zink zijn vlak boven hun smeltpunten bijna onmengbaar
- zilver is veel beter oplosbaar in zink dan in lood
- zilver/zink-legeringen hebben hogere smeltpunten dan zuiver zink.
Bij 863 K wordt zink verwijderd door het lood over te brengen in een “ontzinkketel”. In dit stadium bevat het ontzilverde lood ongeveer 0,6% zink en 0,0004% zilver. Het ontzinken gebeurt door vacuümdestillatie bij 860 K wanneer het zink verdampt.
Tot slot worden alle sporen van antimoon en zink verwijderd door bij 760 K natriumhydroxide te mengen met gesmolten lood (het smeltpunt is 600 K). Het resulterende natriumzinkaat en antimonaat vormen een huid op het oppervlak van het gesmolten lood, die wordt afgeschuimd. Het geraffineerde lood heeft een zuiverheid van 99,99%.
Secundaire productie
Wereldwijd is meer dan 50% van het jaarlijks gebruikte lood afkomstig van gerecycleerde bronnen. Meer dan 90% van het lood dat in de VS wordt gebruikt, is zelfs afkomstig van gerecycled metaal.
| Wereld | 5,5 miljoen ton |
| China | 1,5 miljoen ton |
| V.S. | 1.1 miljoen ton |
| India | 340 000 ton |
| Duitsland | 290 000 ton |
| Mexico | 205 000 ton |
| Brazilië | 188 000 ton |
Gegevens uit:
International Lead Association, 2012.
Lood voor recycling kan de vorm aannemen van schroot (dakbedekkingsplaat, bijvoorbeeld), of van loodverbindingen, zoals de pasta’s van lood-zuurbatterijen. Zuiver metallisch lood kan rechtstreeks worden gesmolten en geraffineerd, maar verbindingen en loodlegeringen moeten worden gesmolten, met gebruikmaking van processen die vergelijkbaar zijn met die voor loodertsen.
Twee-fasen-proces
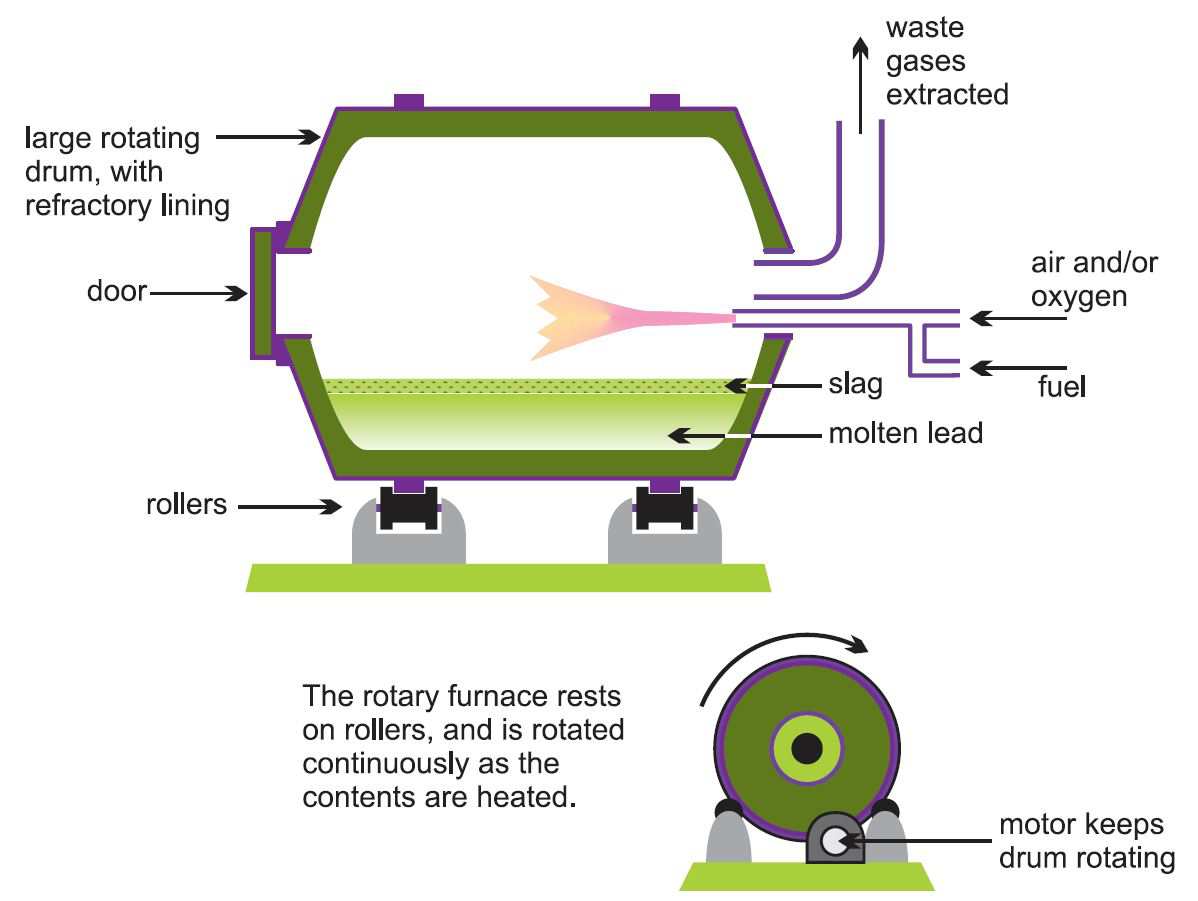
In het twee-fasen-proces voor secundaire productie worden kleinere roterende of reverberatoire ovens (figuur 3) gebruikt in plaats van grotere hoogovens, omdat dit een betere controle van de kwaliteit van het lood geeft. Roterende ovens kunnen lood in bijna elke vorm aanvaarden en kunnen gebruik maken van veel verschillende koolstofbronnen (aardgas, olie en cokes) voor de reductie.
In de eerste fase wordt zeer weinig reductiemiddel gebruikt en zodra de oven is verwarmd, smelt alle metallisch lood en kan het na een paar uur worden afgetapt. Dit heeft een hoge zuiverheid, aangezien andere materialen, waaronder loodverbindingen, in de slak achterblijven. Er wordt nog meer schroot toegevoegd en het proces wordt herhaald totdat er voldoende slak is ontstaan voor de tweede fase.
De tweede fase omvat de reductie van de slak met behulp van een reductiemiddel op basis van koolstof. Natriumcarbonaat (“soda ash”) of calciumcarbonaat wordt ook toegevoegd als een “flux” om te helpen de slak van onzuiverheden te ontdoen. Loodoxiden, loodsulfaat en eventuele antimoonoxiden worden gereduceerd, en het resultaat is “antimoonlood”, dat ook wat bismut en zilver kan bevatten. Het antimoon (2-5%) geeft het lood een grotere sterkte.
Figuur 3 Illustratie van een roterende oven, hier gebruikt bij de secundaire productie van lood.
Eenstapsproces
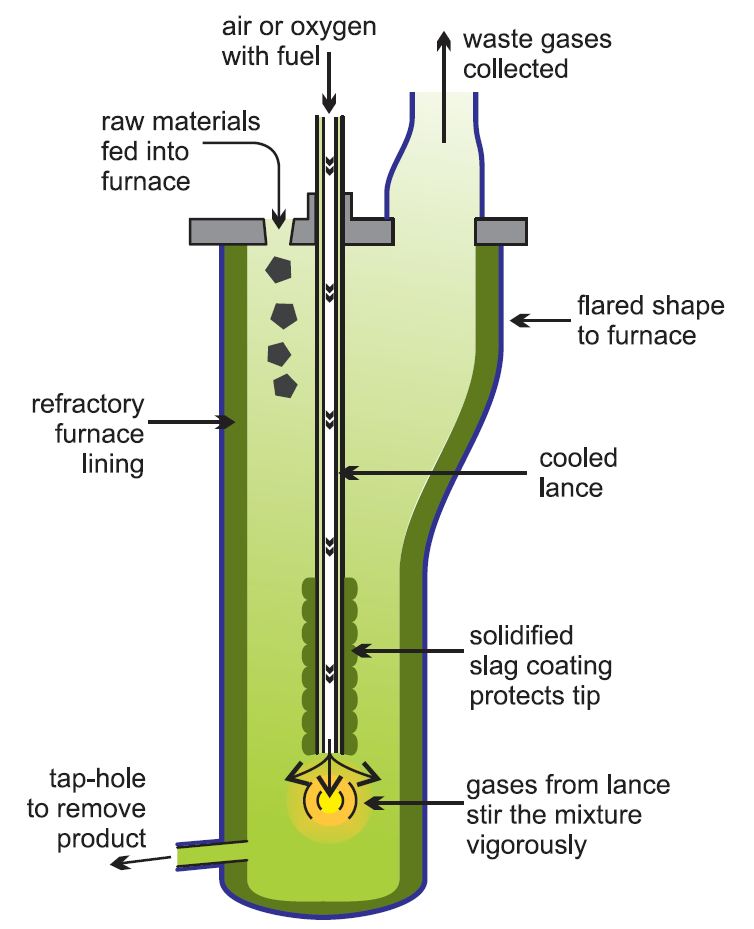
Het Isasmelt-proces, figuur 4, is een voorbeeld van een van de modernste methoden van secundaire loodproductie waarbij een eenstapsproces wordt gebruikt, met name voor de verwerking van de pasta uit batterijen. Dit wordt in een oven gevoerd en gesmolten met behulp van een lans waardoor een mengsel van olie en met zuurstof verrijkte lucht wordt toegevoerd. Het is economischer om met zuurstof verrijkte lucht te gebruiken in plaats van lucht, aangezien dit de reactiesnelheid verhoogt en betekent dat kleinere chemische installaties kunnen worden gebruikt en de brandstofkosten worden verlaagd. Voorts is het gemakkelijker ervoor te zorgen dat geen gassen zoals zwaveldioxide verloren gaan en de atmosfeer verontreinigen. Op het terrein worden zuurstofinstallaties gebouwd.
Figuur 4 De productie van secundair lood met behulp van het Isasmelt-procédé.
In de volgende 36 uur wordt meer pasta, samen met steenkool als reductiemiddel, in de oven gevoerd bij ongeveer 1250 K en wordt om de paar uur lood met een zuiverheid van 99,9% afgetapt.
Later worden vloeimiddelen toegevoegd en wordt de temperatuur verhoogd tot 1500 K. Hierdoor wordt de slak gereduceerd, wat opnieuw antimonialen lood oplevert.
Het Isasmelt-proces heeft een hoger thermisch rendement, en de overblijvende afvalslak heeft een lager restloodgehalte.
Het proces wordt ook gebruikt voor primaire loodproductie.