Die Kenntnis der Anatomie und Elektrophysiologie des Erregungsleitungssystems des Herzens von der atrioventrikulären (AV) Kreuzung bis zu den distalen Purkinje-Fasern ist für das Verständnis der Pathophysiologie des Linksschenkelblocks (LBBB) von wesentlicher Bedeutung.
Embryologie
Während der Kardiogenese ist die Differenzierung in arbeitende Muskelzellen und das Reizleitungssystem nach wie vor Gegenstand von Diskussionen. Es wurden Hypothesen entwickelt, die einzeln oder in Kombination dieses komplexe Thema erklären könnten. Die Komponenten des Herzschrittmachers und des Reizleitungssystems sind in Bezug auf Funktion, Morphologie und molekularen Phänotyp nicht einheitlich. Es haben sich mehrere Modelle und Theorien herausgebildet. Die Vier-Ring-Theorie beschreibt vier Ringe des Reizleitungssystems innerhalb des Herzschlauchs, die sich in Komponenten des Schrittmacher- und Reizleitungssystems differenzieren. Das Rekrutierungsmodell geht davon aus, dass einige Kardiomyozyten schon früh für das Erregungsleitungssystem bestimmt sind. Das Spezifikationsmodell geht davon aus, dass die primären Herzmuskelzellen entweder Gene für das Reizleitungssystem oder für den Arbeitsmyozyten exprimieren.
Anatomie
Das spezialisierte Reizleitungssystem des Herzens besteht aus Zellen, die elektrische Impulse schneller leiten als das umgebende Myokard. Das Erregungsleitungssystem kann in verschiedene anatomische Segmente unterteilt werden, und jedes Segment wird der Reihe nach beschrieben, beginnend mit der AV-Kreuzung und endend mit den Purkinje-Fasern.
Die AV-Kreuzung wird traditionell in drei Regionen unterteilt: Übergangszone, AV-Knoten und durchdringender Teil des AV-Bündels (His-Bündel, gemeinsames Bündel).
Die Übergangszone ist der Bereich, in dem der rechte Vorhof mit dem kompakten AV-Knoten über diskrete Vorhofbahnen, die sogenannten langsamen und schnellen Bahnen, verschmilzt. In der Vergangenheit wurde angenommen, dass die langsamen und schnellen Bahnen parallel verlaufen. Daten aus der Radiofrequenzablation von AV-Knoten- und AV-Reentrant-Tachykardien haben jedoch gezeigt, dass die langsame Bahn enger mit dem anterior-superioren Aspekt des Os coronare sinus verbunden ist. Außerdem zeigen die Daten, dass die schnelle Bahn leicht superior und posterior zum AV-Knoten liegt.
Das nächste Segment ist der AV-Knoten, der anterior und superior zum Ostium des Koronarsinus liegt, direkt über der Insertion des Septumblättchens der Trikuspidalklappe. Dieser Bereich befindet sich an der Spitze des Koch’schen Dreiecks, das durch den Trikuspidalanulus, die Todaro-Sehne und das Ostium des Sinus coronarius gebildet wird. Die Blutversorgung des AV-Knotens erfolgt über die AV-Knotenarterie, die bei 85 %-90 % der Menschen ein Ast der rechten Koronararterie und bei 10 %-15 % der Menschen ein Ast der linken zirkumflexen Koronararterie ist.
An der Spitze des Koch-Dreiecks wird der kompakte AV-Knoten zum durchdringenden His-Bündel. Es durchdringt den zentralen Faserkörper am Ansatz der Todaro-Sehne, verläuft zwischen dem membranösen Septum und dem muskulären Septum und verzweigt sich am Kamm des muskulären Ventrikelseptums. Das His-Bündel ist in drei anatomische Segmente unterteilt. Das proximale oder nicht-penetrierende Segment liegt distal zum AV-Knoten und proximal zum zentralen Faserkörper. Das mittlere oder durchdringende Segment durchdringt den zentralen Faserkörper und verläuft posterior zum membranösen Septum. Das distale oder verzweigte Segment verzweigt sich am Kamm des Muskelseptums in den rechten und den linken Bündelast (siehe Abbildung unten).
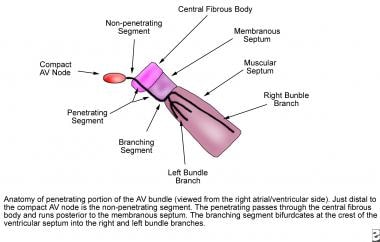 Dieses Bild zeigt die Anatomie des penetrierenden Teils des atrioventrikulären (AV) Bündels.
Dieses Bild zeigt die Anatomie des penetrierenden Teils des atrioventrikulären (AV) Bündels. Der rechte Bündelast, eine direkte Fortsetzung des penetrierenden Bündels, entspringt distal der Verbindung des Septumblättchens der Trikuspidalklappe mit dem membranösen Septum und liegt auf dem rechten Ventrikelseptum knapp unterhalb des Papillarmuskels des Conus. Er ist unverzweigt und verläuft in Richtung der Spitze des rechten Ventrikels entlang des hinteren Randes des Septumbandes, verläuft durch das Moderatorband zur Basis des vorderen Papillarmuskels und verläuft zur freien Wand des rechten Ventrikels.
Der LBB hat seinen Ursprung am Kamm des muskulären Ventrikelseptums knapp distal des membranösen Septums. Sie entspringt fächerförmig und verläuft inferior entlang der linken Ventrikelseptumoberfläche unterhalb des nichtkoronaren Höckers der Aortenklappe. Der LBB verzweigt sich normalerweise in drei Hauptfaszikel. Der anteriore Faszikel ist zur Basis des anterolateralen Papillarmuskels gerichtet, der posteriore Faszikel zur Basis des posteromedialen Papillarmuskels, und in 60 % der Herzen verläuft ein zentraler Faszikel zur Midseptalregion. Wenn kein zentraler Faszikel vorhanden ist, wie bei 40 % der Herzen, wird die Midseptalregion durch Ausstrahlungen des anterioren Faszikels oder des vorderen und hinteren Faszikels versorgt.
Am Ende jedes Bündelastes sind die Purkinje-Fasern auf der endokardialen Oberfläche beider Ventrikel miteinander verflochten und konzentrieren sich in der Regel an den Spitzen der Papillarmuskeln.
Elektrophysiologie der kardialen Reizleitung
Das Herz ist eine zweistufige mechanische Pumpe, die durch präzise getaktete elektrische Impulse koordiniert wird. Damit die Pumpe optimal funktioniert, ermöglichen aufeinanderfolgende Depolarisationen der Vorhöfe und dann der Kammern eine Vorhofkontraktion, die für eine vollständige diastolische Füllung der Kammern sorgt (AV-Synchronität). Nach der Füllung der Ventrikel ermöglicht eine rasche Aktivierung des ventrikulären Myokards eine synchronisierte Kontraktion, um das Blut möglichst effektiv in die großen Gefäße auszustoßen.
Normale kardiale Erregungsleitung
Bei der normalen kardialen Erregungsleitung verläuft die elektrische Erregung des Herzens sequenziell von den Vorhöfen zu den Herzkammern und wird im Oberflächen-Elektrokardiogramm (EKG) dargestellt (siehe Abbildung unten).
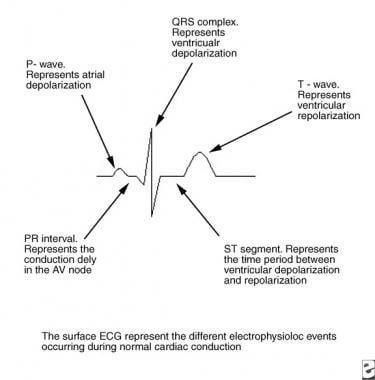 Dieses Bild zeigt die elektrophysiologischen Ereignisse bei der normalen kardialen Erregungsleitung. AV = atrioventrikulär; EKG = Elektrokardiogramm.
Dieses Bild zeigt die elektrophysiologischen Ereignisse bei der normalen kardialen Erregungsleitung. AV = atrioventrikulär; EKG = Elektrokardiogramm. Der im Sinusknoten erzeugte elektrische Impuls durchläuft die Vorhöfe (erkennbar an der P-Welle im EKG) und erreicht den AV-Knoten. Während der Impuls den AV-Knoten durchläuft, verlangsamt sich die Erregungsleitung, so dass Zeit für die Vorhofkontraktion zur Verfügung steht, bevor der Ventrikel aktiviert wird (PR-Segment). Nachdem der Impuls den kompakten AV-Knoten passiert hat, wird er schnell durch das Herzzentrum zu den Ventrikeln geleitet, und zwar über das His-Bündel (penetrierendes Bündel) zum Verzweigungsbündel, den Bündelästen, den distalen Purkinje-Fasern und schließlich zu den ventrikulären Herzmuskelzellen (enger QRS-Komplex).
Die Anatomie des LBB ist variabel. Der Ursprung des LBB ist bei einigen breit und bei anderen schmal (zwischen < 1 mm und 14 mm) und wird wesentlich durch die anatomische Beziehung des His-Bündels zum Ventrikelseptum beeinflusst. Auch die Unterteilung des LBB ist sehr unterschiedlich. Einige Studien legen eine trifaszikuläre Aufteilung des LBB in einen vorderen, hinteren und septalen Ast nahe. Für Kliniker und Elektrophysiologen hat sich das Konzept der bifaszikulären (anteriorer und posteriorer Faszikel) LBB bewährt. In einem normalen Herzen führt der vom His-Bündel ausgehende elektrische Impuls zu einer parallelen und unabhängigen Aktivierung beider Ventrikel, während das Ventrikelseptum in einer Richtung von links nach rechts aktiviert wird. Das reichhaltige Purkinjie-Netzwerk auf jeder Seite leitet den elektrischen Impuls an die Herzmuskelzellen weiter.
Arten des Linksschenkelblocks
Der vollständige LBBB tritt auf, wenn der elektrische Impuls entweder im Haupt-LBB oder sowohl im vorderen als auch im hinteren Faszikel verzögert oder unterbrochen ist. Die Erregungsleitung im rechten Bündelast verläuft normal, und der rechte Ventrikel depolarisiert sich auf normale Art und Weise. Bei einem vollständigen LBBB verläuft die Erregungsleitung vom rechten Ventrikel zunächst zum Interventrikelseptum, dann zu den vorderen und hinteren Teilen des linken Ventrikels und schließlich zur linken freien Seitenwand. Die verzögerte linksventrikuläre Depolarisation ist der Grund für die EKG-Befunde beim Linksschenkelblock (siehe die nachstehenden Abbildungen).
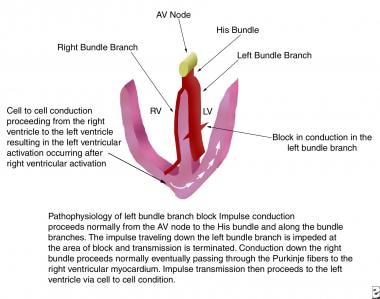 Dieses Bild stellt die Pathophysiologie des Linksschenkelblocks dar. AV = atrioventrikulär; LV = linker Ventrikel; RV = rechter Ventrikel.
Dieses Bild stellt die Pathophysiologie des Linksschenkelblocks dar. AV = atrioventrikulär; LV = linker Ventrikel; RV = rechter Ventrikel. 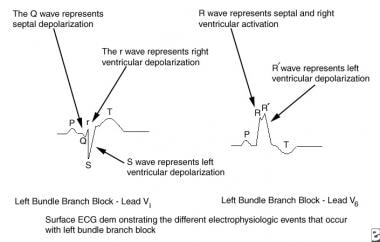 Dieses Bild zeigt die elektrophysiologischen Ereignisse des Linksschenkelblocks. EKG = Elektrokardiogramm.
Dieses Bild zeigt die elektrophysiologischen Ereignisse des Linksschenkelblocks. EKG = Elektrokardiogramm. Der inkomplette LBBB tritt in zwei Formen auf, die jeweils als Hemiblock bezeichnet werden. Beim linken vorderen Hemiblock (LAH) verläuft die Übertragung des elektrischen Impulses entlang des Haupt-LBB und des hinteren Faszikels normal, ist aber im vorderen Faszikel blockiert oder verzögert. Diese Blockade führt zu einer verzögerten Aktivierung des vorderen Teils des linken Ventrikels. Bei LAH kann die Dauer des QRS-Komplexes normal oder nur geringfügig verlängert sein, da die Erregungsleitung im rechten und linken Hauptbündel und im linken posterioren Faszikel normal schnell verläuft. Darüber hinaus ist der QRS-Komplex in der Frontalebene nach oben gerichtet. Dies wird als Linksachsenabweichung bezeichnet, obwohl der Begriff Superiorachsenabweichung den Befund am genauesten beschreibt. Außerdem ist die QRS-Achse normalerweise nach links gerichtet; daher ist der Begriff Linksachsenabweichung semantisch wenig sinnvoll.
Beim linken hinteren Hemiblock verläuft die Übertragung des elektrischen Impulses entlang des Haupt-LBB und des vorderen Faszikels normal, ist aber im hinteren Faszikel blockiert. Diese Blockade führt zu einer verzögerten Aktivierung des hinteren linken Ventrikels. Der QRS-Komplex ist wieder von normaler oder nur geringfügig verlängerter Dauer und weist in der Frontalebene eine nach rechts gerichtete Achse auf. Ein linker posteriorer Hemiblock wird bei Kindern selten beobachtet, und die Diagnose ist schwierig, da bei Kindern mit angeborenen Herzerkrankungen und rechtsventrikulärer Hypertrophie häufig eine Abweichung der rechten Achse vorliegt.