Mehak Pahwa*, BS Sidhu, Rajnish Raj and Eish Kumar
Department of Psychiatry, Government Medical College, Patiala, India
Corresponding Authoring Author: Dr. Mehak Pahwa (garg)
Junior Resident Psychiatrii
Department of Psychiatry, Government Medical College, Patiala, India
Tel: 91 905 188 8070
E-mail:
Received date: May 29, 2015; Accepted date: August 06, 2015; Published date: August 12, 2015
Citation: Pahwa M, Sidhu BS, Raj R, Kumar E (2015) Tramadol vs. Buprenorphine for the Treatment of Opioid Dependence: A Comparative Study. J Addict Res Ther 6:239. doi:10.4172/2155-6105.1000239
Copyright: © 2015 Pahwa M, et al. This is an open-access article distributed under the terms of the Creative Commons Attribution License, which permits unrestricted use, distribution, and reproduction in any medium, provided the original author and source are credited.
Visit for more related articles at Journal of Addiction Research & Therapy
Abstract
Background: Tramadol jest atypowym, działającym ośrodkowo syntetycznym lekiem przeciwbólowym, a jego o-demetylowany metabolit, (+)-o-demetylotramadol (znany jako m1), ma większe powinowactwo do receptora mu-opioidowego, co czyni go kandydatem do leczenia odstawienia opiatów. Cel: Porównanie efektów i względnej użyteczności klinicznej tramadolu i buprenorfiny w leczeniu odstawienia heroiny u pacjentów uzależnionych od opioidów.
Metody: W randomizowanym badaniu otwartej etykiety z grupą równoległą, 70 pacjentów z uzależnieniem od opioidów z dziennym zużyciem heroiny równym 1-10 mg, 10-20 mg, >20 mg metadonu przy użyciu stratyfikowanego proporcjonalnego doboru próby zostało przydzielonych do dwóch grup leczenia tj. Tramadolu i Buprenorfiny. Stosowano elastyczny schemat dawkowania, a lek był miareczkowany przy użyciu (COWS) Klinicznej Skali Odstawienia Opiatów i (CGI) Klinicznej Globalnej Impresji
Wyniki: Stwierdzono istotną statystycznie różnicę pomiędzy obiema grupami u pacjentów z umiarkowanym poziomem uzależnienia, u których 78% pacjentów z grupy Tramadolu i 57% z grupy Buprenorfiny ukończyło detoksykację na koniec 12 tygodni. Natomiast pacjenci z ciężkim stopniem uzależnienia musieli być utrzymywani na buprenorfinie, a detoksykacja nie mogła być zakończona z wysokim odsetkiem rezygnacji w grupie tramadolu
Dyskusja: Tramadol ma dobrą skuteczność w detoksykacji i zapobieganiu nawrotom u pacjentów z umiarkowanym stopniem uzależnienia od opioidów w porównaniu z buprenorfiną, natomiast buprenorfina jest lepsza w leczeniu podtrzymującym i ma większą użyteczność kliniczną w ciężkim stopniu uzależnienia od opioidów, gdzie wymagane jest leczenie podtrzymujące.
Wprowadzenie
W ciągu ostatnich trzydziestu lat w leczeniu odstawienia opioidów stosowano wiele leków, w tym metadon, LAAM, propoksyfen, klonidynę, buprenorfinę podawaną pozajelitowo, a ostatnio także buprenorfinę podawaną podjęzykowo. Stwierdzono, że każda z nich ma swoje zalety i ograniczenia kliniczne. Tramadol jest atypowym, działającym ośrodkowo syntetycznym lekiem przeciwbólowym. W swojej macierzystej postaci tramadol występuje jako racemiczna mieszanina dwóch aktywnych enancjomerów, które ulegają biotransformacji wątrobowej, tworząc N- i O-demetylowane związki. O-demetylowany metabolit, (+)-O-demetylotramadol (znany jako M1), ma większe powinowactwo do receptora mu-opioidowego niż związek macierzysty i jest odpowiedzialny za aktywność mu-opioidową tramadolu, która wynika przede wszystkim z jego wiązania się z mikroreceptorem. Pomimo tej aktywności mikroreceptora, tramadol wydaje się mieć niski potencjał nadużywania i został zatwierdzony jako nieplanowany środek przeciwbólowy w USA w 1994 r. w oparciu w dużej mierze o doświadczenia epidemiologiczne, a szereg badań na zwierzętach i ludziach sugeruje, miał niski potencjał nadużywania. Profil farmakologiczny tramadolu czyni go kandydatem do leczenia odstawienia opiatów; natomiast buprenorfina ma wysoki potencjał nadużywania.
Cele i zadania
Porównanie efektów i względnej użyteczności klinicznej tramadolu i buprenorfiny w leczeniu odstawienia heroiny u pacjentów uzależnionych od opioidów.
Materiały i metody
– Randomizowane, otwarte, równoległe badanie grupowe przeprowadzono w oddziale leczenia uzależnienia w szpitalu trzeciego stopnia w Indiach (Punjab)
– Kryteria włączenia do badania to płeć męska, heroina jako narkotyk z wyboru, aktualne uzależnienie fizyczne od opioidów (tj, objawy odstawienne), oraz nie nadużywanie doustnych opioidowych leków przeciwbólowych.
– Kryteria wyłączenia obejmowały płeć żeńską, poważną chorobę psychiczną (np. schizofrenię), istotny problem medyczny (np, historia napadów drgawkowych lub nadciśnienia tętniczego), brak innego równoczesnego nadużywania leków, tj. alkoholu lub benzodiazepin.
– 82 mężczyzn Pacjentów w grupie wiekowej od 20 do 50 lat, którzy spełnili kryteria włączenia, podzielono na trzy grupy jako łagodne, umiarkowane i ciężkie na podstawie ilości dziennego zażywania heroiny, tj.tj. <10 mg metadonu równoważnego, 10-20 mg metadonu równoważnego i >20 mg metadonu równoważnego.
– Było 35 pacjentów, którzy spełnili kryteria łagodnego używania narkotyków, 32 dla umiarkowanego i 15, które spełniły kryteria ciężkiego używania narkotyków. Spośród tych pacjentów dobrano cechy socjodemograficzne i dokonano proporcjonalnego losowania warstwowego, a pacjentów przydzielono losowo do dwóch grup leczenia (tj. tramadol i buprenorfina) w każdej kategorii.
– Odpadło 12 osób, pozostawiając całkowitą liczbę pacjentów na poziomie 70: 30 w grupie łagodnej (po 15 osób w każdej kategorii), 28 w grupie umiarkowanej (po 14 osób w każdej kategorii) i 12 w grupie ciężkiej (po 6 osób w każdej kategorii).
– Wykonywano badania podstawowe i po 8-12 godzinach od ostatniego przyjęcia heroiny rozpoczynano leczenie 2 mg buprenorfiny i 100 mg tramadolu, które stopniowo zwiększano, jak na objawy odstawienia u pacjenta.
– Stosowano elastyczny schemat dawkowania, a dawkę miareczkowano na podstawie obiektywnej i subiektywnej oceny za pomocą Klinicznej Skali Odstawienia Opiatów (COWS) i Ogólnego Wrażenia Klinicznego (CGI) .
– Pacjenci byli poddawani detoksykacji w warunkach szpitalnych, a następnie intensywnemu leczeniu ambulatoryjnemu. Pomiary przy użyciu COWS i CGI były wykonywane w każdym naprzemiennym tygodniu, a pacjenci byli obserwowani przez 12 tygodni.
Wyniki
W grupie łagodnej (1-10 mg ekwiwalentu metadonu): z 15 pacjentów w każdej kategorii pacjentów, 8(53.33%) pacjentów osiągnęło wczesną pełną remisję i 5(33.33%) wczesną częściową remisję w grupie tramadolu i 36%, 46.66% odpowiednio w grupie buprenorfiny. Umiarkowana (10- 20mg ekwiwalentu metadonu): spośród 14 pacjentów w grupie tramadolu: wczesną pełną remisję uzyskało 5 (35,71), a częściową 6 (42,85%), co daje łącznie 78,57%, natomiast w grupie buprenorfiny 3 (21,42%) pacjentów uzyskało pełną remisję, a 5 (53,17%) częściową, co daje łącznie 57,14% remisji. Różnica między tymi dwoma grupami wynikała z wysokiego odsetka nawrotów w grupie buprenorfiny po detoksykacji, który wynosił 28,57%. Ciężką (>20 mg metadonu) chorobę tylko u 16,6% pacjentów można było utrzymać w grupie tramadolu, podczas gdy 66,66% pacjentów utrzymało się na buprenorfinie pod koniec 12 tygodni. Pacjenci leczeni tramadolem mieli wyższy średni poziom objawów odstawiennych w porównaniu z grupą buprenorfiny oraz większą redukcję objawów odstawiennych w czasie. W grupie tramadolu średnie maksimum COWS w 1. tygodniu wynosiło 36, a w grupie buprenorfiny 24 (p=0,001), natomiast w 12. tygodniu COWS max wynosiło 3 w grupie tramadolu i 8 w grupie buprenorfiny (p<0.05) (ryc. 1), co wskazuje na stopniowe zmniejszanie się objawów odstawiennych w grupie tramadolu i brak nasilenia objawów odstawiennych po odstawieniu leku w porównaniu z nagłym zmniejszeniem się objawów odstawiennych w grupie buprenorfiny, po którym następowało nasilenie objawów odstawiennych przy zmniejszaniu dawki lub po odstawieniu leku (ryc. 2 i 3) (tab. 1).
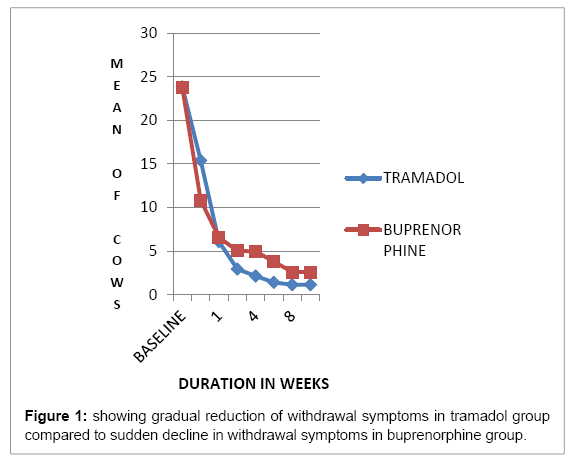
Rycina 1: przedstawiająca stopniowe zmniejszanie się objawów odstawiennych w grupie tramadolu w porównaniu z nagłym zmniejszeniem się objawów odstawiennych w grupie buprenorfiny.

Rysunek 2: przedstawiający porównanie średniej punktacji skali globalnego wrażenia klinicznego w dwóch grupach.
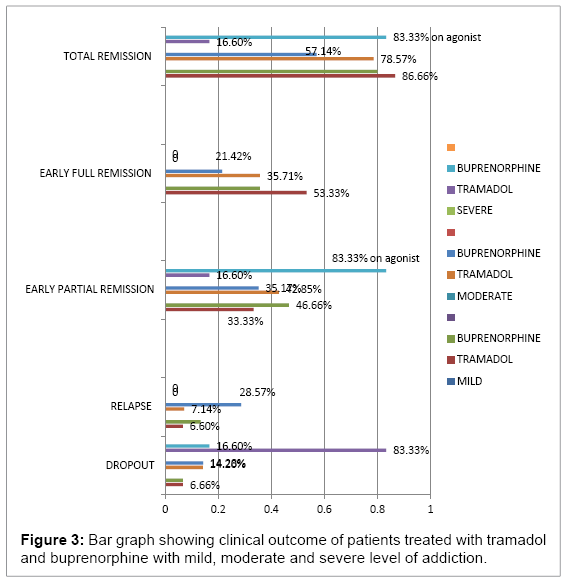
Rysunek 3: Wykres słupkowy przedstawiający wyniki kliniczne pacjentów leczonych tramadolem i buprenorfiną z łagodnym, umiarkowanym i ciężkim stopniem uzależnienia.
| CGI | Tramadol | Buprenorfina | ||||
|---|---|---|---|---|---|---|
| Grupa umiarkowana | MEAN | SD | MEAN | SD | t | P |
| PodstawoweCGI-.S | 10.26 | 25.11 | 10.33 | 25.08 | -0.56 | 0.5 |
| 2 tygodnie CGI-I | 9.20 | 25.40 | 8.66 | 25.55 | 3.22 | 0,006* |
| 12 tygodni CGI-I | 8,066 | 25,72 | 9.133 | 25,45 | -2,41 | 0,02* |
Tabela 1: Test T: Wyniki CGI w grupie umiarkowanego poziomu uzależnienia.
Wnioski
– Tramadol wydaje się mieć porównywalną skuteczność kliniczną jak buprenorfina w leczeniu pacjentów z niskim poziomem uzależnienia od opioidów
– Pacjenci z umiarkowanym poziomem uzależnienia; tramadol ma większą skuteczność w detoksykacji i zapobieganiu nawrotom przy minimalnym potencjale nadużywania.
– Pacjenci z ciężką i trwałą postacią uzależnienia częściej mają współwystępujące schorzenia psychiatryczne i zazwyczaj wymagają długotrwałego kompleksowego leczenia, a u takich pacjentów indukcja i podtrzymywanie leczenia buprenorfiną mogą być skuteczniejsze niż detoksykacja w celu zaangażowania i utrzymania pacjentów w kompleksowym ambulatoryjnym leczeniu uzależnień.
– Detoksykacja z elastycznym schematem dawkowania i dostosowaniem leczenia do indywidualnych potrzeb przynosi lepsze wyniki w porównaniu z szybką lub bardzo szybką detoksykacją z zastosowaniem stałej dawki.
Podsumowanie/Dyskusja
– Tramadol ma dobrą skuteczność w detoksykacji i zapobieganiu nawrotom u pacjentów z umiarkowanym stopniem uzależnienia od opioidów w porównaniu z buprenorfiną.
– Natomiast buprenorfina jest lepsza w leczeniu podtrzymującym i ma większą użyteczność kliniczną w ciężkim stopniu uzależnienia od opioidów, gdzie wymagane jest leczenie podtrzymujące.
– Ustalenia te, jeśli zostaną powtórzone w większych badaniach z lepszymi projektami badawczymi, mają potencjalnie duże znaczenie dla postępowania w przypadku odstawienia opioidów zarówno w warunkach szpitalnych, jak i ambulatoryjnych.
- Raffa RB, Friderichs E, Reimann W, Shank RP, Codd EE, et al. (1993) Complementary and synergistic antinociceptive interaction between the enantiomers of tramadol. J Pharmacol Exp Ther 267: 331-340.
- Preston KL, Jasinski DR, Testa M (1991) Abuse potential and pharmacological comparison of tramadol and morphine. Drug Alcohol Depend 27: 7-17.
- Camí J, Lamas X, Farré M (1994) Acute effects of tramadol in methadone-maintained volunteers. Drugs 47 Suppl 1: 39-43.
- Lanier RK, Lofwall MR, Mintzer MZ, Bigelow GE, Strain EC (2010) Physical dependence potential of daily tramadol dosing in humans. Psychopharmacology (Berl) 211: 457-466.
- Tamaskar R, Parran TV Jr, Heggi A, Brateanu A, Rabb M, et al. (2003) Tramadol versus buprenorfina for the treatment of opiate withdrawal: a retrospective cohort control study. J Addict Dis 22: 5-12.
- Lofwall MR, Walsh SL, Bigelow GE, Strain EC (2007) Modest opioid wycofania suppression efficacy of oral tramadol in humans. Psychopharmacology (Berl) 194: 381-393.
- Wesson DR, Ling W (2003) The Clinical Opiate Withdrawal Scale (COWS). J Psychoactive Drugs 35: 253-259.
- Sobey PW, Parran TV Jr, Grey SF, Adelman CL, Yu J (2003) The use of tramadol for acute heroin withdrawal: a comparison to clonidine. J Addict Dis 22: 13-25.
- Seivewright N (2000) Community treatment of drug misuse: more than methadone. Cambridge University Press.
- RCGP (2004) Guidance for the use of buprenorphine for the treatment of opioid dependence in primary care.
- Guy W(2000) Clinical Global Impressions (CGI) Scale. Modified From: Rush J, et al: Psychiatric Measures, APA,Washington DC.
- Caldiero RM, Parran TV Jr, Adelman CL, Piche B (2006) Inpatient initiation of buprenorphine maintenance vs. detoxification: can retention of opioid-dependent patients in outpatient counseling be improved? Am J Addict 15: 1-7.
- Threlkeld M, Parran TV, Adelman CA, Grey SF, Yu J (2006) Tramadol versus buprenorfina for the management of acute heroin withdrawal: a retrospective matched cohort controlled study. Am J Addict 15: 186-191.
- Van den Brink W, Haasen C (2006) Evidenced-based treatment of opioid-dependent patients. Can J Psychiatry 51: 635-646.
- Lanier RK, Lofwall MR, Mintzer MZ, Bigelow GE, Strain EC (2010) Physical dependence potential of daily tramadol dosing in humans. Psychopharmacology (Berl) 211: 457-466.