6.9 ¿Por qué los objetos absorben de la forma en que lo hacen?
La atmósfera absorbe una cantidad significativa de radiación en el infrarrojo, pero bastante poco en el visible. Además, vemos que los gases absorben fuertemente en algunas longitudes de onda y no en otras. ¿A qué se debe esto?
Para responder a esta pregunta, tenemos que fijarnos en las configuraciones de los electrones que circulan por los átomos y las moléculas. Hace más de 100 años, los científicos comenzaron a utilizar prismas para dispersar la luz del sol y de las llamas que contenían diferentes elementos. Mientras que el sol daba los colores del arco iris, las llamas tenían la luz en líneas o bandas muy definidas. Este rompecabezas se resolvió finalmente hace poco más de 100 años con la invención de la mecánica cuántica, que básicamente dice que los electrones que zumban alrededor de los átomos y las moléculas y las vibraciones y rotaciones de las moléculas sólo pueden tener energías discretas que se rigen por las reglas de conservación del momento angular.

La siguiente lista con viñetas es un curso intensivo de absorción por parte de los electrones de los átomos y las moléculas. Consulte la figura debajo del recuadro.
Curso intensivo: Absorción por los electrones en átomos y moléculas
- Los enlaces químicos y la mecánica cuántica determinan conjuntamente los niveles de energía en los que puede estar cualquier electrón, átomo o molécula.
- La energía de una molécula es la suma de la energía relacionada con la posición de los electrones respecto a sus estados electrónicos estables en tierra, la vibración molecular y la rotación molecular.
- La absorción se produce cuando la energía del fotón coincide con la diferencia entre dos niveles de energía en una molécula, ΔE = Efinal – Einitial = hc/λ.
- Las reglas establecidas por la conservación del momento angular y el espín de los electrones determinan qué transiciones entre niveles de energía están permitidas.
- La cantidad de absorción, llamada simplemente sección transversal de absorción, σ, proviene de muchos factores, pero varía significativamente de una molécula a otra y de una transición a otra. La sección transversal tiene dimensiones de área y comúnmente tiene unidades de cm2.
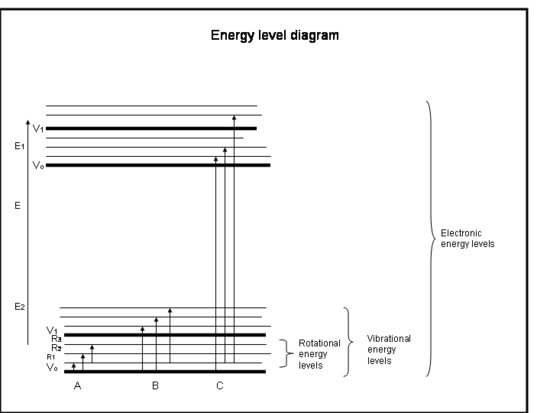
- Las transiciones electrónicas ocurren cuando los electrones realmente saltan a otras órbitas alrededor de los núcleos. Tienen energías equivalentes a la radiación (es decir, a los fotones) en las longitudes de onda del ultravioleta al visible.
- Las transiciones vibracionales ocurren cuando la molécula vibra a una frecuencia diferente o de una manera diferente. Las moléculas diatómicas (por ejemplo, el O2 y el N2) sólo tienen una forma de vibrar: hacia adelante y hacia atrás a lo largo del enlace químico que las une. Pero las moléculas más complicadas (por ejemplo, H2O y CO2) pueden vibrar no sólo con los núcleos acercándose y alejándose entre sí, sino también doblándose en tres direcciones. Estas transiciones vibracionales, acompañadas de movimientos que combinan la vibración y la rotación, tienen energías equivalentes a la radiación infrarroja cercana y media (es decir, a los fotones).
- Las transiciones rotacionales se producen cuando una molécula cambia su velocidad de rotación. Estas transiciones tienen energías equivalentes a la radiación (es decir, fotones) en las longitudes de onda del infrarrojo lejano a las ondas de radio.
- Las energías translacionales de las moléculas en la atmósfera terrestre, ~kT, son generalmente un poco más grandes que la energía necesaria para pasar de un nivel rotacional a otro, de 10 a 100 veces menos que la energía necesaria para pasar de un nivel vibracional a otro, y de cientos a miles de veces menos que lo que se necesita para pasar de un nivel electrónico a otro.
- Ya hemos visto que algunas moléculas y átomos tienen más energía cinética que otros. Todas las moléculas con energía cinética mayor que la diferencia de energía entre niveles rotacionales pueden colisionar con la molécula y darle suficiente energía rotacional para cambiar a un nivel rotacional superior. Así, vemos que la energía rotacional se distribuye en muchos niveles rotacionales, pero que los niveles vibracionales y electrónicos suelen ser los niveles de tierra (de menor energía).
- Los átomos no tienen vibraciones y rotaciones similares a las de las moléculas porque sólo tienen un núcleo, por lo que sus espectros consisten únicamente en transiciones electrónicas.
- Una transición brusca de un nivel discreto a otro, que aparece como una línea en un espectro, se produce en un estrecho rango de energías sobre la diferencia de energía de transición. La radiación resultante se produce en una banda estrecha de longitudes de onda en torno a la longitud de onda central de la línea. La anchura de esta línea (medida a la mitad de la altura máxima de la línea) se denomina anchura de línea.
- Esta anchura de línea natural puede ampliarse por el movimiento de la molécula, lo que se denomina ensanchamiento Doppler, o por colisiones, lo que se denomina ensanchamiento por presión.
- En lo alto de la atmósfera, el ensanchamiento Doppler es dominante porque la presión es baja, pero en lo bajo de la atmósfera, el ensanchamiento por presión se vuelve dominante aunque el ensanchamiento Doppler también aumenta. Así que las líneas de absorción son más anchas cerca de la superficie de la Tierra que más arriba en la atmósfera.
La sección transversal de absorción, σ, varía significativamente sobre la anchura de la línea de absorción. Así, es posible que toda la radiación se absorba en el centro de la línea pero que se absorba muy poco en las «alas».
Interpretación física
Los átomos y las moléculas pueden absorber la radiación (un fotón) sólo si su estructura tiene una diferencia de energía entre niveles que coincida con la energía del fotón (hc/λ). En caso contrario, el átomo o la molécula no absorberán la luz. Una vez que la molécula ha absorbido el fotón, puede perder un fotón y volver a su nivel energético inferior original; o puede romperse si la energía del fotón es mayor que el enlace químico que mantiene unida a la molécula; o puede colisionar con otras moléculas, como el N2 o el O2, y transferirles energía mientras vuelve a su nivel energético inferior. Las colisiones se producen con frecuencia, por lo que la energía del fotón absorbido suele transferirse a energía térmica.
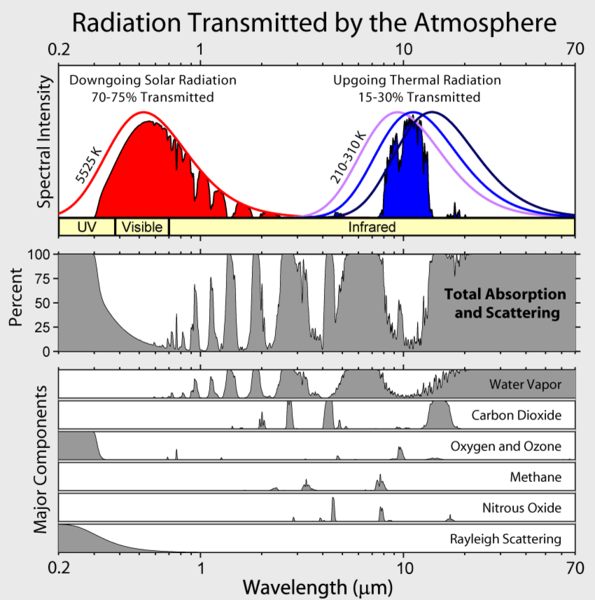
Nótese que la irradiación infrarroja saliente de la Tierra está limitada a unas pocas «ventanas» atmosféricas y que la irradiación en todas las demás longitudes de onda es fuertemente absorbida, principalmente por el vapor de agua, pero también por el dióxido de carbono, el ozono, el óxido nitroso, el metano y otros gases más traza que no se muestran en la figura anterior.