ORIGINAL
Zespół Gorlina-Goltza: postępowanie w raku podstawnokomórkowym twarzy
Zespół Gorlina-Goltza: management of facial basal cell carcinoma
Rocío Gilabert Rodrígueza, Pedro Infante Cossíob, Pablo Redondo Parejob, Eusebio Torres Carranzab, Alberto García-Perla Garcíab and Domingo Sicilia Castroa
aService of Plastic and Reconstructive Surgery, Hospital Universitario Virgen del Rocío, Sevilla, Hiszpania
bService of Oral and Maxillofacial Surgery, Hospital Universitario Virgen del Rocío, Sevilla, Hiszpania
Adres do korespondencji
SUMMARY
Introduction/Objective: Zespół Gorlin-Goltz (GGS) jest dziedziczonym autosomalnie dominująco zaburzeniem, które przede wszystkim predysponuje do proliferacji nowotworów, takich jak rak podstawnokomórkowy i keratocysty szczękowe. Raki podstawnokomórkowe występujące u pacjentów z GGS są zazwyczaj mnogie, klinicznie polimorficzne w wyglądzie, bez predylekcji płci, czasami wykrywane we wczesnym okresie życia i obejmujące nawet obszary nie narażone na działanie promieni słonecznych. Ich zachowanie kliniczne jest zmienne, choć czasami mogą być bardzo agresywne, zwłaszcza na twarzy. W celu zbadania zachowania się raków podstawnokomórkowych u pacjentów z GCS przeprowadzono badanie pacjentów leczonych w naszym szpitalu w latach 2001-2011, którzy spełniali kryteria choroby.
Materiał i metody: Do badania włączono 11 pacjentów z klinicznym i/lub genetycznym rozpoznaniem GGG. Badaliśmy rozkład w zależności od wieku i płci, objawów klinicznych, cech histologicznych, zastosowanej techniki chirurgicznej, obecności nawrotów i ewolucji pacjentów.
Wyniki: U 36% pacjentów stwierdzono raka podstawnokomórkowego na twarzy. Liczba guzów u jednego pacjenta wahała się od 9 do 21. Preferowanym sposobem leczenia było wycięcie chirurgiczne, chociaż u wszystkich pacjentów pojawiły się nowe zmiany i nawroty wymagające kilku zabiegów. Badanie histologiczne wykazało kontakt lub bliskość guza z marginesami chirurgicznymi w 28% zmian.
Wnioski: W literaturze nie ma wystarczających dowodów, aby określić leczenie z wyboru spośród różnych metod dostępnych w leczeniu raka podstawnokomórkowego w SGG. Konieczna jest profilaktyka polegająca na unikaniu ekspozycji na słońce.
Słowa kluczowe: zespół Gorlin-Goltz. Zespół nevoid basal cell carcinoma. Rak podstawnokomórkowy. Queratoquiste maxilar.
ABSTRACT
Wprowadzenie/cel: Zespół Gorlina-Goltza (GGS) jest dziedziczonym autosomalnie dominująco zaburzeniem, które głównie predysponuje do proliferacji guzów, takich jak raki podstawnokomórkowe i keratocysty szczękowe. GGS jest spowodowany mutacją genu Patched na chromosomie 9. Rak podstawnokomórkowy u pacjentów z GGS zwykle występuje jako mnogie guzy, z polimorficznymi cechami klinicznymi, bez predylekcji płciowej, czasami pojawiające się we wczesnym okresie życia, a nawet obejmujące obszary nie narażone na światło słoneczne. Zachowanie kliniczne może być różne, a czasami może być bardzo agresywne, szczególnie w obrębie twarzy. W celu zbadania zachowania się raków podstawnokomórkowych u pacjentów z GGS przeprowadzono badanie na pacjentach, którzy spełniali kryteria choroby i byli leczeni w naszym szpitalu w okresie od 2001 do 2011 roku.
Materiał i metody: Do badania włączono 11 pacjentów z klinicznym i/lub genetycznym rozpoznaniem GGS. Pacjentów analizowano pod względem płci i wieku, aspektów klinicznych, cech histologicznych, zastosowanego leczenia chirurgicznego, obecności nawrotów oraz obserwacji.
Wyniki: Raki podstawnokomórkowe występowały na twarzy u 36% pacjentów. Liczba guzów na jednego pacjenta wahała się od 9 do 21. Preferowanym sposobem leczenia było wycięcie chirurgiczne, chociaż u wszystkich pacjentów pojawiły się nowe zmiany i nawroty, które wymagały kilku zabiegów. Badanie histologiczne wykazało kontakt lub bliskość guza do marginesów chirurgicznych w 28% zmian.
Wnioski: W literaturze nie ma wystarczających dowodów, aby określić leczenie z wyboru spośród różnych dostępnych metod postępowania w raku podstawnokomórkowym w GGS. Konieczna jest profilaktyka polegająca na unikaniu ekspozycji na światło słoneczne.
Słowa kluczowe: Zespół Gorlin-Goltz. Zespół nevoidalnego raka podstawnokomórkowego. Rak podstawnokomórkowy. Keratocysta szczękowa.
Wprowadzenie
Zespół Gorlina-Goltza (GGS) został opisany w 1960 roku przez jego imienników, Gorlina i Goltza1. Opisali oni początkowo triadę charakterystyczną dla tego zespołu: mnogie raki podstawnokomórkowe, keratocysty szczękowe i żebra dwudzielne. Obecnie wiadomo, że jest to choroba genetyczna, dziedziczona w sposób autosomalny dominujący, o niepełnej penetracji i zmiennym fenotypie2,3, znana również jako zespół nerczycowo-podstawnokomórkowy lub zespół raka podstawnokomórkowego. Jest spowodowana mutacją genu Patched (PTCH), genu supresorowego nowotworów, zlokalizowanego na chromosomie 9 (9q22, 3-q31). Szacowana częstość występowania waha się od 1:57 000 do 1:164 000 w zależności od kraju, z ogólnie przyjętą średnią częstością występowania wynoszącą około 1:60 0004.
GGS jest chorobą charakteryzującą się klinicznie predyspozycją do rozwoju licznych nowotworów, jak również występowaniem anomalii rozwojowych. Początek kliniczny występuje w dzieciństwie lub w wieku młodzieńczym i towarzyszy mu szereg objawów, z których najczęstszym jest obecność licznych raków podstawnokomórkowych i odontogennych keratocyst szczękowych. Inne objawy to hiperkeratoza dłoni i stóp, nieprawidłowości w układzie kostnym, ektopowe zwapnienia wewnątrzczaszkowe i dysmorfia twarzy (makrocefalia, rozszczep wargi i podniebienia oraz poważne anomalie oczne)5. Deficyt intelektualny występuje w około 5% przypadków. Mogą również wystąpić problemy oczne, moczowo-płciowe i sercowo-naczyniowe6 . Złośliwe medulloblastoma rozwijają się u 5-10% pacjentów z GGS i mogą być potencjalną przyczyną wczesnego zgonu. Diagnozę ustala się, gdy spełnione są 2 główne lub 1 główne i 2 drugorzędne kryteria kliniczne5 (tabela 1). Ostatecznym testem diagnostycznym jest wykazanie mutacji w genie PTCH.

Twory powstają w SGG w wyniku zmienionych pro-onkogenów lub genów supresorowych nowotworów. Te ostatnie pełnią funkcję supresorową w stosunku do pro-onkogenów. W przypadku raka podstawnokomórkowego nie jest jasne, który z pro-onkogenów jest zaangażowany. Szlak RAS jest zmieniony, ale nie we wszystkich przypadkach. Jeśli chodzi o geny supresorowe nowotworów, wydaje się, że p53 odgrywa drugorzędną rolę w rozwoju tego nowotworu. Predyspozycja tych pacjentów do zachorowania na raka skóry wydaje się wynikać z faktu, że komórki dotknięte mutacją są bardziej podatne na działanie promieni słonecznych ze względu na zmienione mechanizmy naprawy DNA. Rak podstawnokomórkowy dotyka każdego obszaru anatomii skóry, ale głównie pojawia się w miejscach narażonych na promieniowanie ultrafioletowe, głównie na twarzy, plecach i klatce piersiowej. Istnieją pewne różnice pomiędzy rakami podstawnokomórkowymi występującymi w populacji ogólnej i u pacjentów z GBS. W tym ostatnim przypadku są one częściej liczne, polimorficzne w wyglądzie, nie wykazują preferencji co do płci i mogą dotyczyć nawet miejsc nie narażonych na działanie promieni słonecznych. Zazwyczaj występują one klinicznie w wielu postaciach6 , w liczbie od kilku do kilkuset, pojawiają się we wczesnym okresie życia (nawet przy urodzeniu); ich zachowanie kliniczne jest zmienne, chociaż czasami mogą być bardzo agresywne od samego początku, zwłaszcza na poziomie twarzy.
Większość dostępnych dowodów klinicznych dotyczących postępowania z rakiem podstawnokomórkowym w GTS pochodzi z badań przeprowadzonych u pacjentów nieobjętych zespołem. Ze względu na duże doświadczenie w leczeniu tych nowotworów w populacji ogólnej, większość autorów stosuje te same środki terapeutyczne u pacjentów z GBS.
Celem pracy była analiza postępowania w przypadku raka podstawnokomórkowego twarzy u pacjentów z GBS w celu oceny zachowania klinicznego oraz kryteriów diagnostycznych i terapeutycznych w oparciu o badanie kliniczne pacjentów leczonych z powodu GBS w ciągu ostatnich 10 lat w Hospital Universitario Virgen del Rocío w Sewilli (Hiszpania).
Materiał i metody
Przeanalizowano w sposób obserwacyjny i retrospektywny dokumentację kliniczną pacjentów, u których w latach 2001-2011 rozpoznano GTS, leczonych w Klinice Chirurgii Jamy Ustnej i Szczękowo-Twarzowej oraz Chirurgii Plastycznej i Rekonstrukcyjnej. Do badania włączono 11 pacjentów z klinicznym i/lub genetycznym rozpoznaniem GGS, wyłączając osoby z niepełnym wywiadem klinicznym pomimo postawionego rozpoznania. Analizie poddano dane epidemiologiczne (wiek i płeć) oraz dane medyczno-chirurgiczne (liczba i lokalizacja zmian, rozpoznanie histopatologiczne, zastosowana technika operacyjna, obecność nawrotów i ewolucja). Obserwacja kliniczna polegała na okresowych badaniach kontrolnych, trwających średnio 4,5 roku.
Wyniki
Średni wiek pacjentów wynosił 27 lat, większość stanowili mężczyźni (73%). W 45% przypadków wiek w chwili rozpoznania choroby był niższy niż 20 lat. Rozpoznanie kliniczne postawiono u 9 pacjentów (2 kryteria główne lub 1 główne i 2 małe), natomiast u 2 pacjentów postawiono rozpoznanie genetyczne. Trzech pacjentów miało wywiad rodzinny (tabela 2).

W zakresie cech klinicznych (tabela 3) najczęstszym objawem klinicznym była keratocysta szczękowa, występująca u 91% próby (10 pacjentów). Na kolejnych miejscach znalazły się zmiany kostne (63%) i charakterystyczne zapalenie powięzi (54%). U czterech z 11 pacjentów (36%) rozwinęły się raki podstawnokomórkowe (tabela 4). Liczba zmian na jednego pacjenta wahała się od 9 do 21, przy czym u jednego pacjenta nie odnotowano dokładnej liczby zmian. Wszystkie były zlokalizowane głównie w obrębie twarzy (ryc. 1 i 2), następnie szyi i pleców. We wszystkich przypadkach wykonano chirurgiczne wycięcie zmian (ryc. 3). Patologia wykazała w większości przypadków histologię guzkową, a wysoki odsetek marginesów chirurgicznych był zajęty (28% zmian miało kontakt lub bliskość guza do marginesu). We wszystkich przypadkach wykonano więcej niż jedną interwencję chirurgiczną.

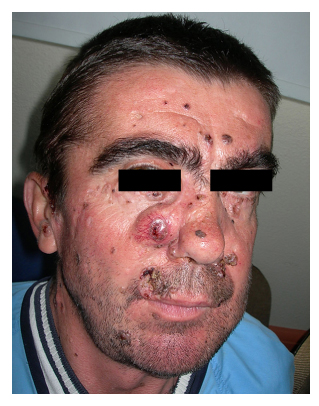
Rycina 1. Pacjent nr 6.
Wielokrotne raki podstawnokomórkowe twarzy.
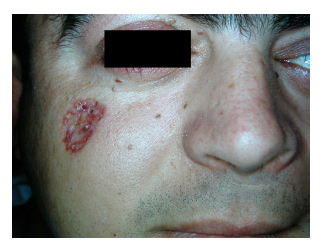
Rycina 2. Pacjent numer 2 przedstawiający
raka podstawnokomórkowego na policzku.

Rycina 3. Pacjent numer 1.
A: Obraz przedoperacyjny mnogich raków podstawnokomórkowych na twarzy i szyi.
B: Natychmiastowe szczegóły pooperacyjne po wycięciu.
U pacjenta numer 4 rozwinęły się liczne nawracające raki podstawnokomórkowe w dolnej trzeciej części twarzy wymagające agresywnego wycięcia, w tym żuchwy i natychmiastowej rekonstrukcji za pomocą 2 następujących po sobie wolnych płatów (strzałkowego osteoseptocutaneous i przedramiennego fasciocutaneous) (ryc. 4). Pacjent numer 6 zgłosił się z rakiem naskórkowym zlokalizowanym na trzonie żuchwy w połączeniu z keratocystą, w wyniku czego zmarł.

Ryc. 4. A: Nawracające raki podstawnokomórkowe w dolnej trzeciej części twarzy.
B: Rekonstrukcja 3D-CT pokazująca zajęcie kości i tkanki okołokostnej.
C: Agresywne wycięcie z mandibulektomią.
D: Kompleksowa rekonstrukcja z 2 kolejnymi wolnymi płatami
(osteoseptocutaneous fibula and antebrachial fasciocutaneous with palmaris minor tendon).
E: Pooperacyjny panoramiczny radiogram.
F: Obraz pooperacyjny pacjenta.
Dyskusja
Jako punkt wyjścia przeprowadzono przegląd literatury w celu oceny informacji naukowych opublikowanych na temat SGG w ciągu ostatnich 10 lat, który ujawnił rosnące zainteresowanie tym tematem, głównie w czasopismach z dziedziny dermatologii, chirurgii jamy ustnej i szczękowej, stomatologii i genetyki. Największa liczba artykułów zgrupowana jest w czasopismach dermatologicznych, prawdopodobnie dlatego, że raki podstawnokomórkowe są jedną z najczęstszych i nawrotowych zmian, a ich lokalizacja (zwłaszcza na skórze twarzy) sprawia, że są bardziej widoczne i łatwiejsze do rozpoznania. Następną grupą czasopism, w kolejności częstotliwości ukazywania się, są czasopisma z zakresu chirurgii szczękowo-twarzowej, stomatologii i genetyki. Keratocysty szczękowe są najczęstszymi zmianami w tym zespole i często są objawem przewodnim, który ukierunkowuje diagnozę.
W naszej serii, jak szeroko opisano w literaturze, keratocysty szczękowe były najczęstszym objawem klinicznym obecnym u 10 pacjentów. Tylko u jednego pacjenta nie stwierdzono keratocyst szczękowych, choć młody wiek tego pacjenta może tłumaczyć brak czasu na ich rozwój (pacjent nr 7). Wyraźnie przeważali mężczyźni, choć w piśmiennictwie nie opisano przewagi płci, więc nie można z tego faktu wyciągać wniosków, biorąc pod uwagę małą liczebność próby. Przedstawiono 4 typowe przypadki SGG o wysokiej ekspresji fenotypowej (pacjenci nr 1, 2, 4 i 6), w których obserwuje się dominujące objawy kliniczne (keratocysty szczękowe i raki podstawnokomórkowe). Chociaż w większości przypadków zakłada się obecność dotkniętego chorobą rodzica, w naszej serii tak nie jest, ponieważ tylko 3 pacjentów (27 w porównaniu do 70-80% opisywanych w literaturze) ma co najmniej jednego znanego nam dotkniętego chorobą członka rodziny (tabela 2). U czterech z 11 pacjentów z SGG rozwinął się rak podstawnokomórkowy. Stanowi to 36% zaangażowania, co jest niskim odsetkiem w porównaniu z 90% częstością klasycznie uznawaną dla tej choroby. Należy zwrócić uwagę na młody wiek niektórych pacjentów. Chociaż zmiany te opisywano w tym zespole już po urodzeniu, nie jest to normą i do ich klinicznej ekspresji konieczne jest kilkuletnie narażenie na czynniki ryzyka (promieniowanie ultrafioletowe). Jednak średni wiek pacjentów z rakiem podstawnokomórkowym w tej serii wynosił 39 lat (najmłodszy 19 lat).
Rak podstawnokomórkowy jest uważany za jeden z najczęstszych złośliwych nowotworów skóry, zwłaszcza u osób rasy kaukaskiej w regionach geograficznych położonych blisko równika, gdzie jest związany z ekspozycją na promieniowanie ultrafioletowe u osób o jasnej karnacji.7 W populacji ogólnej choroba ta występuje między szóstą a siódmą dekadą życia, a jej częstość występowania znacznie wzrosła w ostatnich latach. W populacji ogólnej choroba ta występuje między szóstą a siódmą dekadą życia, a jej częstość występowania znacznie wzrosła w ostatnich latach. Główną przyczyną raka podstawnokomórkowego jest przewlekła ekspozycja na światło słoneczne, w związku z czym zmiany występują zazwyczaj na odsłoniętych częściach ciała: twarzy, uszach, szyi, skórze głowy, ramionach i plecach. Znane czynniki etiologiczne to między innymi ekspozycja na promieniowanie ultrafioletowe (zarówno krótko-, jak i długoterminowe), niektóre chemiczne substancje rakotwórcze (arsen i węglowodory), promieniowanie jonizujące oraz przewlekłe podrażnienia. Istnieje kilka postaci zespołowych, w tym xeroderma pigmentosum i zespół znamienia podstawnokomórkowego (BNS), między innymi8.
Postępowanie w przypadku raka podstawnokomórkowego w BNS jest słabo zbadane i odnosi się głównie do leczenia zachowawczego. Pauwels i wsp. przedstawili terapię fotodynamiczną jako opcję leczenia raka podstawnokomórkowego u pacjentów z SGG z korzystnymi wynikami w porównaniu z zabiegiem chirurgicznym9. Micali i wsp. przeanalizowali rolę miejscowo stosowanego imikwimodu w leczeniu raka podstawnokomórkowego u pacjentów z SGG i podkreślili, że ta metoda terapeutyczna jest skuteczną opcją ze względu na wysoką współpracę pacjentów, którzy wolą ją od wielokrotnych wycięć chirurgicznych10. W badaniach dotyczących postępowania z rakiem podstawnokomórkowym w populacji ogólnej leczenie chirurgiczne (proste wycięcie z obserwacją kliniczną zmian z zajęciem marginesu) wyróżnia się spośród innych opcji terapeutycznych11-13. Chociaż zachowanie raka podstawnokomórkowego w populacji ogólnej jest inne niż w przypadku GTS, do czasu udostępnienia innych szczegółowych badań wydaje się bardziej niż uzasadnione zastosowanie u tych pacjentów bogatego doświadczenia, jakim dysponujemy.
Leczenie raka podstawnokomórkowego polega na całkowitym usunięciu zmiany, co można wykonać kilkoma metodami. Wycięcie chirurgiczne jest najczęściej stosowaną procedurą i wydaje się, że panuje zgoda co do tego, że jest to najlepsza opcja ze względu na wysoki odsetek wyleczeń, szczególnie w przypadku małych i średnich zmian. Inne opcje (krioterapia, elektroresekcja i łyżeczkowanie, radioterapia, chemioterapia miejscowa itp.) są stosowane u pacjentów, u których zabieg chirurgiczny jest przeciwwskazany14 , albo ze względu na cechy guza (liczba lub wielkość), albo z powodu ogólnych czynników dotyczących pacjenta (wiek, ryzyko anestezjologiczne itp.). Ponieważ guzy te mogą stać się bardzo agresywne z naciekaniem okołonerwowym i wielopostaciowością, a zwłaszcza w przypadkach nawrotów, mogą czasami wymagać rozległych resekcji, które pozostawiają ubytki wymagające skomplikowanych rekonstrukcji, jak to miało miejsce u pacjenta 4, u którego wykonano rekonstrukcję żuchwy za pomocą mikronaczyniowego płata strzałkowo-promieniowego.
Chirurgiczne usunięcie raka podstawnokomórkowego charakteryzuje się odsetkiem wyleczeń przekraczającym 90%. Marginesy chirurgiczne są dobrze zdefiniowane, a wyleczenie uważa się za możliwe, jeśli marginesy są czyste. Podobnie jak w przypadku innych form leczenia, wielkość, lokalizacja i podtyp histologiczny mają wpływ na ogólne rokowanie. Nie ma jednolitych zaleceń dotyczących granicy marginesów chirurgicznych. Większość chirurgów wybiera margines co najmniej 3 do 5 mm zarówno w obszarze, jak i głębokości dla małych, dobrze obwiedzionych zmian i 1 cm lub więcej dla dużych, agresywnych zmian.
Zarządzanie jest kontrowersyjne w nowotworach, w których raport patologii anatomicznej wskazuje, że marginesy są zaangażowane. W różnych badaniach u pacjentów z chorobami niesyndromowymi stwierdzono dodatnie zajęcie marginesów od 4 do 16,6%15-18. W naszej serii 28% zmian miało histologicznie bliskie i/lub zaangażowane marginesy, co jest wysokim wskaźnikiem w porównaniu z tymi raportowanymi w populacji ogólnej. Literatura sugeruje, że region głowy i szyi charakteryzuje się wyższym odsetkiem zajęcia marginesów, co można tłumaczyć trudnościami w usuwaniu guzów bez uszkodzenia szlachetnych struktur anatomicznych16,17. W dużych seriach obserwacji pacjentów z rakiem podstawnokomórkowym zaobserwowano jedynie 25% odsetek nawrotów po 5 latach w zmianach z niekompletną resekcją13. Postępowanie zachowawcze z późniejszą obserwacją wydaje się być najrozsądniejszym podejściem w tych przypadkach19,20, biorąc pod uwagę, że po ponownej interwencji chirurgicznej tylko 28-54% zmienionych marginesów jest widocznych15-18. 15-18 U chorych na SGG takie postępowanie i obserwacja wydają się wysoce wskazane w przypadku guzów o ścisłych i/lub dodatnich marginesach histologicznych bez dowodów na rozrost tkanki okołonerkowej i w miejscach łatwo dostępnych do eksploracji, biorąc również pod uwagę duże prawdopodobieństwo sporadycznego pojawiania się nowych raków i ich wielodyscyplinarność, co w dłuższej perspektywie może wymagać kilku dodatkowych zabiegów chirurgicznych w tej okolicy.
Mohs micrographic surgery is the surgical treatment of choice for recurrent lesions in compromised areas (eyelids, orbital rims, etc.)21. It is also indicated for tumours whose clinical characteristics (histological subtype, poorly defined borders, tendency to recurren) or location classify them as high-risk22. Jego przewaga wynika z metodologii zabiegu, która pozwala na 100% kontrolę marginesów chirurgicznych, zarówno w głąb, jak i na powierzchni. To z kolei może zapewnić całkowitą resekcję guza, zagwarantować maksymalne zachowanie zdrowych tkanek i, wtórnie, zoptymalizować późniejszą rekonstrukcję.
Chociaż SGG nie można wyleczyć, wczesna diagnoza pomaga zapewnić multidyscyplinarne podejście w celu uniknięcia powikłań, takich jak pojawienie się nowych raków podstawnokomórkowych w wyniku ekspozycji na promieniowanie słoneczne lub mnogich keratocyst, które mogą zniszczyć szczęki. Rak podstawnokomórkowy jest nowotworem złośliwym, który nie daje przerzutów, ale może być bardzo agresywny, jeśli nacieka na głębsze warstwy skóry. Biorąc pod uwagę, że wycięcie chirurgiczne jest najskuteczniejszą opcją w leczeniu raka podstawnokomórkowego w SGG, ważne jest prewencyjne podejście medyczne, polegające na próbie leczenia zmian, gdy są one niewielkich rozmiarów, w celu zmniejszenia następstw pooperacyjnych. Chociaż istnieje kilka specjalności, które mają szerokie doświadczenie w zakresie SGG, o czym świadczy duża liczba publikacji, podstawowa opieka zdrowotna jest nieobecna w tej dziedzinie, dlatego konieczne jest promowanie edukacji zdrowotnej lub szkolenia specjalistów w tym sektorze w celu zwiększenia wczesnej diagnozy, a w konsekwencji wczesnego rozpoczęcia leczenia i poprawy rokowania. Wyniki wielu badań epidemiologicznych wskazują, że ryzyko zachorowania na raka podstawnokomórkowego wykazuje silną dodatnią korelację z ekspozycją na promieniowanie UV i dlatego pacjenci ci powinni unikać nadmiernej ekspozycji na słońce. Podobnie należy w miarę możliwości unikać radioterapii z uwagi na ryzyko wystąpienia i nawrotu raka podstawnokomórkowego. Chemoprewencja może być stosowana w celu uniknięcia zmian skórnych. Analogi witaminy A, takie jak retinoidy czy izotretynoina, mogą odgrywać ważną rolę w zapobieganiu lub opóźnianiu rozwoju nowych raków podstawnokomórkowych.
Podsumowując, raki podstawnokomórkowe u pacjentów z GGS są związane ze zmianami w mechanizmie supresji nowotworu spowodowanymi mutacjami w genie PTCH, co skutkuje sporadycznym występowaniem tych nowotworów zwłaszcza w odniesieniu do promieniowania ultrafioletowego. Istnieją różnice w charakterystyce klinicznej raków podstawnokomórkowych u pacjentów z SGG i w populacji ogólnej, głównie w zakresie liczby zmian (większa w SGG), wieku zachorowania (niższy w SGG) i zachowania (większa agresywność i częstość nawrotów w SGG). W naszym przeglądzie 11 pacjentów, u 36% stwierdzono raka podstawnokomórkowego na twarzy. Najszerzej akceptowanym w literaturze sposobem leczenia jest wycięcie chirurgiczne i takie też postępowanie zastosowano we wszystkich naszych przypadkach. W naszej serii 28% guzów miało bliskie i/lub naruszone marginesy histologiczne, co jest wysokim wskaźnikiem w porównaniu z seriami w populacji niesyndromowej. Nowe zmiany i nawroty wykryto u 100% chorych po pierwszym leczeniu. Istniejące w literaturze dane są niewystarczające do podjęcia decyzji opartych na dowodach naukowych dotyczących różnych terapii dostępnych w leczeniu raka podstawnokomórkowego w SGG. Zalecana jest profilaktyka polegająca na unikaniu ekspozycji na promieniowanie UV.
Obowiązki etyczne
Ochrona ludzi i zwierząt. Autorzy deklarują, że w ramach tych badań nie przeprowadzano żadnych eksperymentów na ludziach ani zwierzętach.
Poufność danych. Autorzy deklarują, że w tym artykule nie pojawiają się żadne dane pacjentów.
Prawo do prywatności i świadoma zgoda. Autorzy deklarują, że w tym artykule nie pojawiają się dane pacjentów.
Konflikt interesów
Autorzy deklarują, że nie mają konfliktu interesów.
Bibliografia
1. Gorlin RJ, Goltz RW. Mnogi nefoidalny nabłoniak podstawnokomórkowy, torbiel szczękowa i dwudzielne żebro. Zespół. N Engl J Med. 1960; 262:908-12.
2. Stoelinga PJ, Peters JH, van de Staak WJ, Cohen MM. Nowe doniesienia na temat zespołu znamion podstawnokomórkowych. Oral Surg Oral Med Oral Pathol. 1973; 36:686-92.
3. Totten JR. Zespół mnogich znamion raka podstawnokomórkowego. Doniesienie o jej występowaniu w czterech pokoleniach pewnej rodziny. Rak. 1980; 46:1456-62.
4. Visioli F, Martins CA, Heitz C, Rados PV, Sant’Ana Filho M. Is nevoid basal cell carcinoma syndrome really so rare? Propozycja protokołu badawczego na podstawie serii przypadków. J Oral Maxillofac Surg. 2010; 68:903-8.
5. Evans DG, Ladusans EJ, Rimmer S, Burnell LD, Thakker N, Farndon PA. Complications of the nevoid basal cell carcinoma syndrome: results of a population based study. J Med Genet. 1993; 30:460-4.
6. Díaz-Fernández JM, Infante-Cossío P, Belmonte-Caro R, Ruiz-Laza L, García-Perla-García A, Gutiérrez-Pérez JL. Zespół znamienia podstawnokomórkowego. Prezentacja sześciu przypadków i przegląd piśmiennictwa. Med Oral Patol Oral Cir Bucal. 2005; 10 Suppl 1:E57-66.
7. Roewert-Huber J, Lange-Asschenfeldt B, Stockfleth E, Kerl H. Epidemiology and aetiology of basal cell carcinoma. Br J Dermatol. 2007; 157 Suppl 2:47-51.
8. Kyrgidis A, Tzellos TG, Vahtsevanos K, Triaridis S. New concepts for basal cell carcinoma. Demograficzne, kliniczne, histologiczne czynniki ryzyka i biomarkery. A systematic review of evidence regarding risk for tumor development, susceptibility for second primary and recurrence. J Surg Res. 2010; 159:545-56.
9. Pauwels C, Mazereeuw-Hautier J, Basset-Seguin N, Livideanu C, Viraben R, Paul C, et al. Topical methyl aminolevulinate photodynamic therapy for management of basal cell carcinomas in patients with basal cell nevus syndrome improves patient’s satisfaction and reduces the need for surgical procedures. J Eur Acad Dermatol Venereol. 2011; 25:861-4.
10. Micali G, de Pasquale R, Caltabiano R, Impallomeni R, Lacarrubba F. Topical imiquimod treatment of superficial and nodular basal cell carcinomas in patients affected by basal cell nevus syndrome: a preliminary report. J Dermatolog Treat. 2002; 13:123-7.
11. Chren MM, Torres JS, Stuart SE, Bertenthal D, Labrador RJ, Boscardin WJ. Recurrence after treatment of nonmelanoma skin cancer: a prospective cohort study. Arch Dermatol. 2011; 147:540-6.
12. Wallace DL, Jaffe W. Reply to: Do basal cell carcinomas recurring after complete conventional surgical excision? R.W. Griffiths, S.K., Suvarna. J. Stone BJPS. 2005; 58:795-805, J Plast Reconstr Aesthet Surg 2006;59:1247.
13. Sherry KR, Reid LA, Wilmshurst AD. A five year review of basal cell carcinoma excisions. J Plast Reconstr Aesthet Surg. 2010; 63:1485-9.
14. Kopera D, Cerroni L, Fink-Puches R, Kerl H. Different treatment modalities for the management of a patient with the nevoid basal cell carcinoma syndrome. J Am Acad Dermatol. 1996; 34:937-9.
15. Patel SS, Cliff SH, Ward Booth P. Incomplete removal of basal cell carcinoma: what is the value of further surgery? Oral Maxillofac Surg. 2012. (Epub ahead of print).
16. Farhi D, Dupin N, Palangié A, Carlotti A, Avril MF. Incomplete excision of basal cell carcinoma: rate and associated factors among 362 consecutive cases. Dermatol Surg. 2007; 33:1207-14.
17. Bogdanov-Berezovsky A, Cohen A, Glesinger R, Cagnano E, Krieger Y, Rosenberg L. Clinical and pathological findings in reexcision of incompletely excised basal cell carcinomas. Ann Plast Surg. 2001; 47:299-302.
18. Kumar P, Orton CI, McWilliam LJ, Watson S. Incidence of incomplete excision in surgically treated basal cell carcinoma: a retrospective clinical audit. Br J Plast Surg. 2000; 53:563-6.
19. Griffiths RW, Suvarna SK, Stone J. Basal cell carcinoma histological clearance margins: an analysis of 1539 conventionally excised tumours. Wider still and deeper? J Plast Reconstr Aesthet Surg. 2007; 60:41-7.
20. Antoni ML. Chirurgiczne leczenie nieczerniakowych nowotworów skóry. AORN J. 2000; 71:552-4. 556-8, 560-4.
21. Mosterd K, Krekels GA, Nieman FH, Ostertag JU, Essers BA, Dirksen CD, et al. Surgical excision versus Mohs’ micrographic surgery for primary and recurrent basal-cell carcinoma of the fa a prospective randomised controlled trial with 5-years’ follow-up. Lancet Oncol. 2008; 9:1149-56.
22. Galimberti G, Pontón Montaño A, Ferrario D, Kowalczuk A, Galimberti R. Mohs micrographic surgery for the treatment of basal cell carcinoma. Actas Dermosifiliogr. 2010; 101:853-7.