ORIGINAL
Gorlin-Goltz syndrome: management of facial basal cell carcinoma
Gorlin-Goltz syndrome: management of facial basal cell carcinoma: 顔の基底細胞癌の管理
Rocío Gilabert Rodrígueza, Pedro Infante Cossíob, Pablo Redondo Parejob, Eusebio Torres Carranzab, Alberto García-Perla Garcíab and Domingo Sicilia Castroa
aService of Plastic and Reconstructive Surgery(整形外科の診療所)。 Hospital Universitario Virgen del Rocío, Seville, Spain
bService of Oral and Maxillofacial Surgery, Hospital Universitario Virgen del Rocío, Seville, Spain
Address for correspondence
Summary
Introduction/Objectivity: ゴーリン-ゴルツ症候群(GGS)は、主に基底細胞癌や上顎角化嚢腫などの腫瘍が増殖しやすい常染色体優性遺伝性の疾患である。 GGSの患者様に発生する基底細胞癌は、通常多発性で、臨床的に多形性を示し、性差はなく、時に人生の早い時期に発見され、日光の当たらない部分にも発生することがあります。 その臨床行動は様々ですが、特に顔面に対して非常に攻撃的になることがあります。 GCS患者における基底細胞癌の挙動を検討するため、2001年から2011年にかけて当院で治療を受けた患者のうち、本疾患の基準を満たした患者を対象に調査を実施した。
材料と方法:GGGの臨床診断および/または遺伝子診断を受けた11名の患者を対象とした。 年齢と性別による分布、臨床症状、組織学的特徴、使用した手術手技、再発の有無、患者の進化を調査した。
結果:36%の患者さんが顔面に基底細胞癌を有していました。 1人当たりの腫瘍数は9個から21個で、外科的切除が望ましい治療法であったが、すべての患者が新たな病変を生じ、数回の手術を必要とする再発を経験した。 組織学的検査では、28%の病変で腫瘍が手術断端に接触または近接していることが判明した。
結論 SGGの基底細胞癌の管理に利用可能な様々な方法の中から選択する治療法を決定するための文献上の証拠は不十分である。 7019>
Key words: Gorlin-Goltz Syndrome. ネボイド基底細胞腫症候群。 基底細胞癌。
ABSTRACT
はじめに/目的:Gorlin Goltz症候群(GGS)は、主に基底細胞癌や顎角化嚢胞などの腫瘍が増殖しやすい常染色体優性遺伝性の疾患である。 GGS患者様の基底細胞癌は、通常、多型の臨床的特徴、性別に関係なく好発し、時に人生の早い時期に発生し、日光に当たらない部位にも発生します。 臨床的挙動は様々で、特に顔面に非常に侵襲的な場合がある。 そこで、GGS患者における基底細胞癌の挙動を検討するために、2001年から2011年の間に当院で治療を受けた本疾患の基準を満たした患者を対象に調査を行った。
材料と方法:本研究では、臨床診断および/または遺伝子診断でGGSと診断された11名の患者を対象とした。 性・年齢,臨床的側面,組織学的特徴,実施した外科的治療,再発の有無,経過観察について検討した。
結果: 患者の36%に顔面に基底細胞癌が見られた。 1人当たりの腫瘍数は9~21個であった。 治療は外科的切除が望ましいとされたが,全例に新たな病変と再発が生じ,数回の手術を必要とした。 組織学的研究により、28%の病変で腫瘍が手術断端に接触または近接していることが明らかになった。
結論:GGSにおける基底細胞癌の管理に利用可能な様々な方法の中から選択すべき治療法を決定するための文献上の証拠は不十分である。
Key words: Gorlin-Goltz Syndrome. ネボイド基底細胞癌症候群. 基底細胞癌。 顎角化嚢胞
はじめに Gorlin-Goltz症候群(GGS)は、1960年にGorlinとGoltz1によって報告された症候群である。 彼らはまず、本症の特徴である多発性基底細胞癌、上顎角化嚢胞、二分肋骨の三徴候について説明した。 別名、母斑基底細胞症候群、母斑基底細胞癌症候群などとも呼ばれ、常染色体優性遺伝、不完全浸透、表現型が多様な遺伝病であることが知られるようになりました2,3。 9番染色体(9q22, 3-q31)に存在する腫瘍抑制遺伝子であるPatched(PTCH)遺伝子の変異によって引き起こされます。 その推定有病率は国によって1:57,000から1:164,000と差があり、一般に受け入れられている平均有病率は約1:60,000です4。
GGS は、臨床的に多発性新生物の発生傾向および発達異常の発生によって特徴づけられる疾患です。 臨床的な発症は小児期または思春期に起こり、多数の基底細胞癌や上顎歯原性角化嚢胞の存在など、多くの症状の関連性を伴う。 その他、掌蹠角化症、骨格異常、異所性頭蓋内石灰化症、顔面異形成(巨頭症、唇顎裂、高度眼球異常)5などが認められる。 約5%の症例で知的障害が見られる。 また、眼、泌尿器、心血管系の疾患も見られることがあります6 。 悪性髄芽腫はGGS患者様の5-10%に発生し、早期死亡の原因となる可能性があります。 2つの主要な臨床基準、または1つの主要な臨床基準と2つのマイナーな臨床基準を満たす場合に診断が成立する5(表1)。 7019>

腫瘍は、発癌促進遺伝子または腫瘍抑制遺伝子が変化した結果、SGGで発生するものです。 後者は発癌促進遺伝子の抑制機能を発揮する。 基底細胞癌の場合、どの癌原遺伝子が関与しているかは明らかでない。 RAS経路が変化しているが、すべての症例で変化しているわけではない。 腫瘍抑制遺伝子に関しては、p53がこの腫瘍の発生に二次的な役割を果たしているようだ。 これらの患者が皮膚癌になりやすいのは、突然変異の影響を受けた細胞が、DNA修復機構の変化により日光の影響を受けやすくなるためと思われる。 基底細胞がんは、皮膚のどの部分にも発生しますが、主に紫外線にさらされる部分、主に顔、背中、胸に発生します。 一般人に発生する基底細胞癌とGBS患者さんに発生する基底細胞癌には、ある種の違いがあります。 後者では、数が多く、外観が多形で、性別に偏りがなく、日光の当たらない場所でも発症することがあります。 GTSの基底細胞癌の管理について利用可能な臨床的証拠のほとんどは、本症候群に罹患していない患者を対象に行われた研究から得られたものである。
本研究の目的は、Seville Universitario Virgen del Rocío病院(スペイン)で過去10年間にGBSを治療した患者の臨床研究に基づき、臨床挙動と診断・治療基準を評価するためにGBS患者における顔面基底細胞癌の管理を分析することであった。
材料と方法
2001年から2011年に口腔顎顔面外科と形成外科で受診したGTSと診断された患者の臨床記録を観察的、後方視的に調査しました。 GGSの臨床診断および/または遺伝子診断を受けた11名の患者を対象とし、診断を受けているにもかかわらず臨床歴が不完全な患者を除外した。 疫学的データ(年齢と性別)と内科・外科的データ(病変の数と位置、病理組織学的診断、使用した手術手技、再発の有無と経過)を分析した。 臨床的フォローアップは定期的な検診で平均4.5年であった。
結果
患者の平均年齢は27歳で,男性(73%)が大半を占めた。 45%の症例では、診断時の年齢が20歳未満であった。 臨床診断は9名(主要基準2名、主要基準1名、軽微基準2名)、遺伝子診断が2名であった。 3名に家族歴があった(表2)。

臨床的特徴(表3)では、上顎角化嚢胞が最も頻繁に見られる臨床症状で、標本の91%(10名)に見られた。 次いで、骨格の変化(63%)、特徴的な筋膜炎(54%)となっています。 11人中4人(36%)が基底細胞癌を発症した(表4)。 一人当たりの病変数は9から21で、一人の患者さんでは正確な病変数が記録されていない。 いずれも顔面部を中心に(図1、2)、次いで頸部、背部となっている。 全例に外科的切除が行われた(図3)。 病理検査では、ほとんどの症例で結節性組織が認められ、高い割合で手術断端が侵されていた(28%の病変で腫瘍が断端に接触または近接していた)。 全例で1回以上の手術介入が行われた。
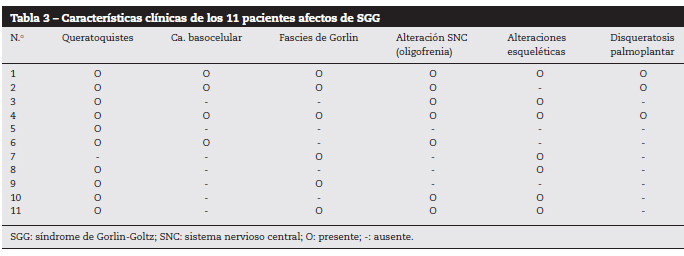

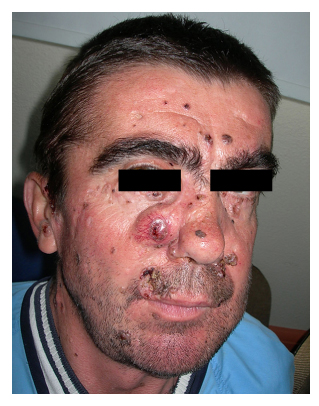
図1 患者番号6。
複数の顔面基底細胞癌。
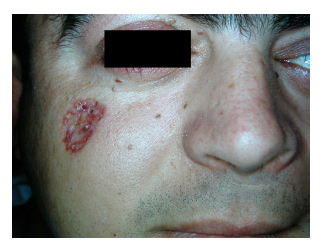
図2. 患者番号2 頬に
基底細胞癌を示す

図3 患者番号1
A:顔面と頸部に多発した基底細胞癌の術前画像です。
B:切除後の術後詳細
患者番号4は、顔面下3分の1に再発した複数の基底細胞癌を発症し、下顎骨切除を含む積極的な切除と2連続フリーフラップ(線維骨胸膜と前腕筋膜)による即時再建を必要としました(図4)。 患者番号6は下顎骨体部に角化嚢胞を伴う表皮癌を呈し、その結果死亡した

図4である。 A:顔面下3分の1に再発した基底細胞癌。
B:骨と神経周囲への浸潤を示す3D-CT再構成。
C:下顎骨切除を伴う積極的な切除を行う。
D: 2枚の連続したフリーフラップによる複合再建
(骨軟骨腓骨と小掌筋腱付き前腕筋膜腓骨)。
E:術後パノラマX線写真。
F: 患者の術後画像
Discussion
出発点として、過去10年間にSGGに関して発表された科学的情報を評価するために文献調査を行ったところ、主に皮膚科、口腔外科、歯科および遺伝学の分野の雑誌で、この話題に対する関心が高まっていることが判明した。 基底細胞癌は最も頻度の高い再発性病変の一つであり、また、部位的にも(特に顔の皮膚に)目に付きやすく診断が容易であるためか、最も多くの論文が皮膚科の雑誌にまとめられている。 次に頻度の高い順に、口腔顎顔面外科、歯科、遺伝学の分野の雑誌である。 上顎角化嚢胞は本症候群で最も頻度の高い病変であり、しばしば診断の方向性を示す徴候である。 上顎角化嚢胞を認めなかったのは1人だけであったが、この患者は年齢が若かったため、角化嚢胞の発生に時間がかからなかったと考えられる(患者番号7)。 明らかに男性の関与が優勢であったが、文献には性別の偏りは記載されておらず、サンプル数が少ないことから、この事実から結論を導き出すことはできない。 表現型の高いSGGの典型的な4例(患者番号1、2、4、6)があり、最も優勢な臨床症状(上顎角化嚢腫と基底細胞癌)が見られることがわかる。 多くの場合、罹患した親が想定されるが、我々のシリーズではそうではなく、罹患した家族が少なくとも一人判明している患者はわずか3人(文献では70-80%)である(表2)。 SGGの11例中4例が基底細胞癌を発症した。 これは、36%の病変であり、本疾患で古典的に考えられている90%の頻度と比較すると低い割合である。 一部の患者さんの年齢が若いことも重要なポイントです。 本症候群では出生時においてもこれらの病変が認められるが、これは標準的なものではなく、臨床的な発現には危険因子(紫外線)にさらされた数年間が必要であるとされている。 しかし、このシリーズの基底細胞癌患者の平均年齢は39歳(最年少19歳)であった。
基底細胞癌は、特に赤道に近い地理的地域の白人で、皮膚の白い人の紫外線への曝露と関連して、最もよく見られる悪性皮膚腫瘍の一つと考えられている。7 一般集団において、この疾患は人生の6~7年の間に起こり、近年その発生率がかなり上昇してきている。 一般的には、60歳代から70歳代にかけて発症し、近年その発症率はかなり高まっています。 基底細胞癌の主な原因は、慢性的な日光への暴露であり、その結果、病変は一般的に顔、耳、首、頭皮、肩、背中など、体の露出部に発生します。 紫外線(短期および長期)、特定の化学発がん物質(ヒ素、炭化水素)、電離放射線、慢性的な刺激などにさらされることが原因として知られています。 色素性乾皮症や基底細胞母斑症候群(BNS)など、いくつかの症候群型がある8。
BNSにおける基底細胞癌の管理はあまり研究されておらず、主に保存療法に言及されている。 Pauwelsらは、SGG患者の基底細胞癌の治療法として光線力学的療法を選択し、手術と比較して良好な結果を得たことを発表した9。 Micaliらは、GTS患者の基底細胞癌の治療における局所イミキモドの役割を分析し、この治療法は、複数の外科的切除よりもそれを好む患者の高い協力により、有効な選択肢であると強調しました10。 一般集団における基底細胞癌の管理に関する研究では、外科的治療(単純切除、縁辺浸潤病変の臨床的経過観察)が他の治療法よりも際立っている11-13。 一般集団における基底細胞癌の挙動はGTSのそれとは異なるが、他の具体的な研究がなされるまでは、我々が持つ豊富な経験をこれらの患者に適用することがより合理的であると思われる。
基底細胞癌の治療には病変部の完全除去が必要だが、これはいくつかの方法によって行うことが可能である。 外科的切除は最も一般的な処置であり、特に小・中規模の病変では治癒率が高いことから、これが最良の選択肢であるという見解で一致しているようである。 腫瘍の特徴(数や大きさ)や一般的な患者要因(年齢、麻酔リスクなど)により、手術が禁忌とされる患者には、その他の選択肢(凍結療法、電極掻爬術、放射線療法、局所化学療法など)が用いられる14。 これらの腫瘍は、神経周囲への浸潤や多発性により非常に侵襲的になる可能性があり、特に再発例では、患者4で発生したように、複雑な再建を必要とする欠損を残す広範囲な切除が必要となることがあります。 切除断端が明確であれば治癒と判断する。 他の治療法と同様に、大きさ、部位、組織学的サブタイプが全体の予後に寄与しています。 サージカルマージンの限界については、統一した勧告はありません。 7019>
Management is controversial in tumours in whichatomic pathology report indicates that margins are involved.多くの外科医は、小さな、よく囲まれた病変では少なくとも面積と深さの両方で3~5mmのマージンを選び、大きな、侵襲性の病変では1cm以上のマージンを選んでいる。 非共発性患者を対象とした様々な研究により、断端陽性率は4~16.6%と報告されている15-18。 我々のシリーズでは、28%の病変が組織学的に近接および/または浸潤した縁を有しており、一般集団で報告されたものと比較して高い割合であった。 文献によると、頭頸部領域は断端への浸潤率が高く、これは高貴な解剖学的構造を傷つけずに腫瘍を切除することの難しさによって説明されるかもしれない16,17。 基底細胞癌の患者を追跡調査した大規模なシリーズでは、不完全切除の病変では5年後の再発率は25%しか観察されていない13。 外科的再手術の後、患部断端の28-54%しか示されないことを念頭に置き、その後の経過観察と保存的管理を行うことが、これらの症例では最も賢明なアプローチであると思われる19,20。 15-18 SGG患者において、このような経過観察と観察の姿勢は、組織学的断端が近接・陽性で神経周囲への進展が認められない腫瘍で、検査が容易に行える部位にある場合、新しいがんが散発的に発生する可能性が高いこととその多領域性を考慮すると、長期的にはその部位に何度か追加の外科的処置を要する可能性もあり、非常に好ましいと思われる。
Mohs micrographic surgeryは、危険部位(眼瞼、眼窩縁など)の再発病変に対する外科的治療法です21。 また、臨床特性(組織サブタイプ、境界が不明瞭、再発傾向)や部位により高リスクに分類される腫瘍にも適応となります22。 その利点は、深部と表面の両方において、手術のマージンを100%コントロールすることができる手術の方法論に基づいています。 7019>
SGGは完治しないが、早期診断により、太陽光線への曝露による新たな基底細胞癌の出現や顎を破壊する多発性角化嚢胞などの合併症を回避するための集学的アプローチを提供することができる。 基底細胞がんは、転移はしないが、皮膚の深層に浸潤すると深刻な侵襲を受ける悪性腫瘍である。 SGGの基底細胞癌の治療において、外科的切除が最も有効な選択肢であることを考えると、術後の後遺症を減らすために、病変が小さいうちに治療を試みるという予防医学的アプローチが重要であると言えます。 SGGについては、多くの論文が発表されているように、多くの経験を持つ専門家がいますが、プライマリーケアはこの分野には存在せず、早期診断、ひいては早期治療開始、予後改善のために、この分野の専門家の健康教育やトレーニングを推進することが必要です。 いくつかの疫学研究の結果、基底細胞癌のリスクは紫外線曝露と強い正の相関を示しており、したがって、これらの患者は過度の日光曝露を避けるべきであることが示されている。 同様に、放射線治療も基底細胞癌の発生や再発のリスクがあるため、可能であれば避けるべきです。 皮膚病変を回避するために化学予防を行うことができる。
以上のことから、GGS患者における基底細胞癌は、PTCH遺伝子の変異による腫瘍抑制機構の変化と関連しており、特に紫外線との関係で散発的に発生することが示唆された。 SGG患者と一般住民の基底細胞癌の臨床的特徴には、主に病変数(SGGで多い)、発症年齢(SGGで低い)、挙動(SGGで高い侵襲性と再発率)の点で違いがある。 11人の患者のレビューでは、36%が顔面に基底細胞癌を呈していた。 文献上最も広く認められている治療法は外科的切除であり、我々の全例でもこの治療法が採用された。 我々のシリーズでは、28%の腫瘍で組織学的断端が近接していたり、損なわれていたりしたが、これは非症候群集団のシリーズと比較して高い割合であった。 初回治療後に新たな病変や再発が発見された割合は100%であった。 SGGの基底細胞癌の管理に利用可能な様々な治療法の中から証拠に基づく決定を行うには、文献における既存のデータは不十分である。 紫外線を浴びない予防的なアプローチが推奨されます。
倫理的責任
人と動物の保護。 本研究のために、人体や動物に対する実験が行われていないことを宣言する。
データの機密性。 この記事には患者さんのデータは一切登場しないことを宣言しています。
プライバシーとインフォームドコンセントへの権利。 著者らは、この論文に患者データが掲載されていないことを宣言する。
利益相反
著者らは、利益相反がないことを宣言する。
参考文献
1. Gorlin RJ, Goltz RW.(共著)。 多発性母斑基底細胞上皮腫、顎膿胞、二分肋。 症候群である。 N Engl J Med. 1960; 262:908-12.
2. Stoelinga PJ, Peters JH, van de Staak WJ, Cohen MM. 基底細胞母斑症候群のいくつかの新しい知見。 Oral Surg Oral Med Oral Pathol. 1973; 36:686-92.
3.トッテンJR. 多発性母斑基底細胞癌症候群。 一家4代に渡って発生した報告。 がんです。 1980; 46:1456-62.
4. Visioli F, Martins CA, Heitz C, Rados PV, Sant’Ana Filho M. Nevoid basal cell carcinoma syndromeは本当に稀なのか? ケースシリーズに基づく調査プロトコルの提案。 J Oral Maxillofac Surg. 2010; 68:903-8.
5. Evans DG, Ladusans EJ, Rimmer S, Burnell LD, Thakker N, Farndon PA. 母斑基底細胞癌症候群の合併症:集団ベースの研究の結果。 J Med Genet。 1993; 30:460-4.
6. Díaz-Fernández JM, Infante-Cossío P, Belmonte-Caro R, Ruiz-Laza L, García-Perla-García A, Gutiérrez-Pérez JL.を参照。 基底細胞母斑症候群。 6 症例の提示と文献レビュー。 メッド口腔Patol口腔Cir Bucal。 2005; 10 Suppl 1:E57-66。
7. Roewert-Huber J, Lange-Asschenfeldt B, Stockfleth E, Kerl H. Epidemiology and aetiology of basal cell carcinoma(基底細胞腫の疫学と病因). Br J Dermatol. 2007; 157 Suppl 2:47-51.
8. Kyrgidis A, Tzellos TG, Vahtsevanos K, Triaridis S. New concepts for basal cell carcinoma. 人口統計学的、臨床的、組織学的危険因子、およびバイオマーカー。 腫瘍発生のリスク、二次原発の可能性、および再発に関するエビデンスの系統的レビュー。 J Surg Res. 2010; 159:545-56.
9. Pauwels C, Mazereeuw-Hautier J, Basset-Seguin N, Livideanu C, Viraben R, Paul C, et al. 基底細胞母斑症候群の患者における局所アミノレブリン酸メチル光力学療法による基底細胞癌の管理は、患者の満足度を高め外科的処置の必要性を減少させる。 J Eur Acad Dermatol Venereol.2011; 25:861-4.
10. Micali G, de Pasquale R, Caltabiano R, Impallomeni R, Lacarrubba F. Topical imiquimod treatment of superficial and nodular basal cell carcinomas in patients affected by basal cell nevus syndrome: a preliminary report. 2002; 13:123-7.
11. Chren MM, Torres JS, Stuart SE, Bertenthal D, Labrador RJ, Boscardin WJ. 非黒色腫皮膚癌の治療後の再発:前向きコホート研究(Prospective Cohort Study). 2011; 147:540-6.
12. Wallace DL, Jaffe W. Reply to: 基底細胞癌は従来の外科的完全切除後に再発するか? R.W. グリフィス、S.K.、Suvarna. J. ストーン BJPS. 2005; 58:795-805. J Plast Reconstr Aesthet Surg 2006;59:1247.
13. Sherry KR, Reid LA, Wilmshurst AD. 基底細胞癌切除術の5年間のレビュー。 J Plast Reconstr Aesthet Surg. 2010; 63:1485-9.
14. Kopera D, Cerroni L, Fink-Puches R, Kerl H. 母斑基底細胞癌症候群の患者の管理における異なる治療法。 J Am Acad Dermatol.
15. 基底細胞癌の不完全な切除:さらなる手術の価値は? Oral Maxillofac Surg. (Epub ahead of print).
16. Farhi D, Dupin N, Palangié A, Carlotti A, Avril MF. 基底細胞癌の不完全切除:連続した362症例における割合と関連因子。 皮膚外科 2007; 33:1207-14.
17. Bogdanov-Berezovsky A, Cohen A, Glesinger R, Cagnano E, Krieger Y, Rosenberg L. Clinical and pathological findings in reexcision of incompletely excised basal cell carcinomas. 2001; 47:299-302.
18. 手術で治療された基底細胞癌における不完全切除の発生率:レトロスペクティブ臨床監査。 このような場合、「痒いところに手が届く」という言葉があります。
20. Anthony ML. 非黒色腫皮膚癌の外科的治療。 AORN J. 2000; 71:552-4. 556-8, 560-4.
22. Galimberti G, Pontón Montaño A, Ferrario D, Kowalczuk A, Galimberti R. Mohs Micrographic Surgery for the treatment of basal cell carcinoma. Actas Dermosifiliogr。