US Pharm. 2015;40(12):HS5-HS11.
ABSTRACT : La cirrhose est un diagnostic hétérogène qui a un impact sur la fonction hépatique, notamment sur le métabolisme et la clairance des médicaments, mais l’effet exact reste flou. Des idées fausses et une variabilité de pratique importante existent parmi les professionnels de la santé concernant l’utilisation d’analgésiques chez les patients souffrant de dysfonctionnement hépatique. Sur la base de données limitées sur l’innocuité et l’efficacité, l’acétaminophène est l’analgésique préféré chez les patients atteints d’une maladie du foie qui ne boivent pas activement, et il peut être dosé jusqu’à 2 à 3 g/jour. Les anti-inflammatoires non stéroïdiens (AINS) doivent être évités en raison de leurs effets indésirables d’insuffisance rénale, de rétention hydrique et de risque accru de saignement. Les opioïdes doivent être utilisés avec précaution et initiés avec des produits à libération immédiate à faibles doses avec des intervalles prolongés et une surveillance étroite. Tous les analgésiques doivent être titrés avec précaution pour obtenir un soulagement sûr et adéquat de la douleur chez les patients souffrant d’insuffisance hépatique.
La cirrhose est définie comme une fibrose hépatique permanente secondaire à une lésion ou à un dommage. Il s’agit d’un diagnostic hétérogène, entraînant des degrés variables de formation de nodules, de dysfonctionnement des organes, de complications, ainsi qu’une morbidité et une mortalité importantes. Les causes de la cirrhose comprennent l’abus d’alcool, l’hépatite B et C, le cancer et la stéato-hépatite non alcoolique.1 Les » maladies chroniques du foie et cirrhose « , en tant que diagnostic principal, ont représenté plus de 101 000 admissions à l’hôpital en 2010.2 En 2013, elles ont été signalées comme la principale cause de décès chez les personnes âgées de 25 à 64 ans, et la 12e cause de décès pour tous les âges, entraînant plus de 36 000 décès2.
Malheureusement, ces chiffres peuvent être sous-estimés en raison des limites des critères diagnostiques des codes de la Classification internationale des maladies (CIM), qui ne prennent pas en compte les complications liées à la cirrhose. Une étude suggère que les décès liés au foie pourraient être jusqu’à deux fois plus élevés que ce qui est actuellement rapporté par le CDC.3
Les prestataires de soins de santé connaissent bien le rôle vital du foie dans le métabolisme et la clairance de nombreux médicaments. La cirrhose peut entraîner le développement de shunts porto-hépatiques, diminuant finalement le métabolisme de premier passage qui se produit avec de nombreux médicaments oraux. La diminution de la production d’albumine peut également entraîner une augmentation des concentrations libres de médicaments fortement liés aux protéines. On pense généralement qu’à mesure que le dysfonctionnement hépatique progresse, l’élimination des médicaments est altérée ; cependant, les patients atteints d’hépatite chronique ou de cancer hépatique, en l’absence de cirrhose, peuvent n’avoir qu’une faible modification de la clairance des médicaments.4 On ne sait toujours pas dans quelle mesure la cirrhose affecte l’élimination des médicaments.
Bien que certains médicaments aient des paramètres d’ajustement rénal spécifiques, les ajustements de dose hépatiques peuvent ne pas être facilement disponibles. De nombreuses études ont évalué la pharmacocinétique et les taux sériques d’analgésiques des patients, qui ne sont pas nécessairement en corrélation avec la réponse des patients. D’autres études disponibles se sont principalement concentrées sur l’hépatite C, bien que de nombreux patients développent un dysfonctionnement hépatique et une cirrhose secondaires à d’autres causes. Les scores de Child-Pugh, qui ne sont pas couramment calculés dans la pratique, orientent souvent la posologie, mais les recommandations qui en résultent peuvent encore être vagues, en l’absence de directives claires pour l’application clinique. La prise en charge des patients peut être encore compliquée par une insuffisance rénale concomitante, qu’elle soit liée à la maladie hépatique, comme le syndrome hépatorénal, ou à une autre cause.4
Utilisation d’analgésiques dans la cirrhose
La prise en charge de la douleur est souvent un défi pour les professionnels de santé, mais elle reste une composante très importante de la prestation de soins de qualité aux patients et constitue un facteur commun de la satisfaction des patients.5 Une prévalence élevée de la douleur a été constatée chez les patients atteints d’une maladie hépatique chronique, entre 32% et 77%.6-8 La douleur et les régimes antidouleur à base d’opioïdes se sont avérés être des prédicteurs significatifs de l’utilisation des soins de santé chez les patients atteints d’une maladie hépatique.8
Une étude rétrospective a révélé que 77% des patients avant une greffe de foie (n = 108) ont signalé des douleurs corporelles, plus d’un tiers indiquant des sites multiples.7 La douleur aurait affecté le travail, le sommeil, la mobilité, l’appétit, le plaisir et l’humeur. Environ 90 % d’entre eux ont déclaré avoir reçu un traitement pharmacologique, mais seulement 33 % ont perçu un soulagement. Des opioïdes à courte durée d’action ont été prescrits dans 40 % des cas, et 32 % des patients ont déclaré s’être vu prescrire cinq analgésiques ou plus. Les auteurs ont conclu que la douleur chez les patients atteints de maladie hépatique en phase terminale (ESLD) est très fréquente, qu’elle a un impact sur la fonctionnalité et qu’elle est souvent sous traitée, malgré les nombreuses thérapies pharmacologiques prescrites7.
La polypharmacie a été suggérée comme une approche courante de la gestion de la douleur, probablement due à des prescripteurs trop prudents utilisant de très faibles doses de plusieurs médicaments plutôt qu’une titration et une optimisation minutieuses d’un nombre réduit d’agents.7 La polypharmacie augmente les coûts, complique la compréhension de l’efficacité des agents, crée des doublons thérapeutiques et augmente le risque inhérent d’interactions médicamenteuses et d’effets indésirables. La gestion de la douleur dans la cirrhose présente un domaine complexe de la pharmacothérapie avec des considérations uniques de pathophysiologie hépatique altérée et un équilibre fin entre le soulagement adéquat de la douleur et l’évitement d’effets indésirables potentiels importants.7
Acetaminophène
Il est communément admis que l’acétaminophène doit être évité chez les patients souffrant de dysfonctionnement hépatique en raison de son risque bien connu d’hépatotoxicité en cas de surdosage. Ce risque est directement lié à la saturation d’autres voies métaboliques et à la déplétion des réserves de glutathion (GSH).5 Environ 5% de l’acétaminophène est métabolisé par les enzymes CYP450 (principalement 2E1, ainsi que 1A3 et 3A4) en un métabolite réactif, la N-acétyl-p-benzoquinone imine (NAPQI). En présence de GSH, la NAPQI est conjuguée et excrétée par voie rénale. Lorsque le GSH n’est pas disponible, la NAPQI s’accumule et provoque la nécrose et l’apoptose des hépatocytes.
Les alcooliques peuvent développer une induction du CYP2E1 en raison de l’ingestion chronique d’alcool et avoir des niveaux de GSH diminués par la malnutrition. De tels changements physiologiques peuvent entraîner un risque accru de lésions hépatiques induites par l’acétaminophène chez ces patients. Par conséquent, il est à craindre que tous les patients atteints de cirrhose présentent des taux de GSH plus faibles et un risque accru d’hépatotoxicité avec l’acétaminophène. Bien qu’une demi-vie prolongée ait été documentée chez les patients atteints de cirrhose, aucune étude prospective à long terme n’est disponible pour évaluer la sécurité de l’acétaminophène. Certaines études suggèrent que les lésions hépatiques sont rares avec une posologie appropriée et que l’acétaminophène est bien toléré dans les maladies hépatiques chroniques stables jusqu’à 4 g/jour, sans aucun signe d’augmentation de l’activité du CYP ou d’épuisement critique des réserves de GSH.5,9,10
Des doses quotidiennes totales d’acétaminophène de 2 à 3 g sont recommandées pour une utilisation à court et à long terme chez les patients cirrhotiques qui ne consomment pas activement d’alcool, selon l’avis des experts.4,5 Contrairement à la croyance commune, l’acétaminophène est considéré comme l’agent privilégié en cas de dysfonctionnement hépatique lorsqu’il est maintenu dans une limite de dose quotidienne totale, mais il doit être évité chez les patients qui consomment activement de l’alcool.4,11,12 L’acétaminophène IV est contre-indiqué en cas d’insuffisance hépatique grave et de maladie hépatique active grave13.
Anti-inflammatoires non stéroïdiens (AINS)
Chez les patients cirrhotiques, des altérations du métabolisme et de la biodisponibilité sont attendues avec les AINS en raison d’un métabolisme CYP et d’une liaison protéique importants.5 Cependant, la préoccupation pour les patients atteints de cirrhose concerne principalement les effets physiologiques des AINS. Ces médicaments inhibent la synthèse des prostaglandines, ce qui entraîne une diminution du débit sanguin rénal et du taux de filtration glomérulaire (TFG) ainsi qu’une altération de l’excrétion rénale du sodium et de l’eau, ce qui peut aggraver l’ascite et augmenter le risque de syndrome hépatorénal chez les patients atteints de cirrhose.4 Les AINS sont connus pour provoquer une irritation, une ulcération et une perforation gastro-intestinales et augmenter le risque global de saignement chez les patients en raison de l’inhibition de la production de thromboxane A2 par les plaquettes.4,5 En raison de la thrombocytopénie, de la diminution de la synthèse des facteurs de coagulation et des varices œsophagiennes associées à l’hypertension portale, les patients atteints de cirrhose peuvent présenter un risque accru d’hémorragie, qui peut mettre leur vie en danger4. Pour ces raisons, les AINS doivent être évités en cas de cirrhose.
Opioïdes
Les opioïdes sont la classe de médicaments la plus courante pour l’analgésie, en particulier pour les douleurs modérées et sévères ou les douleurs non soulagées par l’acétaminophène et les AINS. Les opioïdes peuvent contribuer à des complications importantes en cas de cirrhose, notamment en précipitant une encéphalopathie, ce qui justifie la prudence quant à leur utilisation.5 Il est raisonnable de garder à l’esprit que les effets des opioïdes peuvent être inversés par la naloxone, tandis que les complications d’une douleur non traitée ou insuffisamment traitée peuvent être importantes.14 Les opioïdes peuvent être nécessaires après que les traitements non pharmacologiques et non opioïdes appropriés ont donné des résultats insuffisants.7
L’oxydation est la principale voie métabolique des opioïdes (souvent via les enzymes CYP), à l’exception de la morphine, et on considère qu’elle est affectée par un dysfonctionnement hépatique.4,15 L’oxydation est réduite en cas de maladie hépatique, ce qui entraîne une diminution de la clairance du médicament et/ou une augmentation de la biodisponibilité orale avec une réduction du métabolisme de premier passage. Alors que l’on pense que la glucuronidation est moins affectée par un dysfonctionnement hépatique léger à modéré, elle peut être importante en cas de maladie grave.4 En gardant ces considérations à l’esprit, certains opioïdes sont considérés comme sûrs, efficaces et préférables aux AINS pour la gestion de la douleur modérée à sévère avec l’utilisation de doses réduites et d’intervalles prolongés. Cependant, en raison de l’imprécision des recommandations, la décision est souvent laissée au jugement clinique du praticien.15 Les agents à longue durée d’action ne peuvent être envisagés qu’après avoir déterminé le dosage sûr et efficace des agents à courte durée d’action.5
Tramadol : Le tramadol subit un métabolisme hépatique à plus de 80 %.4 Bien que l’on s’attende à ce qu’il procure un moindre soulagement de la douleur chez les patients cirrhotiques en raison d’une biotransformation réduite, cela n’a pas été observé dans les études cliniques.4 Une étude a noté une différence significative dans la concentration maximale (Cmax) et le temps maximal (Tmax), une clairance réduite de moitié et une demi-vie d’élimination jusqu’à 3 fois le contrôle chez 20 patients atteints de malignité hépatique par rapport à 10 témoins sains.16 Les auteurs recommandent de prolonger l’intervalle posologique, considérant que le tramadol à 50 mg toutes les 12 heures est sûr et efficace. D’autres ont recommandé 25 mg toutes les 8 heures en cas de dysfonctionnement hépatique.5 Les ressources d’information sur les médicaments, comme Lexicomp, recommandent 50 mg toutes les 12 heures pour les patients atteints de cirrhose et précisent que le produit à libération prolongée ne doit pas être utilisé chez les patients présentant un dysfonctionnement hépatique sévère (classe C de Child-Pugh).17
Le tramadol peut être bénéfique dans les douleurs rebelles en raison de son inhibition partielle du recaptage de la sérotonine et de son activité sur les voies périphériques de la douleur.5 La prudence est de mise avec le tramadol chez les patients ayant des antécédents de convulsions et en association avec d’autres médicaments sérotoninergiques, en raison de son effet d’abaissement du seuil de convulsion et du développement possible d’un syndrome sérotoninergique, respectivement. La dose et la fréquence du tramadol doivent également être réduites en fonction de la fonction rénale.17
Hydrocodone et oxycodone : L’hydrocodone et l’oxycodone dépendent des CYP2D6 et 3A4 pour leur métabolisme en leurs métabolites plus puissants, l’hydromorphone et l’oxymorphone, respectivement.5 L’effet analgésique de ces médicaments peut être moins puissant chez les patients souffrant de dysfonctionnement hépatique en raison d’une diminution de la conversion en leurs métabolites actifs, tandis qu’une diminution de la clairance et une demi-vie prolongée peuvent produire plus d’effets indésirables.4,5 Il est recommandé d’initier le traitement avec des doses plus faibles et des intervalles prolongés, en prévoyant un temps adéquat entre les doses pour éviter l’accumulation et en titrant selon la réponse du patient. Il faut faire preuve de prudence avec les produits combinés à base d’acétaminophène (par exemple, Vicodin, Percocet), en s’assurant que la dose quotidienne totale d’acétaminophène ne dépasse pas la limite recommandée de 2 à 3 g/jour, toutes sources confondues.5
Morphine : La morphine est considérée comme ayant une extraction hépatique élevée lors du métabolisme de premier passage, ce qui fait qu’elle n’est biodisponible qu’à hauteur de 30 à 40 % après administration orale chez des patients en bonne santé.4,5 La morphine est métabolisée par le foie en morphine-6-glucuronide (métabolite actif) et en morphine-3-glucuronide (métabolite inactif ayant des effets neurotoxiques potentiels), qui sont ensuite éliminés par voie rénale. Avec un métabolisme de premier passage réduit chez les patients cirrhotiques, la morphine est probablement plus biodisponible et des doses orales plus faibles sont recommandées.4,5,15 Les études ont constamment montré une diminution de la clairance et une demi-vie prolongée de la morphine chez les patients cirrhotiques. Il a été recommandé d’augmenter jusqu’à deux fois l’intervalle entre les doses pour éviter l’accumulation du médicament, tant en administration IV qu’orale.5 La morphine doit être évitée en cas d’insuffisance rénale, y compris le syndrome hépatorénal, en raison de l’accumulation importante de ses métabolites et du risque de neurotoxicité.4
Hydromorphone : Certaines études rapportent une Cmax augmentée jusqu’à quatre fois après une dose unique d’hydromorphone à libération immédiate chez des patients présentant une maladie hépatique modérée, en raison d’une diminution du métabolisme de premier passage en cas de dysfonctionnement hépatique et d’une extraction hépatique élevée.4 Il a été recommandé de commencer par des doses plus faibles mais de maintenir un intervalle posologique similaire.4,5 La pharmacocinétique de l’hydromorphone n’a pas été étudiée chez les patients présentant une maladie hépatique sévère. La clairance de l’hydromorphone semble être relativement peu affectée, en particulier par un dysfonctionnement rénal. Cependant, il a été suggéré que l’hydromorphone ne soit pas utilisée en cas de syndrome hépatorénal en raison du risque observé d’accumulation de son métabolite neuroexcitateur, l’hydromorphone-3-glucuronide.4
Fentanyl : Bien que le fentanyl soit fortement lié aux protéines, on pense qu’il n’est pas affecté par la cirrhose.4,5,15 Le fentanyl peut être mieux toléré chez les patients cirrhotiques, car il n’a pas de métabolites toxiques.4 Cependant, le fentanyl peut ne pas être l’agent le plus approprié en raison de sa puissance très élevée et d’autres scénarios cliniques (ex, douleur aiguë, gestion ambulatoire et nécessité d’une administration orale).15
L’utilisation de timbres transdermiques de fentanyl a été recommandée comme option de première ligne pour les douleurs rebelles par certains auteurs, mais cela est controversé car on a constaté que les patients atteints de cirrhose présentaient des concentrations Cmax et une aire sous la courbe (AUC) élevées lors de l’utilisation des timbres, 35 % et 73 % respectivement.4,5,18 Il est important de se rappeler que l’utilisation d’un timbre de fentanyl ne doit être envisagée qu’une fois que les besoins en opioïdes ont été déterminés par la titration d’opioïdes à courte durée d’action.15 Il est recommandé d’initier le traitement à 50 % de la dose habituelle en cas d’insuffisance hépatique légère à modérée et d’éviter l’utilisation en cas d’insuffisance hépatique grave.18 Le fentanyl est considéré comme une bonne option en cas d’insuffisance rénale, et l’administration IV peut être envisagée en cas de syndrome hépatorénal, car c’est l’un des opioïdes les moins affectés par le dysfonctionnement rénal.4,5
Mépéridine : Dans la pratique actuelle, la mépéridine est rarement utilisée pour l’analgésie en raison du risque de convulsions avec l’accumulation de son métabolite, la normépéridine. Bien que les concentrations de normépéridine puissent être moindres en raison de la diminution de l’activité du CYP chez ces patients, il existe une biodisponibilité accrue liée à une diminution de la liaison aux protéines et à un retard de la clairance, et le métabolite peut toujours s’accumuler.4,5,15 La mépéridine doit être évitée en cas de cirrhose.
Codéine : Chez les patients sains, l’effet analgésique de la codéine est variable en raison de la variation phénotypique du CYP2D6, affectant la conversion en morphine. Chez les patients présentant un dysfonctionnement hépatique, les taux sériques de codéine peuvent être plus variables en raison d’une diminution de l’activité du CYP, entraînant une diminution de l’effet analgésique.4,5,15 En raison d’un manque général d’études chez les patients cirrhotiques, la codéine n’est pas recommandée.
Méthadone : Pour la gestion de la dépendance aux opiacés, la méthadone est souvent utilisée. Ce médicament présente de nombreux défis en raison de sa variabilité interindividuelle importante en matière de biodisponibilité, de liaison aux protéines et de sa longue demi-vie.4,5,15 Il est principalement métabolisé par le CYP3A4.15 Une accumulation peut se produire lors de l’administration de doses répétées en cas de dysfonctionnement hépatique grave, et les concentrations plasmatiques peuvent être élevées en cas d’ingestion aiguë d’alcool4. L’utilisation de la méthadone pour l’analgésie chez les patients atteints d’une maladie du foie n’a pas été étudiée ; elle n’est donc pas recommandée pour cet usage chez ces patients.4 Cependant, les avantages des programmes d’entretien à la méthadone surveillés pour la dépendance aux opioïdes, comme l’abus d’héroïne, peuvent l’emporter sur les risques potentiels.5
Buprénorphine : L’administration orale de buprénorphine, un agoniste opioïde mu partiel, entraîne un métabolisme de premier passage important et un faible effet analgésique, alors que l’administration sublinguale permet à environ 50 % à 55 % du médicament d’éviter l’inactivation par le CYP3A4.4,15 Malheureusement, aucune étude sur la buprénorphine n’est actuellement disponible pour déterminer si des ajustements de dose sont nécessaires ou si la pharmacocinétique reste inchangée en cas d’insuffisance hépatique. Des cas d’hépatite ont été signalés lors de l’utilisation de la buprénorphine chez des patients présentant un dysfonctionnement hépatique préexistant. Pour ces raisons, la buprénorphine doit être utilisée avec précaution chez les patients présentant une maladie hépatique.
Divers
Lidocaïne : L’utilisation de timbres topiques de lidocaïne est une considération courante pour le contrôle de la douleur localisée. Bien que la lidocaïne orale soit considérée comme ayant une extraction hépatique élevée avec un métabolisme de premier passage, aucune littérature n’a été trouvée discutant de la pharmacocinétique ou de l’utilisation de timbres de lidocaïne pour la gestion de la douleur chez les patients cirrhotiques19. La douleur en cas de dysfonctionnement hépatique peut être diffuse et/ou associée à une ascite, ce qui limite l’indication des patchs de lidocaïne topiques.7 En raison du manque de preuves et de la toxicité possible, la lidocaïne doit être utilisée avec prudence chez les patients souffrant de dysfonctionnement hépatique et uniquement pour les douleurs localisées.
Antidépresseurs tricycliques (TCA) : Les TCA ont longtemps été le pilier du traitement de la douleur neuropathique.5 Les TCA subissent un métabolisme de premier passage et une excrétion rénale. Ces agents sont bien connus pour leurs effets anticholinergiques, auxquels les patients cirrhotiques peuvent être plus sensibles. La constipation est une préoccupation importante, qui peut précipiter l’encéphalopathie hépatique chez ces patients. Ces médicaments doivent être utilisés avec précaution et seulement si nécessaire. S’ils sont utilisés, la nortriptyline et la désipramine peuvent être préférées en raison de leur plus faible puissance et de leur moindre sédation, tachycardie et hypotension orthostatique. Il est recommandé de commencer par de faibles doses en cas de maladie hépatique et de titrer lentement en fonction de la réponse du patient.4
Anticonvulsivants : Les anticonvulsivants jouent également un rôle dans la gestion de la douleur neuropathique (via la modulation des neurotransmetteurs), mais ces médicaments sont couramment métabolisés par le foie et excrétés par voie rénale.5 Des doses plus faibles et des intervalles prolongés peuvent être nécessaires chez les patients cirrhotiques. La carbamazépine est associée à une hépatotoxicité et doit être évitée chez les patients présentant un dysfonctionnement hépatique. La gabapentine est l’agent préféré, car elle n’est pas métabolisée par voie hépatique ni liée aux protéines, mais elle doit être ajustée en fonction de la fonction rénale.4
Résumé et recommandations
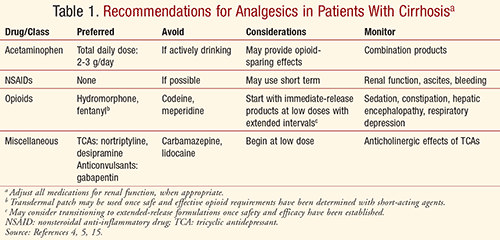
Avec tous les patients, la prise en charge de la douleur doit être individualisée en fonction des avantages par rapport aux risques, avec une surveillance étroite du soulagement de la douleur et des effets indésirables. La gestion de la douleur doit impliquer une approche multidisciplinaire d’interventions pharmacologiques, comportementales, psychologiques et physiques pour obtenir les meilleurs résultats et optimiser la qualité de vie, de manière sûre et efficace. Les praticiens doivent toujours garder à l’esprit le risque accru de lésions hépatiques induites par les médicaments chez les patients atteints d’une maladie hépatique préexistante, y compris la cirrhose.5 En gardant à l’esprit les profils pharmacocinétiques et d’effets indésirables des différents médicaments analgésiques, les praticiens doivent tenir compte des recommandations résumées dans le TABLEAU 1 pour obtenir un contrôle sûr et adéquat de la douleur chez les patients cirrhotiques.