Informe de un caso
Una masa omental: ¿Alguna idea?
Mascianà G*, Gallo IF, Valeri S y Coppola R
Departamento de Cirugía General, Campus Universitario Bio-Médico, Italia
*Autor correspondiente: Mascianà Gianluca, UniversitàCampus Bio-Medico, Via Alvaro delPortillo 21 – 00128 Roma, Italia
Publicado: 20 Jul, 2017
Cite este artículo como: Mascianà G, Gallo IF, Valeri S, CoppolaR. Una masa omental: ¿Alguna idea? AnnClin Case Rep. 2017; 2: 1406.
Abstract
El pseudomixoma extraperitoneal (PE) es un hallazgo raro, la causa más común es la ruptura de un mucocele del apéndice en el retroperitoneo. Aquí presentamos un caso de una paciente de 52 años con una masa en el abdomen derecho y un vago dolor abdominal inferior que fue sometida a la resección de una masa extraperitoneal encapsulada. El examen histopatológico reveló un seudomixoma mucinoso con un bajo grado de diferenciación. Presentamos un caso de pseudomixoma extraperitoneal con una revisión de la literatura.
Presentación del caso
Una paciente de 52 años fue remitida a nuestro hospital por una masa en el abdomen derecho y un vago dolor abdominal bajo. El único hecho destacable en su historia pasada era un fibroide neoplásico en la mama derecha que había sido extirpado 10 años antes.
Investigaciones
Un examen abdominal reveló una masa grande y fija en la región subcostal derecha. No había linfadenopatías cervicales, axilares o inguinales, ni signos de ascitis. Las demás pruebas fueron normales, salvo un ligero aumento del nivel de CEA (8,5 ng/ml; valor normal: 0-2,5). La tomografía computarizada (TC) de tórax y abdomen reveló una masa redondeada de 100 mm x 70 mm x 80 mm en el flanco derecho, con márgenes regulares, una cápsula parcial y una calcificación interna de 19 mm con calcificación mural y estrías centrales hiperdensas (figura 1). La aspiración de la masa, guiada por ecografía, dio como resultado un material celular. Las exploraciones endoscópicas superior e inferior fueron negativas.
Tratamiento
El caso se discutió en una reunión del equipo multidisciplinar. Ante la dificultad de realizar un diagnóstico preoperatorio, la paciente fue sometida a una intervención quirúrgica en la que se encontró una masa extraperitoneal encapsulada y libre de todas las estructuras circundantes, incluidos el páncreas, los riñones y el intestino. Esta masa se resecó completamente sin romper la cápsula. El análisis histopatológico reveló un pseudomixoma mucinoso con un bajo grado de diferenciación.La inmunohistoquímica fue positiva para CK20 y CK7. La paciente fue dada de alta 4 días después de la cirugía sin ninguna complicación. En el seguimiento, 3 años después, no había signos de recidiva.
Figura 1
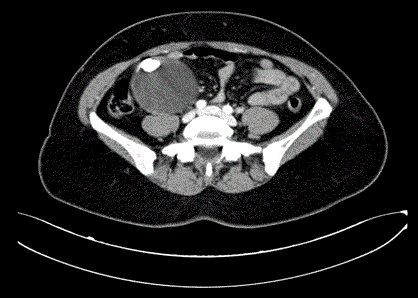
Figura 1
Exploración por TAC del abdomen y la pelvis, demostrando la masa en el abdomen derecho.
Tabla 1
Título grande
| Autor | Paciente (edad/sexo) | Año de publicación | Tumor primario | Tratamiento |
| Bonnan | 37 M | 1948 | Mucocele de apéndice | Evacuación de quiste en procedimiento de 2 fases |
| Precoz | 57 M | 1968 | Mucocele de apéndice | Disolución del tumor |
| Temprana | 63 M | 1968 | Apéndice | Excisión |
| Brady | 67 M | Apéndice | Quimioterapia retroperitoneal de citorreducción quirúrgica | |
| Moran | 58 M | 1988 | NA | Drenaje, apendicectomía y repetición del drenaje. Quimioterapia, radioterapia agentes mucolíticos, hipertermia por radiofrecuencia |
| Baker | 33 M | 1988 | Rectum | Drenaje, omentectomía |
| Snyder | 50 F | 1992 | Apéndice | Escisión, omentectomía, histerectomía total y ooforectomía |
| Fann | 47 M | 1993 | NA | Excisión |
| Radosavljevic | 41 M | 1993 | Apéndice | Quimioterapia |
| Shelton | 81 M | 1994 | Cistadenoma mucinoso apendicular | Disección y apendicectomía |
| Tamai | 39 NA | 1995 | Adenocarcinoma mucinoso apendicular | Hemicolectomía derecha, resección del músculo iliopsoas derecho, peritonectomía parcial |
| Baba | NA | 1995 | Cistadenoma mucinoso apendicular | NA |
| Mor | 65 M | 1996 | Cistadenocarcinoma apendicular | Disección y apendicectomía |
| Ben-Hur | 65 M | 1996 | Apendicectomía | Excisión |
| Stevens | 56 M | 1997 | Adenocarcinoma mucinoso apendicular | Drenaje, radioterapia |
| Tsai | 69 M | 1998 | Adenoma mucinoso apendicular | Drenaje |
| Matsuoka | 58 F | 1999 | Cistadenoma mucinoso (primario o secundario | NA |
| Koizumi | 46 M | 1999 | Adenocarcinoma mucinoso apendicular | Hemicolectomía derecha |
| Edrees | 53 F | 1999 | Adenocarcinoma mucinoso apendicular adenocarcinoma | Hemicolectomía derecha y quimioterapia sistémica de cribado |
| Peek | 38 M | 1999 | Apéndice | Excisión, quimioterapia |
| Koizumi | 53 M | 1999 | Apéndice | NA |
| Al-Bozom | 75 M | 2000 | Apéndice | Quimioterapia |
| Kojima | 78 F | 2001 | Cistadenocarcinoma apendicular | Hemicolectomía derecha |
| Angelescu | NA M | 2001 | Quiste paraentérico mucinoso | NA |
| Liu | 68 F | 2001 | Adenocarcinoma mucinoso apendicular | Apendectomía debulking de mucosa, quimioterapia intraoperatoria, quimioterapia sistémica |
| Solkar | 57 M | 2004 | NA | Excisión de quiste radioterapia quimioterapia |
| Hirokawa | 55 F | 2004 | Cáncer de colon ascendente | Hemicolectomía u ooforectomía derecha, extirpación de la mucosa. Quimioterapia sistemática A |
| Niwa | 80 F | 2007 | Adenocarcinoma mucinoso apendicular | Extracción de mucosa e íleon, ciego ambos ovarios y útero |
| Cakmak | 51 F | 2009 | Adenocarcinoma mucinoso apendicular | Resección en bloque con apendicectomía de una porción de hueso ilíaco, quimioterapia sistémica y radioterapia |
| Chamisa | 48 F | 2011 | Ovario | Disección de ooforectomía derecha y quimioterapia |
| Ioannidis | 74 M | 2012 | Adenocarcinoma de mucinosis apendicular | Disolución derecha hemicolectomía quimioterapia |
| Ioannidis | 68 F | 2012 | Adenocarcinoma mucinoso apendicular | Debullición Hemicolectomía derecha quimioterapia |
| Lim | 53 F | 2014 | Apéndice | Histerectomía abdominal total, salpingooforectomía bilateral, omentectomía, apendicectomía y citorreducción no óptima |
| Mavrodin | 56 F | 2014 | Apendicectomía | Apendicectomía, histerectomía total con anexectomía derecha, omentectomía |
| Spyropoulos | 70 F | 2014 | Apéndice | Hemicolectomía derecha |
| 84 M | 2014 | NA | Inspeccionado y palpado sin reconocimiento del apéndice | |
| Joo | 80 F | 2015 | Ovario | Salpingooforectomía bilateral con adhesiolisis masiva y escisión de una masa en el espacio retroperitoneal |
| Martines | 66 F | 2015 | Apéndice | Lavado peritoneal, histerectomía, salpingooforectomía bilateral, omentectomía y apendicectomía |
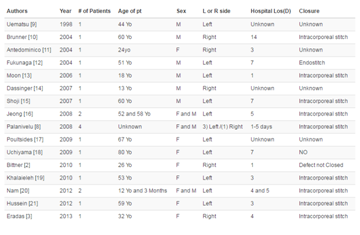
Tabla 1: 37 casos reportados apéndice.
Tabla 1
37 casos reportados apéndice.
Figura 2
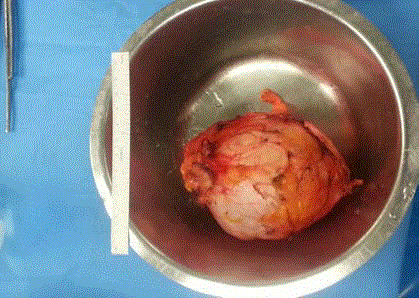
Figura 2
Espécimen quirúrgico.
Discusión
Werth describió por primera vez el pseudomixoma peritonei en 1884 como la presencia de material mucinoso y gelatinoso en la cavidad peritoneal. En 1948, Bonann describió un pseudomixoma que afectaba sólo al retroperitoneo, que posteriormente fue expuesto por Coppini en 1950. Veinte años más tarde, Early describió un mucocele retroperitoneal del apéndice que contenía 10 litros de moco y que no se había roto, lo que permitió realizar una escisión curativa completa; esto fue denominado por Moran como pseudomixoma extra peritonei (PE) en 1988. Shelton etal. lo denominaron posteriormente Pseudomyxoma retroperitonei. El pseudomixoma retroperitoneal es una enfermedad rara de la que sólo se han descrito 37 casos en la literatura; la causa más común es la rotura del amucocele del apéndice en el retroperitoneo (Tabla 1). Afecta a ambos sexos en la misma medida, prevalentemente después de los 60 años, con otras localizaciones primarias potenciales que incluyen un neoplasma mucinoso del ovario o del intestino, o un cistadenoma/cistadenocarcinoma primario retroperitoneal; un análisis histopatológico revela agregados de células mucinosas y epiteliales que muestran grados variables de atipia y diferenciación. Las células suelen ser positivas para CK20 y negativas para CK7. El pseudomixoma puede clasificarse como grado I oadenomucinosis peritoneal diseminada benigna, como grado II o subtipo intermedio, y como grado III o carcinomatosis mucinosa peritoneal maligna. En la mayoría de los casos, la patogénesis del pseudomixoma retroperitoneal se explica por una fuga a través del peritoneo (presentación retroperitoneal asociada a un pseudomixoma intraperitoneal). En ausencia de pseudomixoma peritoneal, una variante de la anatomía del apéndice (localización retroperitoneal) puede explicar el pseudomixoma extraperitoneal, aunque esta hipótesis es todavía especulativa. El diagnóstico preoperatorio es muy raro; son frecuentes los síntomas como la fatiga, la disminución del apetito con pérdida de peso, la presencia de una masa palpable y el dolor abdominal o lumbar de progresión lenta. El CEA y el CA 19.9 están aumentados entre el 56% y el 75% y entre el 58% y el 67% de los pacientes, respectivamente. La ecografía puede detectar la mucina como líquido retroperitoneal y ayudar a realizar el diagnóstico mediante la aspiración con aguja, mientras que la TC con contraste intravenoso, oral y rectal puede distinguir la sustancia mucinosa del líquido acuoso normal mediante el análisis de las propiedades de densidad (5-20 unidades Hounsfield para la mucina frente a 0 unidades Hounsfield para el agua). En la TC, la pseudomixomaretroperitonei aparece como una masa que a menudo es multiquística, tiene septos o paredes gruesas y puede caracterizarse por calcificaciones murales que desplazan las estructuras adyacentes . CirugíaEl tratamiento del pseudomixoma difiere sustancialmente dependiendo de si es intraperitoneal o extraperitoneal. En el caso del pseudomixoma intraperitoneal, Sugarbaker et al. recomiendan una intervención quirúrgica agresiva y compleja que incluye la extirpación del material mucinoso, la citorreducción y la peritonectomía para eliminar la mayor cantidad posible de enfermedad macroscópica (cirugía citorreductora, CRS) con quimioterapia hipertérmica intraperitoneal (HIPEC).En cambio, el tratamiento recomendado para el pseudomixoma extraperitoneal es, al igual que para la enfermedad benigna, la resección del lugar de origen, a veces seguida de quimioterapia sistemática. Glehen et al. informaron de una mediana de supervivencia de 156 meses, con tasas de supervivencia a 5 y 10 años del 72% y el 55%, respectivamente, en 501 pacientes con pseudomixomaperitonei que habían sido sometidos a RSC (completa o incompleta) seguida de HIPEC. La mayoría de los pacientes (~70%) se sometieron a una citorreducción completa. Este enfoque de tratamiento uniforme ha dado lugar a una supervivencia a 10 años mejor que la registrada en los controles históricos. Aunque no se dispone de datos sobre el uso de quimioterapia hipertermia-retroperitoneal, este tratamiento debería considerarse debido a la elevada tasa de recidiva. CirugíaEl riesgo de recidiva es tal que el seguimiento, basado en un examen físico, una TC y marcadores séricos, es esencial. El tratamiento combinado en el pseudomixoma retroperitoneo se asocia a una supervivencia de 20 años en hasta el 70% de las pacientes, mientras que la tasa de supervivencia del pseudomixoma intraperitoneo, en el que están implicadas las estructuras abdominales vitales, es más corta.
- Werth R. Pseudomyxomaperitonei. Arch Gynaecol. 1884; 24: 100-118.
- Bonnan LJ, Davis JG. Mucocoele retroperitoneal del apéndice. A case report with characteristic roentgen features. Radiology. 1948; 51: 375-382.
- Coppini B. Su di un rarissimo caso di pseudomixoma retroperitoneale di probabile origine appendicolare. G Clin Med. 1950; 31: 601-612.
- Early KS, Stephenson DV, Davis WC. Mucocele retroperitoneal gigante que simula pseudomixomaperitonei y adenocarcinoma mucinoso. Am J Surg. 1968; 116: 439-443.
- Moran CJ, Morgan RH. Pseudomyxoma extraperitonei. J Roy Soc Med. 1988; 81: 668-669.
- Shelton MW, Morian JP, Radford DM. Pseudomixoma retroperitonei asociado a apendicistadenoma. Am Surg. 1994; 60: 958-960.
- Ioannidis O, Cheva A, Paraskevas G, Papadimitriou N, Konstantara A, Chatzopoulos S, et al. Pseudomyxomaretroperitonei: informe de 2 casos y revisión de la literatura. Rev Esp Enferm Dig. 2012; 104: 268-275.
- Pai RK, Longacre TA. Tumores mucinosos apendiculares y pseudomioperitoneos: características histológicas, problemas diagnósticos y propuesta de clasificación. Adv Anat Pathol. 2005; 12: 291-311.
- Smeenk RM, Verwaal VJ, Zoetmulder FA. Pseudomyxoma peritonei. Cancer Treat Rev. 2007; 33: 138-145.
- Smeenk RM, Bruin SC, van Velthuysen ML, Verwaal VJ. Pseudomy- xoma peritonei. Curr Probl Surg. 2008; 45: 527-575.
- Al-Bozom IA. Presentación extraperitoneal de pseudomixoma peritonei como masa escrotal: informe de un caso y revisión de la literatura. Ann Saudi Med. 2000; 20: 297-299.
- Lee NK, Kim S, Kim HS, Jeon TY, Kim GH, Kim DU, et al. Spectrum of mucin-producing neoplastic conditions of the abdomen and pelvis: crosssectional imaging evaluation. World J Gastroenterol. 2011; 17: 4757-4771.
- Sugarbaker PH. Pseudomixomaperitonei. Un cáncer cuya biología se caracteriza por un fenómeno de redistribución. Ann Surg. 1994; 219: 109-111.
- Glehen O, Mohamed F, Sugarbaker PH. Citorreducción incompleta en 174 pacientes con carcinomatosis peritoneal por malignidad apendicular. Ann Surg. 2004; 240: 278-285.
- González-Moreno S, Sugarbaker PH. La hemicolectomía derecha no confiere una ventaja de supervivencia en pacientes con carcinoma mucinoso del apéndice y siembra peritoneal. Br J Surg. 2004; 91: 304-311.
- Hinson FL, Ambrose NS. Pseudomyxoma peritonei. Br J Surg. 1998; 85: 1332-1339.
- Sugarbaker PH. ¿Nuevo estándar de atención para los neoplasmas epiteliales apendiculares y el síndrome de pseudomixomaperitonei? Lancet Oncol. 2006; 7: 69-76.