Thomas A. Oetting, MS, MD
Konversion till extrakapsulär kataraktutdragning (ECCE) kommer ofta vid en svår tidpunkt. Linsen är på väg att falla söderut, glaskroppen har prolapserat och kirurgen är stressad. Det är viktigt att förstå stegen och processen för konvertering till ECCE, och studier före krisen kommer att bidra till att lindra stressen när denna oundvikliga process inträffar. Vi kommer att behandla flera områden: identifiering av patienter med risk för behov av konvertering till ECCE, indikationer för konvertering, konvertering från topisk till sub-Tenons, sårförberedelse, uttryckning av linsmaterialet, stängning av såret, placering av IOL, postoperativa frågor och ett kort avsnitt om främre vitrektomi.
Patienter med risk för konvertering till ECCE: En av de viktigaste delarna av den preoperativa processen för kataraktpatienter är att bedöma de faktorer som ökar den kirurgiska svårigheten och som kan leda till konvertering till ECCE eller på annat sätt komplicera ingreppet: Du kanske vill lägga till operationstid i ditt schema eller be om ytterligare utrustning. Du kanske vill byta till ett överlägset limbalsår som underlättar konvertering till ECCE i stället för ett temporalt klart corneasnitt. Du kanske vill göra en retrobulbar blockering i stället för lokal anestesi eftersom fallet kan ta längre tid eller är mer sannolikt att bli komplicerat. I vissa situationer får de preoperativa riskfaktorerna dig att överväga att bjuda in någon mer erfaren person för att göra fallet.
Svårighetsfaktorer (i fallande ordning efter betydelse)1
- Zonulär laxitet (pseudoexfoliation-PXF, anamnes på trauma, Marfans syndrom etc.)
- Rockhårda linser (röda eller svarta linser)
- Pupillstorlek (varför är den liten? PXF, diabetes s/p laser, central posterior synechiae – CPS, floppy från tamsulosin/Flomax)
- Kan inte ligga platt särskilt länge (t.ex. kronisk obstruktiv lungsjukdom – KOL, klaustrofobi, tremor, allvarlig fetma)
- Stort ögonbryn som begränsar den övre åtkomsten
- Smal vinkel som begränsar det främre kammarutrymmet
- Predisposition för hornhinnedekompensation: (t.ex. Fuch’s dystrofi eller corneal guttata, PPMD, hård kärna)
- Svaga röda reflexer vit/svart katarakt som försvårar kontinuerlig curvilinear capsulorhexis (CCC)
- Förfluten kirurgi, t.ex. befintlig trab eller tidigare pars plana vitrektomi (PPVx)
- Predisposition för exponering:
- : Botox, tidigare ögonlockstrauma, diabetes mellitus (DM)
- Antikoagulantia (t.ex.g., warfarin/Coumadin, asparin)
- Monokulär patient
| Faktor | Tid | Utrustning/Anestesi | |
|---|---|---|---|
| Zonular Laxity | Double |
|
|
| Rock Hard Lens | Add 50% |
|
|
| Small Pupil | Tillägger 50% |
|
|
| Flomax | Tillägg 50% |
|
|
| Svaga röda reflexer | Tillägg 50 % |
|
|
| Big Brow | Tillägg 25% |
|
|
| Narrow Angle | Add 25% |
|
|
| Predisposition för hornhinnedekompensation | 0% |
|
|
| Existerande Trabeculectomy bleb | 0% |
|
|
| Prior vitrektomi (PPVx) | 0% |
|
|
| Kan inte ligga platt | 0% |
|
|
| Antikoagulant Använd | 0% |
|
|
| Monokulär patient | 0% |
|
|
| (modifierad från Oetting, Cataract Surgery for Greenhorns, http://medrounds.org/cataract-surgery-greenhorns) | |||
Indikationer för konvertering: Konvertering till ECCE är indicerat när phakoemulsifiering misslyckas. Ibland beror detta på en mycket hård lins som inte ger efter för ultraljud eller en lins som är tillräckligt hård för att kirurgen är orolig för att den nödvändiga ultraljudsenergin ska skada en tentativ hornhinna (t.ex. Fuchs’ endotelial dystrofi eller posteriör polymorf dystrofi ). Ibland övergår man till ECCE när en felaktig capsulorhexis blir radiell, särskilt med en hård kristallin lins, när kirurgen är orolig för att risken för att linsen ska falla ner är för stor vid fortsatt phakoemulsifiering. En kirurg kan välja att konvertera till ECCE när den främre kapseln är svår att se och kapsulorhexis måste fullbordas med burköppnare-tekniken (med användning av Trypanblå färgning är detta dock mindre vanligt). Oftare är konverteringen indicerad när den kristallina linsen är lös på grund av svaga zonuli eller en reva i den bakre kapseln som gör phakoemulsifiering mindre säker än att utvidga såret och avlägsna det kvarvarande linsmaterialet. Indikationer för konvertering till ECCE inkluderar:
- Hård kristallin lins eller instabilt endotel
- Radialremiss i främre kapsel med hård lins
- Dålig visualisering trots Trypanfärgningsmedel
- Posteriortal kapselremiss
- Zonulära dialys
Konvertering till sub-Tenons anestesi. Ofta omvandlar vi fall från topisk clear corneal till ECCE. Även om ECCE kan göras under topikal är det vanligtvis bekvämare och säkrare att ge ytterligare bedövning som vanligtvis är en subtenoninjektion med bupivicain och lidokain. Detta ger en viss akinesi och ytterligare anestesi. Det förekommer vanligen subkonjunktival blödning och om injektionen görs för framifrån kan den orsaka kemoisis och ballongbildning i bindhinnan. Stegen för sub-Tenons injektion beskrivs nedan:1
- Förbered en 3cc-spruta med lika delar 2 % lidokain/0.75% bupivakain
- Placera lacrimalkanylen (eller Masketkanylen) med en mjuk kurva för att närma sig globen
- Välj en kvadrant för blocket (bäst är att välja en lateral kvadrant för att undvika de sneda musklerna)
- Låt patienten titta bort från den valda kvadranten för att öka exponeringen
- Använd .12 för att dra tillbaka conjuctiva
- Gör ett litet snitt ner till sclera med Wescott-saxen
- Omdirigera Wescott-saxen med kurvan neråt och dissekera trubbigt genom kvadranten
- Dissektera förbi ekvatorn (liknande som att använda Stevens tenotomisaxen i pedi/retina)
- Använd .12 Forceps för motdrag
- Placera kanylen genom snittet och dirigera förbi ekvatorn innan du injicerar
- Lokalbedövningsmedlet ska flyta lätt och orsaka lite kemos — Om inte, omskär med Wescott-saxen för att komma mer bakre
- Använd 2-3 cc av lokalblandningen
Tång som håller öppen den bakre lappen av dissektionen till subtenonsutrymmet. Lacrimal canula med mjuk kurva som närmar sig globens kurva redo att föra in lokalbedövningsmedel.
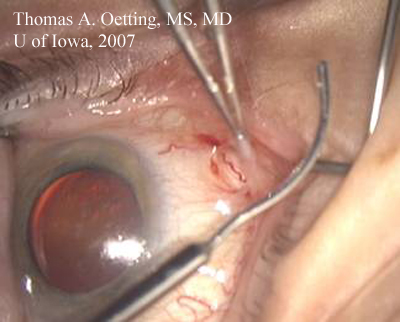
Konvertering av såret: Det viktigaste steget för att konvertera till ECCE är att antingen förlänga det befintliga såret eller stänga och göra ett nytt. ECCE kommer att kräva ett stort snitt på från 9-12 mm som försluts med sutur. Beslutet att utvidga det befintliga såret eller göra ett nytt sår beror på flera faktorer: det ursprungliga sårets läge, brynets storlek, tidigare kirurgisk historia och eventuellt behov av framtida kirurgi.
| Originalsår | Fördelar med att göra ett nytt sår för ECCE | Fördelar med att förlänga befintligt sår för ECCE |
|---|---|---|
| Temporal |
|
|
| Supero-temporal (vänster öga) |
|
|
| Infero-temporal (höger öga) |
|
|
| Superior |
|
|
Att göra ett nytt snitt under konverteringen är identiskt med det för en planerad ECCE. Det ursprungliga snittet försluts med en 10-O nylonsutur. Kirurgen och mikroskopet roteras eftersom kirurgen ska sitta överordnat. Stegen för att göra ett nytt överlägset snitt är följande:
- Konjunktival peritomi på cirka 170 grader
- Använd 64- eller halvmåneblad för att göra limbala rännan med en ackordlängd på 11 mm
- Bipolär kauteri för hemostas
- Använd keratome för att göra det första snittet med början i rännan in i AC
- Förläng det första snittet till rännans hela längd (med sax eller kniv)
- Säkerhetssuturer placeras i förväg (vanligen 7-0 Vicryl)
.
Det kan vara svårt att utvidga ett befintligt snitt och tekniken är annorlunda för skleraltunnlar jämfört med tydliga hornhinnesnitt. I båda fallen förs dock den ursprungliga förlängningen till limbus. När det gäller ett ursprungligt skleralt snitt förs snittet framåt så att det ansluter till limbus i båda ändar innan det förlängs längs limbus till en längd av ca 11 mm. När det gäller ett befintligt hornhinnesnitt förs hornhinnesnittet bakåt mot limbus innan såret förlängs längs limbus med en ackordlängd på cirka 11 mm. När iriskrokar används i en diamantkonfiguration kan såret förlängas för att bevara den subincisionella kroken och den stora pupillen.2
- Konjunktival peritomi på cirka 170 grader
- Använd 64- eller halvmåneblad på vardera sidan av det befintliga såret för att göra ett limbalt spår med en ackordlängd på 11 mm
- Bipolär kauteri för hemostas
- Användning. halvmånebladet för att föra befintligt skleralsår framåt eller befintligt hornhinnesår bakåt för att ansluta till limbus
- Förläng det ursprungliga snittet till spårets hela längd (med sax eller kniv)
- Säkerhetssuturer placeras i förväg (vanligtvis 7-0 Vicryl)
För att ta bort linsen: Man måste vara mycket försiktigare när man tar bort kärnan under den typiska omvandlingen till ECCE som följer med glaskroppsförlust. Först måste den främre kapseln vara tillräckligt stor för att låta nucleus komma ut, vilket kan kräva relaxerande snitt i vissa fall. När zonulerna är svaga eller den bakre kapseln är trasig kan linsen inte tryckas ut med vätska eller externt tryck, vilket ofta görs vid en planerad ECCE med intakt kapsel/zonulerna. Efter att eventuell glaskropp avlägsnats (se nedan) måste linsen försiktigt slussas ut ur främre kammaren med minimalt tryck på globen. Om den bakre kapseln och zonlorna är intakta kan linsen uttryckas enligt beskrivningen med en planerad ECCE.
Uttag av lins med intakt kapselkomplex:
- Mobilisera linsen (fysiskt med cystotom eller med hydrodissektion – var försiktig)
- Linsen avlägsnas med linseslinga eller med mot-tryckteknik
- Såret försluts med säkerhetssuturer och ytterligare central Vicryl-sutur
- Kortikalt material avlägsnas med hjälp av I/A-anordning (antingen automatiserad eller manuell)
- Instilla oftalmisk viskoelastisk anordning (OVD)
- Linsen placeras i bakre kammaren
- Såret försluts med 10-O-nylon och Vicryl-suturer avlägsnas.
- OVD avlägsnas
Linsen avlägsnas med glaskroppen närvarande:
- Mobilisera linsen med Viscoat canulla (tippa linsen så att sårsidan är anterior)
- Släpp linsöglan under linsen, ”tå upp” instrumentet, ta bort linsen
- Såret försluts med säkerhetssuturer och ytterligare central vicrylsutur
- Anteriör vitrektomi (se nedan)
- Kortikalt material avlägsnas med hjälp av torr teknik eller främre vitrektor
- Instilla oftalmisk viskoelastisk anordning (OVD)
- Lins placeras i sulcus eller i främre chanber
- Såret försluts med 10-O-nylon och Vicryl-suturer avlägsnas
- OVD avlägsnas
Placering av IOL: Val av IOL vid ECCE-konvertering beror på det kvarvarande kapselkomplexet.3,4 Nyckeln till IOL-centrering är att få båda haptikerna på samma ställe: antingen båda i påsen eller båda i sulcus.
- När den bakre kapseln är intakt efter en konvertering till ECCE är den främre kapselöppningen vanligtvis dåligt definierad, vilket kan göra det svårt att placera påsen. Om den främre kapseln och därmed påsen är väldefinierad kan man placera en akryl-IOL i ett enda stycke utan att vika den direkt och försiktigt i påsen med hjälp av Kelman-pincett.
- När den bakre kapseln är intakt och den främre kapseln är dåligt definierad ska du placera en tredelad IOL i sulcus, t.ex. en stor silikon IOL eller MA50 akryl, genom att placera dessa direkt och ovikt i sulcus med Kelman-pincett. Se till att båda haptikerna är i sulcus.
- När den bakre kapseln är skadad, om tillräckligt med främre och bakre kapsel finns kvar för att stödja IOL:n, definiera sulcus med viscoat och placera IOL:n direkt i sulcus. Se till att båda haptikerna är i sulcus. Om IOL:n inte verkar stabil ska du placera McCannel-suturer för att fästa IOL:n vid iris eller ta bort och ersätta den med en AC IOL (glöm inte att placera en posteriort iridektomi med vitrektorn).
- När kapseln är allvarligt skadad och inte kan stödja en IOL ska IOL placeras i främre kammaren. Använd Kelman-tång för att placera IOL:n, säkra sedan kammaren och använd en Sinskey-krok för att placera AC IOL:n i sitt slutliga läge. (Glöm inte att placera en perifer iridektomi med vitrektorn).
Postoperativa problem: Postoperativ vård för patienter efter konvertering från phaco till ECCE är lite mer komplicerad och fokuserar på att förebygga cystoidt makulaödem (CME) och begränsa inducerad astigmatism. Ofta är vården mycket lik den för en planerad ECCE med cirka tre postoperativa besök (ett samma eller nästa dag, ett en vecka senare och ett cirka 5-6 veckor senare). Beroende på mängden astigmatism kan patienten behöva flera besök för att sekventiellt ta bort suturer samtidigt som man eliminerar inducerad astigmatism.
Första postoperativa besöket: Detta besök sker ofta samma eftermiddag (4-6 timmar efter operationen) eller nästa morgon med huvudsaklig tonvikt på att kontrollera IOP, leta efter sårläckage och söka efter kvarvarande linsmaterial eller glaskropp i främre kammaren. De flesta sårläckor bör förvisso sys, men om AC inte har bildats är det obligatoriskt att stänga dessa. Resterande kärnmaterial bör avlägsnas under de närmaste dagarna om det finns, men kvarvarande kortikalt material löses ofta upp med liten inflammation. Man kan förvänta sig dålig syn i 20/200-området på grund av astigmatism och ödem. Den främre kammaren bör bildas och har vanligtvis måttliga celler (10-20 celler/hpf med 0,2 mm stråle). Om IOP är mindre än 10 mmHg ska du söka noggrant med högt index av misstanke om läckage med hjälp av Seidel-test. Om IOP ligger i intervallet 10-29 är allt förmodligen okej om inte patienten är en vaskulopat, i vilket fall din övre gräns för IOP-tolerans bör sänkas. Om IOP ligger i intervallet 30-39 bör man överväga kammarundertryckning. Om IOP är >40 bör man överväga kammarundertryckning och ”burping” eller ”blödning” av IOP genom paracentes eller en främre kammartapp. IOP bör kontrolleras på nytt 60-90 minuter senare för att säkerställa att behandlingen är framgångsrik. Titta på fundus för att utesluta näthinneavlossning (RD) och choroidal utgjutning eller blödning. Vanligtvis sätts patienterna på prednisolonacetat 1 % 1 droppe 4 gånger dagligen (QID), cyklogyl 1 % 1 droppe 2 gånger dagligen (BID) och ett antibiotikum 1 droppe QID under nästa vecka.
Vecka 1 postoperativt besök: Synen och trycket bör förbättras dramatiskt hos patienterna under nästa vecka efter ett fall som konverterades till ECCE. Synen bör ligga i 20/100-området med pinhole-förbättring till cirka 20/50. Synen begränsas vanligen av kvarvarande ödem och astigmatism. I en studie av våra ECCE-fall fann vi cirka 7,0 dioptrier cylinder vid besöket efter en vecka. Du bör förvänta dig mycket lite inflammation och dokumentera att ingen RD finns. Sök efter kvarvarande linsmaterial i det främre segmentet och den bakre polen. Du kan avbryta cyklogylen och antibiotikan. Avtrappa långsamt prednisolonacetatetatet (t.ex. 1 gtt QID i ytterligare 7 dagar, sedan 1 gtt tre gånger dagligen i 7 dagar, sedan 1 gtt BID i 7 dagar, sedan 1 gtt QD i 7 dagar, sedan 1 gtt QD i 7 dagar) och sätt sedan ut. Om patienten löper risk för cystoidt makulaödem (CME), vilket är möjligt vid glaskroppsförlust, bör du fortsätta med prednisolon med den högre frekvensen (t.ex. QID) och påbörja ett icke steroida läkemedel (t.ex. aktuellt ketorolak eller motsvarande 1 gtt QID) fram till nästa besök 4-6 veckor senare.
Vecka 5 postoperativt besök: Synen bör fortsätta att förbättras när astigmatismen lägger sig och hornhinnan klarnar ytterligare. Ögat ska vara bekvämt. Synen bör ligga i 20/80-området och förbättras till 20/40 med pinhole. I vår studie var den astigmatism som inducerades av ECCE-suturer cirka 5,0 dioptrier vid snittet. Det främre segmentet bör vara lugnt och IOP normalt (såvida inte patienten är en ”steroidresponderare”). Överväg CME som en möjlighet hos patienter där konvertering krävdes eftersom dessa fall ofta är långa och kan medföra glaskroppsförlust. Utvärdera enligt klinisk indikation genom undersökning eller anamnes med optisk koherenstomografi (OCT) eller flouresceinangiografi (FFA).
Här i återhämtningen är huvudfrågan astigmatisk kontroll med borttagning av suturer. Använd keratometri, refraktion, streckretinoskopi eller topografi för att styra borttagningen av suturerna. Om keratometrin är 45,00 @ 90 och 40,00 @ 180, letar du efter täta suturer runt 90 grader (klockan 12) som orsakar 5 dioptrier av cylindern. Du kan ta bort endast en sutur vid 5 veckor, men vid utvärderingen efter 8 veckor kan du överväga att ta bort 2 suturer åt gången. Planen är att ta bort en sutur och se hur hornhinnan sätter sig. När astigmatismen är mindre än cirka 1,0-1,5 dioptrier bör du sluta ta bort suturerna och korrigera eventuell kvarvarande astigmatism med refraktion. Använd antibiotikadroppar profylaktiskt under några dagar efter varje suturborttagning. Efter det här besöket bör du överväga följande val vid varje besök (slösa inte för mycket tid på att tänka på andra möjligheter och kom ihåg att alla inte kommer att vara 20/20):
- dra ut ett stygn (dvs. cylindern vid stygnets axel är större än 1,0 till 1,5 dioptrier på manifest refraktion )
- ge glasögon (dvs. inget stygn att dra eller cylindern är mindre än 1 på MR)
- besök FFA eller OCT eftersom du misstänker CME
Anteriör vitrektomi. Konvertering till ECCE åtföljs nästan alltid av vitreus. Ibland kommer konverteringen när linsen är för hård och kapseln är intakt, men oftast verkar det som om konverteringen kommer när zonulerna eller kapseln släpper vitreus i den främre segmentkirurgens motvilliga händer. Vi kommer att behandla orsakerna och tecknen på glaskroppsprolaps och principerna för främre vitrektomi i olika situationer.
Causer för glaskroppsprolaps. Glaskroppen kommer antingen runt zonulerna eller genom en reva i den bakre kapseln. Bakre kapselrevor orsakas vanligen av 1) en främre reva som sträcker sig bakåt – vanligast, 2) en bakre reva – sekundärt till att phaknålen eller choppern är för djup, 3) under manipulation med I/A-instrumentet, eller 4) en befintlig skada (t.ex. posteriort polär katarakt, iatrogen från PPVx, eller från penetrerande linstrauma). Zonulära problem är ofta redan existerande (t.ex. på grund av trauma, PXF eller Marfans syndrom) men kan också vara iatrogena på grund av kraftig rotation av linsen eller dragning i kapseln under I/A.
Tecken på glaskroppsprolaps. Det första tecknet på glaskroppsprolaps är förnekelse. Något verkar vara fel men du kan inte riktigt peka ut problemet. Först förnekar man att det finns ett problem, men snart blir det tydligt. Fler tecken på vitreusprolaps är 1) fördjupning av kammaren, 2) utvidgning av pupillen, 3) linsmaterialet är inte längre centrerat, 4) linspartiklar kommer inte längre till phaco eller I/A, och 5) linsen roterar inte längre fritt. När du misstänker glaskroppsprolaps bör du placera dispersiv OVD i ögat innan du tar bort phaknålen eller I/A och kan kontrollera såret med en Weck-Cel (eller liknande pilsvamp) för glaskropp.
Grundläggande principer för främre vitrektomi. Nyckeln till en lyckad främre vitrektomi är att kontrollera ögats fluidik. Det första steget är att stänga kammaren. Detta är ofta svårt när man har konverterat till en ECCE eftersom såret är stort. Du måste dock stänga såret så att den enda utgången för vätska är aspirations-/skäranordningen. Separera spolningsanordningen från aspirations-/skäranordningen så att du kan skapa en tryckskillnad så att glaskroppen uppmuntras att gå till aspirations-/skäranordningen. Den sista viktiga punkten är att skära lågt och spola högt. Om du kan placera spolningsanordningen i den främre kammaren ovanför aspirationen/skäraren nära den bakre kapselns plan kommer glaskroppen att lämna den främre kammaren.
|
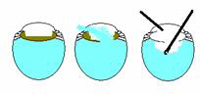 |
I allmänhet bör flaskans höjd vara låg – precis tillräckligt hög för att AC ska kunna bildas och inte så hög att vätska och eventuellt glaskropp trycks ut från ögat. Skärhastigheten bör vara så hög som möjligt vid skärning av glaskropp och låg vid skärning av kortikalt linsmaterial. Vi kommer separat att diskutera tidig, medellång och sen glaskroppsförlust nedan.
Vitreus Presenteras tidigt i fallet -medan det mesta av den kristallina linsen finns i ögat: Detta är den värsta tidpunkten för vitreusprolaps och man bör starkt överväga att konvertera till ECCE. De steg som bör övervägas beskrivs nedan:1
- Om det är aktuellt, gör en sub-Tenons-injektion (som beskrivits ovan)
- Överväg att stänga det temporala snittet med 10-0 och gör ett separat snitt med peritomi överst framför allt (som diskuterats ovan)
- Använd dispersivt viskoelastiskt medel för att lyfta linsen upp i närheten av såret och för att förflytta vitreus mer posteriort.
- Kan behöva Weck-Cel vitrektomi för att städa upp om glaskroppen är mycket prolapsad
- Använd linsslinga för att ta bort linsen (som beskrivits ovan)
- Håll en Wescott-sax redo när du loopar ut linsen för att skära glaskroppen
- Slut med 3 st vardera 7-0 Vicryl-säkerhetssuturer (en i mitten och en på vardera sidan 3 mm bort, vilket gör det möjligt att ta bort suturen i mitten för att placera 6 mm IOL)
- Möjligen behöver man lägga till lite 10-0 nylon vid sårkanterna för att vara säker på att det är vattentätt
- Anteriör vitrektomi (som diskuterats ovan, separera asp/skärare från spolare)
- Torrt avlägsnande av kvarvarande kortikalt material med en spruta på en 27-års kanyl
- Använd J-kanyl eller paracentes om det behövs för subincisionellt material
- Överväg färgning med Kenalog (se nedan)
- Placera IOL om möjligt i sulcus (justera styrka) eller använd en AC IOL (glöm inte perifer iridotomi)
- Miochol för att få ner pupillen – placerar IOL i sulcus, Pupillens topp hjälper till att upptäcka glaskropp
Glaskropp som uppträder i mitten av fallet – medan man tar bort kortikalt material: Detta verkar vara den vanligaste tidpunkten för förlust av glaskropp. Ofta får man den bakre kapseln precis när det sista kärnfragmentet tas bort. Det finns naturligtvis ingen anledning att övergå till ECCE i detta fall. Följande steg är användbara:1
- Placera viscoat i området med tår eller dialys innan man tar bort instrumenten
- Gör separat 1 eller 1.5 mm snitt för främre vitrektomi
- Separat spolning (genom paracentese) och asp/skärning (genom större paracentese)
- Kan behöva suturera det ursprungliga såret för att hålla kammaren formad
- Spola högt och skär/sug lågt – skapar en tryckgradient för att trycka tillbaka glaskroppen
- Inställningar lågt vakuum 100-område, låg flaskhöjd 50-område, max skärhastighet
- Försök att få bort en del av det kvarvarande kortikala materialet
- Torrt avlägsnande av kvarvarande kortikalt material med en spruta på en 27 gauge-kanyl
- Använd J-kanyl eller paracentes om det behövs för subinkisionellt material
- Överväg färgning med kenalog (se nedan)
- Placera IOL om möjligt i sulcus eller AC (om AC glöm inte perifer iridotomi)
- Miochol för att få ner pupillen
Hur man hanterar glaskroppar som kommer sent i fallet – när man placerar IOL: Detta är den minst problematiska och minst vanliga tidpunkten för att förlora vitreus. Huvudfrågan är att se till att IOL:n är stabil medan man tar hand om glaskroppen och sedan säkra en korrekt IOL i antingen AC, sulcus eller bag:1
- Placera viscoat i området med tår eller dialys innan man tar bort instrumenten
- Gör separat 1 eller 1.5 mm snitt för främre vitrektomi
- Separat spolning (genom paracentese) och asp/skärning (genom större paracentese)
- Kan behöva suturera det ursprungliga såret för att hålla kammaren formad
- Spola högt och skär/sug lågt – skapar en tryckgradient för att trycka tillbaka V:et
- Inställningar lågt vakuum 100 intervall, låg flaskhöjd 50 intervall, max skärhastighet
- Om sulcus kan bära en IOL, då
- Förflytta befintlig tredelad IOL till sulcus
- Ersätt en befintlig endelad IOL med-3-stycken IOL i sulcus
- Överväg att fånga optiken i främre kapsel om CCC är rund och centrerad
- Om revan i den bakre kapseln är rund och säker
- Placera viscoat i hålet
- Placera försiktigt en IOL i enstaka stycken i påsen (var mycket försiktig med 3-stycken IOL i 3-stycken IOL).bit lins i påsen)
- Miochol för att få ner pupillen
Färgning av glaskroppen med Kenalog: Scott Burk på Cincinatti Eye beskrev hur han använde Kenalog utanför märkningen för att färga vitreus som hade prolaberat in i främre kammaren5 (följ länken till Facebook-videon). Eftersom Kenalog inte är godkänt av FDA för denna indikation och eftersom vissa retnalkirurger har drabbats av steril (och till och med infektiös) endoftalmit efter att ha använt Kenalog, är användningen av Kenalog kontroversiell. Det är dock ett mycket användbart komplement till främre vitrektomi. Metoden för att blanda triamcinolonet (Kenalog) till en spädning 10:1 och för att tvätta bort konserveringsmedlet följer nedan:
- TB-spruta till uttagen 0.2 ml väl omskakad triamcinolon (40 mg/ml)
- Ta bort nålen och ersätt med ett 5 (eller 22) mikron sprutfilter (Sherwood Medical)
- Tvinga suspensionen genom filtret och kassera den konserveringsmedelsfyllda vätskan
- Kenalog kommer att fastna på sprutans sida av filtret
- Överför filtret till en 5 ml spruta fylld med balanserad saltlösning (BSS)
- Driv försiktigt BSS genom filtret för att ytterligare skölja ur konserveringsmedlet
- Upprepa sköljningen några gånger
- Placera en 22 gauge nål på den distala änden av filtret
- Teckna upp 2 ml BSS i sprutan genom filtret för att resuspensionera Kenalog
- Kenalog (nu utan konserveringsmedlet och spädd 10:1) kommer att färga glaskroppssträngar vita
- Oetting, TA, Cataract Surgery for Greenhorns, Finns på http://medrounds.org/cataract-surgery-greenhorns. Tillgänglig den 9 september 2007
- Dupps WJ Oetting TA, Diamond iris retractor configuration for small-pupil extracapsular or intracapsular cataract surgery. J Cataract Refract Surg Vol 30(12):2473-2475.
- Chang DF, Oetting TA, Kim T, Curbside Consultations in Anterior Segment Surgery, Slack Inc, Thorofare NJ, 2007.
- Henderson BA, Essentials of Cataract Surgery, Slack Inc, Thorofare NJ, 2007.
- Burk SE, Da Mata AP, Snyder ME, Schneider S, Osher RH, Cionni RJ. Visualisering av glaskroppen med hjälp av Kenalog-suspension J Cataract Refract Surg. 2003 Apr;29(4):645-51.