- Introduktion
- Material och metoder
- Deltagare
- Studieprocedurer, EEG-datainsamling och analys
- Resultat
- Deltagare
- Resting State EEG
- Fp1-kanalens effektspektrala tätheter (PSDs) jämförelse
- Fp1 Channel Resting EEG Test/Retest Comparison
- Diskussion
- Författarbidrag
- Finansiering
- Intressekonfliktförklaring
- Acknowledgments
Introduktion
Neurodegenerativa sjukdomar utgör ett enormt globalt medicinskt behov som inte kan tillgodoses och som kräver utveckling av nya sjukdomsförändrande terapier. Med tanke på dessa sjukdomars smygande karaktär och den höga kostnaden för många diagnostiska tester finns det ett stort behov av allmänt tillgängliga, tillförlitliga och billiga biomarkörer för att följa utvecklingen av neurodegenerativa processer inom tidsramar som lämpar sig för läkemedelsutveckling. I detta sammanhang kan EEG ha en anmärkningsvärd potential. Även om EEG är känsligt för kända livsstilsfaktorer och läkemedel har det många betydande fördelar. EEG återspeglar synaptisk aktivitet, som är en gemensam nämnare för den funktionella effekten av neurodegenerativa processer. EEG är en icke-invasiv, bärbar, säker och billig teknik som är allmänt accepterad och kräver relativt kort tid för att samla in data. Kvalitativ EEG används rutinmässigt i klinisk praxis för att diagnostisera epilepsi. På senare tid har en integrering av en kvantitativ EEG-biomarkör (qEEG) och en klinisk bedömning föreslagits för bedömning av ADHD (attention-deficit/hyperactivity disorder) och har beviljats av FDA (Food and Drug Administration) klass II-beteckning för att stödja den kliniska bedömningen av ADHD (Lenartowicz och Loo, 2014; Snyder et al., 2015). qEEG befinner sig i ett undersökningsstadium för att användas som en endpoint vid neurodegenerativa sjukdomar i kliniska prövningar. De senaste framstegen inom dataanalyser, tolkning och förbättrad rumslig upplösning har dock ökat potentialen för EEG som en tillförlitlig, exakt biomarkör för neurodegenerativ sjukdomsprogression. Många rapporterade observationsanalyser av qEEG i viloläge stöder dess potentiella värde som biomarkör för upptäckt av neurala signaturer av neurodegeneration vid Alzheimers sjukdom (Babiloni et al, 2011; Moretti et al., 2011; Berka et al., 2014; Chen et al., 2015; Garn et al., 2015; Ruffini et al., 2016; Waninger et al., 2016), Parkinsons sjukdom (Sarnthein och Jeanmonod, 2007; Babiloni et al., 2011; Soria-Frisch et al, 2014; Shani Waninger et al., 2015; Kroupi et al., 2017) och frontotemporal demens (Pijnenburg et al., 2008; Nishida et al., 2011; Caso et al., 2012; Goossens et al., 2016).
Under årens lopp har EEG-hårdvarutekniken också utvecklats och flera trådlösa flerkanaliga system har dykt upp som levererar högkvalitativa EEG-signaler och fysiologiska signaler i en enklare, mer bekväm och bekvämare utformning än de traditionella, besvärliga systemen. Traditionella EEG-system kräver lång tid för montering och applicering, vilket vanligtvis innebär att patientens hårbotten slits. Appliceringstiden och obehaget gör dessa traditionella system svåra att använda i befolkningsgrupper som lider av demens, där det ofta är svårt att samarbeta med långvariga kliniska förfaranden. Flera av de trådlösa system som för närvarande finns tillgängliga kan dock appliceras på 20 minuter eller mindre utan obehag under appliceringen och med en bekväm passform under mätningarna. I kombination med framsteg inom signaldetektion och kvantitativa analystekniker är trådlösa system idealiska kandidater för relativt snabb, tolerabel klinisk bedömning av potentiellt utmanande demenspopulationer, t.ex. beteendevariant frontotemporal demens, som kännetecknas av framträdande beteende- och personlighetsförändringar.
På senare tid har det också funnits en växande marknad för bärbar teknik för konsumenter, vilket har lett till system med begränsade kanaler som är tillgängliga för personligt bruk, t.ex. för meditations- och avslappningsträning. Det är tänkbart att dessa system, även om de har en begränsad täckning, också kan användas i utvalda kliniska studier. Tillämpningen av dessa konsumentsystem i klinisk forskning har dock inte undersökts i någon större utsträckning, och systemens noggrannhet och tillförlitlighet vid upprepade mätningar är inte väletablerad. Vidare är det inte klart om den begränsade kanalförvärvet kan ge tillräckliga data och anatomisk täckning för att bedöma de neurala signaturerna hos patienter som drabbats av neurodegenerativa sjukdomar.
Den aktuella studien var utformad för att ge en första utvärdering av potentialen hos konsument-EEG-system för kliniska prövningar, genom att jämföra användarvänlighet, noggrannhet och tillförlitlighet hos två trådlösa flerkanaliga EEG-system av medicinsk kvalitet, B-Alert X24 och Enobio 20, med två konsumentbaserade system med begränsade kanaler, Muse och Mindwave.
Material och metoder
Deltagare
Studiepopulationen omfattade fem friska deltagare som uppfyllde kraven för studien (tabell 1). Försökspersoner uteslöts om de, efter genomgång av deras sjukdomshistoria, samtidiga mediciner och livsstil (alkohol- och koffeinförbrukning samt rökstatus), inte ansågs vara friska. Mer specifikt uteslöts de från studien om de hade en historia av epilepsi eller andra sömn-, neurologiska eller psykiatriska störningar eller tog mediciner eller hade en livsstil som var känd för att påverka EEG-signalen, t.ex. rökning och betydande alkohol- och koffeinintag.

Tabell 1. Studiepopulationens demografi och grundläggande egenskaper.
Ett skriftligt informerat samtycke inhämtades från alla studiedeltagare i enlighet med de riktlinjer för experimentella undersökningar med människor som krävs av Chesapeake Institutional Review Board.
Studieprocedurer, EEG-datainsamling och analys
För att undvika potentiell EEG-signalvariabilitet i samband med näringsintag och cirkadiska variationer skedde alla besök på morgonen efter en standardfrukost med lågt kolhydratinnehåll och högt proteininnehåll (för att minimera sömnighet efter födseln) på studieplatsen för Advanced Brain Monitoring (ABM) research labs. Dessutom ombads deltagarna att undvika alkoholhaltiga drycker kvällen före studiebesöket samt att fasta och undvika koffein på morgonen för besöket.
EEG-data förvärvades under två separata besök med ~1 veckas mellanrum från två medicinska EEG-system med flera kanaler (20 kanaler), B-Alert (Advanced Brain Monitoring, ABM) och Enobio (Neuroelectrics) (figur 1, tabell 2) och två konsumentsystem med begränsade kanaler, Muse (Interaxon, 2 kanaler) och Mindwave (Neurosky, en kanal) (figur 1, tabell 2) i följande ordning: Muse, Mindwave, B-Alert, Enobio. B-Alert X24 EEG-system och Enobio är båda CE-medicinskt certifierade trådlösa 20-kanaliga system som används i den internationella standardmonteringen 10-20 och samlar in EEG-signaler med en samplingsfrekvens på 256 Hz. Dessutom har B-Alert godkänts av FDA för användning som medicinsk utrustning.
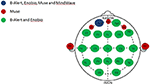
Figur 1. Anatomisk kanalfördelning för EEG-system med flera och begränsade kanaler. Representation av de delade och unika kanalerna bland de fyra utvärderade EEG-systemen. Den gemensamma kanalen för alla fyra EEG-system, Fp1 (blå); kanaler som är unika för Muse-systemet (röd); kanaler som delas mellan flerkanalssystemen, B-Alert och Enobio (grön).

Tabell 2. Jämförelser av EEG-system.
B-Alert använder mastoiderna som referenskanal. Enobio kan användas med en mastoidreferens, öronklämma eller med hjälp av andra platser i hårbotten. Mindwave har också en referens på öronklämman och Muse har tre referenskanaler på pannan. Alla system innehöll kontroll av signalkvalitet, men till skillnad från de medicinska EEG-systemen har båda konsumentsystemen torra elektroder och ingen impedanskontroll.
Dessa tekniker valdes ut på grundval av deras förmåga att förse slutanvändare med råa EEG-utdata genom praktisk och icke kostnadsdrivande tillgång.
Tio minuters EEG i viloläge förvärvades under ögon öppna (EO) med visuell fixering på en krysssymbol som presenterades på en datorskärm (5 min) samt medan ögonen var stängda (EC) i 5 min.
Med tanke på att alla fyra system endast delar FP1-kanalen (figur 1) utfördes EEG-mönster (råa och dekontaminerade), spektrala effekttätheter (PSD) och jämförelser av test/retest-tillförlitlighet mellan de fyra EEG-system som utvärderades i studien med fokus på Fp1-elektroden i både EO- och EC-tillstånd.
EEG-data från varje system laddades in i MATLAB (Mathworks) med hjälp av specialbyggda funktioner. De EEG-data som registrerades under pauser och instruktioner kasserades före analysen. EEG:s effektspektraltäthet för varje 1 s epok beräknades med hjälp av Welchs modifierade periodogrammetod med ett Hamming-fönster med en avsmalning av 1 s längd. PSD:er beräknades på EEG i vila under både öppna och stängda ögon. För att möjliggöra lika enheter (μV) tillämpades en korrektionsfaktor på 1,25 (Muse), 0,25 (MindWave) eller 1 000 (Enobio 20). Alla PSD-data från Fp1-kanalen medelvärdesbildades för de fem försökspersonerna för varje besök. Test-retest utfördes genom att beräkna och plotta Vist1/Visit2.
Resultat
Deltagare
Deltagarna var alla friska frivilliga med en genomsnittsålder på 27 år, de var alla högerhänta och icke-rökare och övervägande män (60 %). Deras demografi och grundläggande egenskaper sammanfattas i tabell 1.
Resting State EEG
EEG-data samlades framgångsrikt in från alla fyra testade system. På grund av de torra elektroderna och det begränsade antalet kanaler var inställningstiden som väntat betydligt kortare för konsument-EEG-systemen. Det fanns dock ingen observerad skillnad i försökspersonernas tolerans och acceptans mellan de fyra systemen.
Mönster av EEG-rådata under EO- (figur 2) och EC- (figur 3) förhållanden samlades in och utvärderades från varje system. Muse och Mindwave var mer benägna till artefakt på grund av ögonblinkningar och muskelrörelser i frontalregionen vid ögonöppning (figur 2).
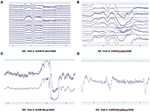
Figur 2. Utdrag av EO-rådata från B-Alert (A) och Enobio (B) Muse (C) och MindWave (D) inom samma deltagare under samma besök.
Figur 3. Utdrag av EC-rådata från B-Alert (A) och Enobio (B) Muse (C) och MindWave (D) inom samma deltagare under samma besök.
Fp1-kanalens effektspektrala tätheter (PSDs) jämförelse
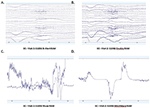
Genomsnittliga PSDs i Fp1-kanalen, som är gemensamma för de fyra EEG-systemen, för besök 1 och besök 2 beräknades och plottades för både EO- (figurerna 4A, B) och EC- (figurerna 4C, D) förhållanden. I EO-tillståndet var B-alert- och Enobio-spektra ungefär lika, medan Mindwave var något högre men följde en liknande kurva. En bredbandig ökning av effekten observerades för PSD:er som förvärvades med Muse-systemet. På samma sätt var B-alert, Enobio och Mindwave PSD:erna i EC-tillståndet (figurerna 4C och 4D) likartade, men en ökad bredbandseffekt observerades för Muse-spektra, som också verkade ha högre variation än de andra systemen. Toppar vid 8-12 Hz (alfabandet) var synliga i de spektrum som förvärvades med B-Alert-, Enobio- och Mindwave-systemen vid varje besök. Medan det fanns en tydlig alfa-topp för Muse power-spektra vid besök 2, observerades ingen topp i spektrumen från besök 1.
Figur 4. Fp1 Power Spectral Densities (PSD) från alla fyra EEG-system i EO-tillståndet vid besök 1 (A) och besök 2 (B) och EC-tillståndet vid besök 1 (C) och besök 2 (D).
Fp1 Channel Resting EEG Test/Retest Comparison
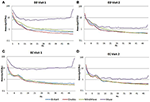
I EC-tillståndet låg Power Spectral Ratio mellan 0,975 och 1,025 för B-Alert, Enobio och Mindwave (figur 5A). Muse-systemets PSD-förhållanden hade större variation än de andra tre systemen med förhållanden mellan 1,125 och 1,225. I EO-tillståndet verkade det finnas något större variation för Enobio i de långsamma vågorna Delta (1-3 Hz), Theta (3-7 Hz) och långsam alfa (8-10) och för B-Alert och Mindwave i de snabbare vågorna Beta (13-30 Hz) och Gamma (25-40 Hz). Förhållandena låg dock fortfarande mellan 0,975 och 1,05. I likhet med EC-tillståndet hade testet/retestet för Muse högre variation, med kvoter upp till 1,2 (figur 5B).
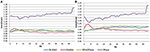
Figur 5. Test-retestförhållande för EC (A) och EO (B) tillstånd.
Diskussion
Denna studie jämförde kvantitativ EEG-signal och test-retesttillförlitlighet för medicinska och konsument-EEG-system för att utvärdera deras potentiella tillämpning i klinisk forskning och kliniska prövningar. Nyligen populära konsument-EEG-system utvärderades på grund av deras låga kostnad, breda tillgänglighet och potential för hemmabaserade studier i utmanande populationer. Bland de populära tillämpningarna av EEG-system för konsumentbruk finns meditation och avslappningsträning samt hantering av ångest och smärta. I nyligen genomförda undersökningar har man undersökt deras användbarhet utöver spelande: NeuroSky har visat sig kunna upptäcka början av sömnstadium 1 (Van Hal et al., 2014) och det har också funnits intresse för att bedöma konsument-EEG inom hjärnans datorgränssnitt (Bialas och Milanowski, 2014; Kim et al., 2015; Taherian et al., 2017). Tillämpningen av enklare EEG-system (t.ex. 6 kanaler) undersöks också för nödsituationer (Jakab et al., 2014). En tidigare utvärdering, även om den använde ett mer komplext headset, visade att kommersiellt tillgängliga konsument-EEG-system med flera ledningar, t.ex. Emotiv EPOC 16-elektrodkapseln, också kan ha ett värde vid utvärdering av kliniska förhållanden (Schiff et al., 2016).
Denna studie gav bevis för att EEG-data av ganska god kvalitet kan samlas in framgångsrikt från konsument-EEG. Det fanns dock skillnader i effektökning, testgenomgång och form av den alfa-topp som observerades vid 8-13 Hz. Mindwave visade överlag liknande Fp1-effektspektra som de medicinska systemen med en liten bredbandig ökning jämfört med B-Alert och Enobio. Muse visade en bredbandig ökning av effektspektra, vilket kan återspegla artefakt i de data som förvärvats av en torr elektrod.
Consumer EEG-system visade en betydligt bekvämare och snabbare uppsättning,vilket är optimalt för deras avsedda användning i underhållnings- och självhjälpstillämpningar. Deras datakvalitet påverkades dock överlag negativt av artefaktkänsligheten i samband med den torra elektroden. Som väntat försämrades datakvaliteten särskilt under EO. Bristen på impedanstestningskapacitet och tillämpningen på frontalregionen, som är särskilt känslig för ögonblinkningar och muskelrörelser vid ögonöppning, bidrog sannolikt också till denna relativa artefakt. Dessutom är den bedömning som utförs av konsument-EEG-system till sin natur begränsad och begränsad till den enda anatomiska hjärnregionen som täcks av de få kanalerna, vilket utesluter utvärderingar av flera nätverk.
Torra elektroder kan också vara mer benägna att leda till obehag med tiden och utgöra en högre risk för felplacering på pannan, vilket leder till felaktig signalinsamling och test/retest. Jämfört med utrustning av medicinsk kvalitet var tillförlitligheten för test/retest lägre i EEG-system för konsumenter. Tillförlitligheten mättes med en test/retest-värdering för alla system (figur 5). B-Alert, Enobio och Mindwave presterade relativt bra, medan Muse hade relativt låg tillförlitlighet. Vidare, även om en tydlig alfa-topp påvisades för Muse vid besök 2 (figur 4), tyder avsaknaden av en alfa-topp vid besök 1 på en bristande konsistens som kan bero på artefakt. Konsistenta och tillförlitliga mätningar av hjärnaktivitet är avgörande i kliniska prövningar när man övervakar sjukdomsutvecklingen och utvärderar effekten av ett experimentellt terapeutiskt preparat. Även om konsumentsystemen kan vara användbara för en snabb bedömning när tiden är begränsad, kan dessa begränsningar av konsument-EEG hindra deras tillämpningar i forsknings- och kliniska prövningsmiljöer, och ett system av medicinsk kvalitet med hög test-retest-tillförlitlighet rekommenderas för användning som en farmakodynamisk endpoint i kliniska bedömningar.
Sluttningsvis belyste jämförelsen mellan medicinska och konsument-EEG-system under experimentella förhållanden differentiering i prestanda och, särskilt, specifika begränsningar i användningen som skulle kunna hindra tillämpningar av konsumentsystem i forsknings- och kliniska prövningsmiljöer. Å andra sidan är de medicinska systemen med flera ledningar mindre idealiska för underhållningsändamål som kräver snabb inställning och databehandling från ett minimalt antal elektroder. Den största begränsningen i den här studien beror på den lilla studiepopulationen och avsaknaden av randomisering av ordningen på de system som användes för insamling. Data förvärvades i samma ordning av systemen för att undvika effekter av tidpunkten för förvärvet som kan påverka EEG på grund av cirkadiska rytmer. EEG-effektmätningar har dock visat sig vara mycket tillförlitliga och upprepningsbara för individer när man använder standard-EEG-system. Av denna anledning ansågs den valda provstorleken informativ.
Slutsatsen är att EEG-data framgångsrikt kan samlas in från alla fyra testade system, inklusive konsument-EEG-system, med varierande begränsningar i fråga om användbarhet, datakvalitet och tillförlitlighet som styr deras optimala tillämpningar, inklusive i kliniska prövningar. Mottaglighet för artefakter och variabilitet i test/retest-tillförlitlighet som är förknippade med nuvarande konsument-EEG-system föreslår användning av EEG-system av medicinsk kvalitet för robusta kliniska tvärsnitts- och longitudinella EEG-datainsamlingar.
Författarbidrag
ER och AV: deltog i utformningen och designen av projektet, analysen och tolkningen av data samt i utarbetandet av manuskriptet. SW, CB och GR: deltog i utformningen och designen av projektet, dess genomförande, analys och tolkning av data samt utarbetande av manuskript. Alla författare har deltagit i utarbetandet, skrivandet och revideringen av manuskriptet och alla har läst och godkänt den slutliga versionen av manuskriptet.
Finansiering
Denna studie stöddes av Biogen.
Intressekonfliktförklaring
ER och AV: Anställda på Biogen. SW och CB: Anställda vid Advanced Brain Monitoring, Inc. GR: Anställd på Neuroelectrics.
Acknowledgments
Vi vill tacka studiedeltagarna för deras tid och bidrag till den här studien. Biogen-teamet deltog i studiens utformning, analys och tolkning av data, i skrivandet av rapporten och i beslutet att skicka in artikeln för publicering.
Babiloni, C., De Pandis, M. F., Vecchio, F., Buffo, P., Sorpresi, F., Frisoni, G. B., et al. (2011). Kortikala källor till elektroencefalografiska rytmer i vila vid Parkinsonrelaterad demens och Alzheimers sjukdom. Clin. Neurophysiol. 122, 2355-2364. doi: 10.1016/j.clinph.2011.03.029
PubMed Abstract | CrossRef Full Text | Google Scholar
Berka, C., Verma, A., Korszen, S., and Johnson, R. (2014). ”Development of EEG biomarkers for Alzheimer’s disease”, i GTC Biomarkers Summit (San Diego, CA).
Bialas, P., and Milanowski, P. (2014). Ett högfrekvent steady-state visuellt framkallad potentialbaserat hjärndatorgränssnitt med hjälp av EEG-headset av konsumentklass. Conf. Proc. IEEE Eng. Med. Biol. Soc. 2014, 5442-5445. doi: 10.1109/EMBC.2014.6944857
PubMed Abstract | CrossRef Full Text | Google Scholar
Caso, F., Cursi, M., Magnani, G., Fanelli, G., Falautano, M., Comi, G., et al. (2012). Kvantitativt EEG och LORETA: värdefulla verktyg för att skilja FTD från AD? Neurobiol. Aging 33, 2343-2356. doi: 10.1016/j.neurobiolaging.2011.12.011
PubMed Abstract | CrossRef Full Text | Google Scholar
Chen, C. C., Hsu, C. Y., Chiu, H. W., Hu, C. J. och ChiehLee, T. (2015). Frekvenskraft och koherens av elektroencefalografi är korrelerade med svårighetsgraden av Alzheimers sjukdom: en multicenteranalys i Taiwan. J. Formos Med. Assoc. 114, 729-735. doi: 10.1016/j.jfma.2013.07.008
PubMed Abstract | CrossRef Full Text | Google Scholar
Garn, H., Waser, M., Deistler, M., Benke, T., Dal-Bianco, P., Ransmayr, G., et al. (2015). Kvantitativa EEG-markörer relaterar till Alzheimers sjukdomens svårighetsgrad i det prospektiva demensregistret Österrike (PRODEM). Clin. Neurophysiol. 126, 505-513. doi: 10.1016/j.clinph.2014.07.005
PubMed Abstract | CrossRef Full Text | Google Scholar
Goossens, J., Laton, J., Van Schependom, J., Gielen, J., Struyfs, H., Van Mossevelde, S., et al. (2016). EEG dominant frekvenstopp skiljer mellan Alzheimers sjukdom och frontotemporal lobär degeneration. J. Alzheimers Dis. 55, 53-58. doi: 10.3233/JAD-160188
PubMed Abstract | CrossRef Full Text | Google Scholar
Jakab, A., Kulkas, A., Salpavaara, T., Kauppinen, P., Verho, J., Heikkilä, H., et al. (2014). Nytt trådlöst elektroencefalografisystem med minimal förberedelsetid för användning i nödsituationer och prehospital vård. Biomed. Eng. Online 13:60. doi: 10.1186/1475-925X-13-60
CrossRef Full Text | Google Scholar
Kim, M., Kim, B. H. och Jo, S. (2015). Kvantitativ utvärdering av ett billigt icke-invasivt hybridgränssnitt baserat på EEG och ögonrörelser. IEEE Trans. Neural. Syst. Rehabil. Eng. 23, 159-168. doi: 10.1109/TNSRE.2014.2365834
PubMed Abstract | CrossRef Full Text | Google Scholar
Kroupi, E., Castellano, M., Ibanez, D., Montplaisir, J., Gagnon, J. F., Postuma, R., et al. (2017). ”Deep networks using auto-encoders for PD prodromal analysis,” in Proceedings of 1st HBP Student Conference (Vienna).
Lenartowicz, A., and Loo, S. K. (2014). Användning av EEG för att diagnostisera ADHD. Curr. Psychiatry Rep. 16:498. doi: 10.1007/s11920-014-0498-0
CrossRef Full Text | Google Scholar
Moretti, D. V., Frisoni, G. B., Binetti, G. och Zanetti, O. (2011). Anatomiskt substrat och EEG-markörer i hårbotten är korrelerade hos personer med kognitiv nedsättning och Alzheimers sjukdom. Front Psychiatry 1:152. doi: 10.3389/fpsyt.2010.00152
PubMed Abstract | CrossRef Full Text | Google Scholar
Nishida, K., Yoshimura, M., Isotani, T., Yoshida, T., Kitaura, Y., Saito, A., et al. (2011). Skillnader i kvantitativt EEG mellan frontotemporal demens och Alzheimers sjukdom enligt LORET. Clin. Neurophysiol. A 122, 1718-1725. doi: 10.1016/j.clinph.2011.02.011
PubMed Abstract | CrossRef Full Text | Google Scholar
Pijnenburg, Y. A., Strijers, R. L., Made, Y. V., van der Flier, W. M., Scheltens, P. och Stam, C. J. (2008). Undersökning av funktionell konnektivitet i vila EEG vid frontotemporal lobardegeneration. Clin. Neurophysiol. 119, 1732-1738. doi: 10.1016/j.clinph.2008.02.024
PubMed Abstract | CrossRef Full Text | Google Scholar
Ruffini, G., David, I.-S., Castellano, M. och Soria-Frisch, A. (2016). ”EEG-driven RNN-klassificering för prognos av neurodegeneration hos riskpatienter”, i Internet Corporation for Assigned Names and Numbers (ICANN) (Copenhargen).
Google Scholar
Sarnthein, J. och Jeanmonod, D. (2007). Hög thalamokortikal theta-koherens hos patienter med Parkinsons sjukdom. J. Neurosci. 27, 124-131. doi: 10.1523/JNEUROSCI.2411-06.2007
PubMed Abstract | CrossRef Full Text | Google Scholar
Schiff, S., Casa, M., Di Caro, V., Aprile, D., Spinelli, G., De Rui, M., et al. (2016). Ett billigt, användarvänligt elektroencefalografiskt inspelningssystem för bedömning av hepatisk encefalopati. Hepatology 63, 1651-1659. doi: 10.1002/hep.28477
PubMed Abstract | CrossRef Full Text | Google Scholar
Shani Waninger, S. K., Berka, C., Tan, V. och Johnson, R. (2015). ”A novel portable neurocognitive biomarker assessment for Parkinson’s Disease”, i GTC Biomarkers Summit (San Diego, CA).
Snyder, S. M., Rugino, T. A., Hornig, M. och Stein, M. A. (2015). Integrering av en EEG-biomarkör med en klinikers ADHD-utvärdering. Brain Behav. 5:e00330. doi: 10.1002/brb3.330
PubMed Abstract | CrossRef Full Text | Google Scholar
Soria-Frisch, J. M., Ibanez, D., Dunne, S., Grau, C., Ruffini, G., Rodrigues-Brazete, J., et al. (2014). ”Machine Learning for a Parkinsons prognosis and diagnosis system based on EEG,” in Proceedings International Pharmaco-EEG Society Meeting IPEG (Leipzig).
Taherian, S., Selitskiy, D., Pau, J., and Claire Davies, T. (2017). Är vi där än? Utvärdering av kommersiella hjärn-datorgränssnitt för kontroll av datorprogram av personer med cerebral pares. Disabil. Rehabil. Assist. Technol. 12, 165-174. doi: 10.3109/17483107.2015.1111943
PubMed Abstract | CrossRef Full Text | Google Scholar
Van Hal, B., Rhodes, S., Dunne, B. och Bossemeyer, R. (2014). Billig EEG-baserad sömndetektering. Conf. Proc. IEEE Eng. Med. Biol. Soc. 2014, 4571-4574. doi: 10.1109/EMBC.2014.6944641
PubMed Abstract | CrossRef Full Text | Google Scholar
Waninger, S., Stikic, M., Tatinada, R. och Verma, A. (2016). ”Identification of neurophysiological biomarkers of MCI using resting state, EEG,” in Alzheimer’s Association International Conference (Toronto, ON).
Google Scholar
.