![]()
Apa are efecte importante asupra tuturor sistemelor biologice. Ceea ce face ca apa să fie atât de unică sunt două proprietăți foarte importante.
Apa este o moleculă polară
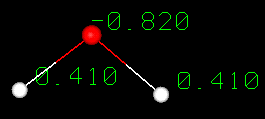 O moleculă de apă se formează atunci când doi atomi de hidrogen se leagă covalent cu un atom de oxigen. Într-o legătură covalentă electronii sunt împărțiți între atomi. În apă împărțirea nu este egală. Atomul de oxigen atrage electronii mai puternic decât cel de hidrogen, ceea ce conferă apei o distribuție asimetrică a sarcinilor. Moleculele care au capete cu sarcini parțial negative și pozitive sunt cunoscute ca molecule polare. Această proprietate polară este cea care permite apei să separe moleculele de solut polar și explică de ce apa poate dizolva atât de multe substanțe.
O moleculă de apă se formează atunci când doi atomi de hidrogen se leagă covalent cu un atom de oxigen. Într-o legătură covalentă electronii sunt împărțiți între atomi. În apă împărțirea nu este egală. Atomul de oxigen atrage electronii mai puternic decât cel de hidrogen, ceea ce conferă apei o distribuție asimetrică a sarcinilor. Moleculele care au capete cu sarcini parțial negative și pozitive sunt cunoscute ca molecule polare. Această proprietate polară este cea care permite apei să separe moleculele de solut polar și explică de ce apa poate dizolva atât de multe substanțe.
Apa este foarte coerentă .
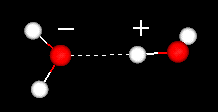 Regiunile pozitive dintr-o apă vor atrage regiunile cu sarcină negativă din alte ape. Punctele arată legătura de hidrogen. Într-o legătură de hidrogen, un atom de hidrogen este împărțit de alți doi atomi. Donatorul este atomul de care hidrogenul este mai strâns legat. Acceptorul (care are o sarcină parțial negativă) este atomul care atrage atomul de hidrogen. Faceți clic aici sau pe imaginea din stânga pentru a vedea un film cu două molecule de apă.
Regiunile pozitive dintr-o apă vor atrage regiunile cu sarcină negativă din alte ape. Punctele arată legătura de hidrogen. Într-o legătură de hidrogen, un atom de hidrogen este împărțit de alți doi atomi. Donatorul este atomul de care hidrogenul este mai strâns legat. Acceptorul (care are o sarcină parțial negativă) este atomul care atrage atomul de hidrogen. Faceți clic aici sau pe imaginea din stânga pentru a vedea un film cu două molecule de apă.
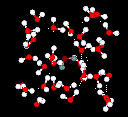 Legăturile de hidrogen sunt mult mai slabe decât legăturile covalente. Cu toate acestea, atunci când un număr mare de legături de hidrogen acționează la unison, ele vor avea un efect contributiv puternic. Acesta este cazul în cazul apei.
Legăturile de hidrogen sunt mult mai slabe decât legăturile covalente. Cu toate acestea, atunci când un număr mare de legături de hidrogen acționează la unison, ele vor avea un efect contributiv puternic. Acesta este cazul în cazul apei.
Vezi: legături de hidrogen în apă și gheață — Water and Ice hydrogen bonds using Jsmol
Apa lichidă are o structură parțial ordonată în care legăturile de hidrogen se formează și se desfac în mod constant.
Vezi un film flash cu moleculele de apă în acțiune.
Pe de altă parte, gheața are o structură de rețea rigidă.
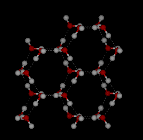
În apa lichidă, fiecare moleculă este legată de hidrogen cu aproximativ 3,4 alte molecule de apă. În gheață fiecare fiecare moleculă este legată de hidrogen cu alte 4 molecule.
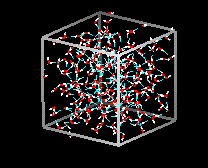
Comparați cele două structuri de mai jos. Observați spațiile goale din structura gheții.
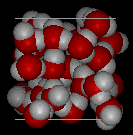
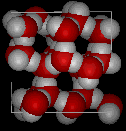
În gheața Ih, fiecare apă formează patru legături de hidrogen cu distanțe O—O de 2,76 Angstromi față de cel mai apropiat vecin de oxigen. Unghiurile O-O-O-O sunt de 109 grade, tipice unei structuri reticulare coordonate tetraedral. Densitatea gheții Ih este de 0,931 gm/cubic cm. Aceasta se compară cu o densitate de 1,00 gm/cubic cm. pentru apă.
Există unsprezece forme diferite de gheață cristalină care sunt cunoscute. Forma de hexaganol cunoscută sub numele de gheață Ih este singura care se găsește în mod natural. Structura reticulară a gheții 1h este prezentată aici.
 Imagine
Imagine
.