- Introducere
- Materiale și metode
- Participanți
- Proceduri de studiu, achiziția și analiza datelor EEG
- Rezultate
- Participanți
- Resting State EEG
- Comparare a densităților spectrale de putere (PSD) ale canalului Fp1
- Comparare EEG în stare de repaus a canalului Fp1 Test/Retest
- Discuție
- Contribuții ale autorilor
- Finanțare
- Declarație privind conflictul de interese
- Recunoștințe
Introducere
Dezordinele neurodegenerative reprezintă nevoi medicale globale uriașe nesatisfăcute și necesită dezvoltarea de noi terapii de modificare a bolii. Având în vedere natura insidioasă a acestor afecțiuni și costul ridicat al multor teste de diagnosticare, există o nevoie semnificativă de biomarkeri disponibili pe scară largă, fiabili și necostisitori pentru a urmări evoluția proceselor neurodegenerative în intervale de timp adecvate pentru dezvoltarea de medicamente. În acest context, EEG ar putea avea un potențial remarcabil. Deși EEG este sensibil la factorii cunoscuți ai stilului de viață și la medicamente, are multe avantaje considerabile. EEG reflectă activitatea sinaptică, care este un numitor comun pentru impactul funcțional al proceselor neurodegenerative. EEG este o tehnologie neinvazivă, portabilă, sigură și ieftină, care este larg acceptată și necesită un timp de achiziție relativ scurt. EEG-ul calitativ este utilizat în mod obișnuit în practica clinică pentru diagnosticarea epilepsiei. Mai recent, o integrare a unui biomarker EEG cantitativ (qEEG) și evaluarea clinicianului au fost propuse pentru evaluarea tulburării de deficit de atenție/hiperactivitate (ADHD) și a primit din partea FDA (Food and Drug Administration) desemnarea de clasă II pentru a sprijini evaluarea clinică a ADHD (Lenartowicz și Loo, 2014; Snyder et al., 2015). qEEG se află în stadii de investigare pentru a fi utilizat ca punct final în bolile neurodegenerative în studiile clinice. Cu toate acestea, progresele recente în analizele de date, interpretarea și îmbunătățirea rezoluției spațiale au crescut potențialul EEG ca biomarker fiabil și precis pentru evoluția bolilor neurodegenerative. Multe analize observaționale raportate ale qEEG în stare de repaus susțin valoarea sa potențială ca biomarker pentru detectarea semnăturilor neuronale ale neurodegenerării care apar în boala Alzheimer (Babiloni et al., 2011; Moretti și colab., 2011; Berka și colab., 2014; Chen și colab., 2015; Garn și colab., 2015; Ruffini și colab., 2016; Waninger și colab., 2016), boala Parkinson (Sarnthein și Jeanmonod, 2007; Babiloni și colab., 2011; Soria-Frisch și colab, 2014; Shani Waninger et al., 2015; Kroupi et al., 2017) și demența frontotemporală (Pijnenburg et al., 2008; Nishida et al., 2011; Caso et al., 2012; Goossens et al., 2016).
De-a lungul anilor, tehnologia hardware EEG a evoluat, de asemenea, și au apărut mai multe sisteme multicanal fără fir care furnizează semnale EEG și fiziologice de înaltă calitate într-un design mai simplu, mai convenabil și mai confortabil decât sistemele tradiționale, greoaie. Sistemele EEG tradiționale necesită timp îndelungat de asamblare și aplicare, implicând de obicei abraziunea scalpului pacientului. Timpul de aplicare și disconfortul fac ca aceste sisteme tradiționale să fie dificil de utilizat la populațiile afectate de demență, unde cooperarea cu procedurile clinice îndelungate este adesea dificilă. Cu toate acestea, mai multe sisteme fără fir disponibile în prezent pot fi aplicate în 20 de minute sau mai puțin, fără disconfort în timpul aplicării și cu o potrivire confortabilă în timpul achizițiilor. Combinate cu progresele înregistrate în tehnicile de detectare a semnalelor și de analiză cantitativă, sistemele fără fir sunt candidații ideali pentru evaluarea clinică relativ rapidă și tolerabilă a unor populații de demență potențial dificile, cum ar fi demența frontotemporală cu variantă comportamentală, caracterizată prin schimbări proeminente de comportament și de personalitate.
Mai recent, a existat, de asemenea, o piață în creștere pentru tehnologiile purtabile de consum care a condus la sisteme cu canale limitate disponibile pentru uz personal, cum ar fi meditația și antrenamentul pentru relaxare. Este de conceput că aceste sisteme, deși au o acoperire limitată, pot fi, de asemenea, utilizate în studii clinice selectate. Cu toate acestea, aplicarea acestor sisteme de consum în cercetarea studiilor clinice nu a fost explorată pe scară largă, iar acuratețea și fiabilitatea acestor sisteme pentru măsurători repetate nu au fost bine stabilite. În plus, nu este clar dacă achiziția cu canale limitate poate oferi suficiente date și acoperire anatomică pentru a evalua semnăturile neuronale la pacienții afectați de boli neurodegenerative.
Studiul actual a fost conceput pentru a oferi o evaluare inițială a potențialului sistemelor EEG de consum pentru studiile clinice, prin compararea ușurinței de utilizare, a acurateței și a fiabilității a două sisteme EEG wireless multicanal de calitate medicală, B-Alert X24 și Enobio 20, cu două sisteme de consum cu canale limitate, Muse și Mindwave.
Materiale și metode
Participanți
Populația studiată a inclus cinci participanți sănătoși care au îndeplinit condițiile de eligibilitate pentru studiu (tabelul 1). Subiecții au fost excluși dacă, după examinarea istoricului medical, a medicamentelor concomitente și a stilului de viață (consumul de alcool și cofeină, precum și statutul de fumător), nu au fost considerați sănătoși. Mai exact, au fost excluși din studiu dacă aveau antecedente de epilepsie sau alte tulburări de somn, neurologice sau psihiatrice sau dacă luau medicamente sau aveau un stil de viață despre care se știe că afectează semnalul EEG, cum ar fi fumatul și un consum considerabil de alcool și cofeină.

Tabelul 1. Datele demografice ale populației de studiu și caracteristicile de bază.
Consimțământul informat scris a fost obținut de la toți participanții la studiu, în conformitate cu liniile directoare pentru investigații experimentale cu subiecți umani solicitate de Chesapeake Institutional Review Board.
Proceduri de studiu, achiziția și analiza datelor EEG
Pentru a evita potențiala variabilitate a semnalului EEG asociată cu aportul nutrițional și variațiile circadiene, toate vizitele au avut loc dimineața, după un mic dejun standard cu conținut scăzut de carbohidrați și bogat în proteine (pentru a minimiza somnolența post-prandială) la locul de studiu al laboratoarelor de cercetare Advanced Brain Monitoring (ABM). În plus, participanților li s-a cerut să evite băuturile alcoolice cu o seară înainte de vizita de studiu, precum și să țină post și să evite cofeina în dimineața vizitei.
Datele EEG au fost achiziționate în timpul a două vizite separate, la o distanță de ~1 săptămână, de la două sisteme EEG medicale multicanal (20 de canale), B-Alert (Advanced Brain Monitoring, ABM) și Enobio (Neuroelectrics) (Figura 1, Tabelul 2) și două sisteme de consum cu canale limitate, Muse (Interaxon, 2 canale) și Mindwave (Neurosky, un canal) (Figura 1, Tabelul 2) în următoarea ordine: Muse, Mindwave, B-Alert, Enobio. Sistemul EEG B-Alert X24 și Enobio sunt ambele sisteme fără fir cu 20 de canale, certificate medical CE, aplicate în montajul internațional standard 10-20 și achiziționează semnalul EEG la o rată de eșantionare de 256 Hz. În plus, B-Alert a fost autorizat de FDA pentru a fi utilizat ca dispozitiv medical.
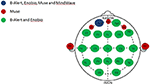
Figura 1. Distribuția canalelor anatomice ale sistemelor EEG cu mai multe canale și cu canale limitate. Figura 2. Reprezentarea canalelor partajate și unice între cele patru sisteme EEG evaluate. Canalul comun tuturor celor patru sisteme EEG, Fp1 (albastru); canalele unice pentru sistemul Muse (roșu); canalele partajate între sistemele cu mai multe canale, B-Alert și Enobio (verde).

Tabelul 2. Comparații între sistemele EEG.
B-Alert utilizează mastoidele ca și canal de referință. Enobio poate fi utilizat cu o referință mastoidiană, cu o clemă de ureche sau folosind alte locații ale scalpului. Mindwave are, de asemenea, o referință pe buza urechii, iar Muse are trei canale de referință pe frunte. Toate sistemele au inclus verificarea calității semnalului, însă, spre deosebire de sistemele EEG medicale, ambele sisteme de consum au electrozi uscați și nu au verificat impedanța.
Aceste tehnologii au fost selectate pe baza capacității lor de a oferi utilizatorilor finali ieșiri EEG brute prin acces practic și fără costuri prohibitive.
Au fost achiziționate zece minute de EEG în stare de repaus în timpul ochilor deschiși (EO) cu fixare vizuală pe un simbol încrucișat prezentat pe ecranul unui computer (5 min), precum și în timp ce ochii erau închiși (EC) timp de 5 min.
Din moment ce toate cele patru sisteme au în comun doar canalul FP1 (Figura 1), modelele EEG (brute și decontaminate), densitățile spectrale de putere (PSD) și comparațiile de fiabilitate test/retest între cele patru sisteme EEG evaluate în cadrul studiului au fost efectuate concentrându-se pe electrodul Fp1 atât în condițiile EO, cât și în condițiile EC.
Datele EEG de la fiecare sistem au fost încărcate în MATLAB (Mathworks) folosind funcții construite la comandă. Datele EEG înregistrate în timpul pauzelor și instrucțiunilor au fost eliminate înainte de analiză. Densitatea spectrală de putere a EEG pentru fiecare epocă de 1 s a fost calculată folosind metoda periogramei modificate a lui Welch cu o fereastră Hamming conică de 1 s lungime. PSD au fost calculate pe EEG în repaus, atât în timpul perioadelor cu ochii deschiși, cât și în timpul perioadelor cu ochii închiși. Pentru a permite unități egale (μV), s-a aplicat un factor de corecție de 1,25 (Muse), 0,25 (MindWave) sau 1.000 (Enobio 20). Toate datele PSD ale canalului Fp1 au fost mediate pentru cei cinci subiecți pentru fiecare vizită. Testul-retest a fost efectuat prin calcularea și reprezentarea grafică a Vist1/Visită2.
Rezultate
Participanți
Participanții au fost toți voluntari sănătoși cu o vârstă medie de 27 de ani, au fost toți dreptaci și nefumători, și predominant bărbați (60%). Datele lor demografice și caracteristicile de bază sunt rezumate în tabelul 1.
Resting State EEG
Datele EEG au fost colectate cu succes de la toate cele patru sisteme testate. Așa cum era de așteptat, din cauza electrozilor uscați și a numărului limitat de canale, timpul de configurare a fost considerabil mai mic pentru sistemele EEG de consum. Cu toate acestea, nu s-a observat nicio diferență în ceea ce privește toleranța și acceptarea subiecților între cele patru sisteme.
S-au colectat și evaluat de la fiecare sistem modele de date EEG brute în condițiile EO (Figura 2) și EC (Figura 3). Muse și Mindwave au fost mai predispuse la artefacte datorate clipirii ochilor și mișcării musculare în regiunea frontală cu deschiderea ochilor (figura 2).
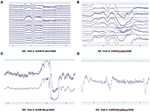
Figura 2. Extrase de date brute EO de la B-Alert (A) și Enobio (B) Muse (C) și MindWave (D) în cadrul aceluiași participant în timpul aceleiași vizite.
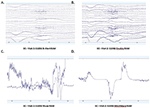
Figura 3. Extracte de date brute EC de la B-Alert (A) și Enobio (B) Muse (C) și MindWave (D) în cadrul aceluiași participant în timpul aceleiași vizite.
Comparare a densităților spectrale de putere (PSD) ale canalului Fp1
S-au calculat PSD-urile medii în canalul Fp1 comune tuturor celor patru sisteme EEG pentru vizita 1 și vizita 2 și au fost reprezentate grafic pentru ambele condiții EO (figurile 4A,B) și EC (figurile 4C,D). În condiția EO, spectrele B-alert și Enobio au fost aproximativ egale, în timp ce Mindwave a fost ușor crescut, dar a urmat o curbă similară. O creștere în bandă largă a puterii a fost observată pentru PSD-urile achiziționate cu sistemul Muse. În mod similar, în condiția EC (figurile 4C,D), PSD-urile B-alert, Enobio și Mindwave au fost similare, însă s-a observat o creștere a puterii în bandă largă pentru spectrele Muse, care, de asemenea, au părut să aibă o variație mai mare decât celelalte sisteme. Vârfurile de la 8-12 Hz (banda alfa) au fost vizibile în spectrele achiziționate cu sistemele B-Alert, Enobio și Mindwave la fiecare vizită. În timp ce a existat un vârf alfa clar pentru spectrele de putere Muse la vizita 2, nu a fost observat niciun vârf în spectrele de la vizita 1.
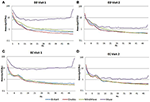
Figura 4. Densitățile spectrale de putere (PSD) Fp1 de la toate cele patru sisteme EEG în condiția EO la Vizita 1 (A) și Vizita 2 (B) și în condiția EC la Vizita 1 (C) și Vizita 2 (D).
Comparare EEG în stare de repaus a canalului Fp1 Test/Retest
În condiția EC, raportul spectral de putere a fost între 0,975 și 1,025 pentru B-Alert, Enobio și Mindwave (Figura 5A). Rapoartele PSD ale sistemului Muse au avut o variație mai mare decât celelalte trei sisteme, cu rapoarte cuprinse între 1,125 și 1,225. În condiția EO, a părut să existe o variație ușor mai mare pentru Enobio în undele lente Delta (1-3 Hz), Theta (3-7 Hz) și alfa lent (8-10), iar pentru B-Alert și Mindwave în undele mai rapide Beta (13-30 Hz) și Gamma (25-40 Hz). Cu toate acestea, ratele erau încă între 0,975 și 1,05. În mod similar cu condiția EC, testul/retestul pentru Muse a avut o variație mai mare, cu rapoarte de până la 1,2 (Figura 5B).
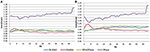
Figura 5. Rapoartele test-retest pentru condiția EC (A) și EO (B).
Discuție
Acest studiu a comparat semnalul EEG cantitativ și fiabilitatea test-retest a sistemelor EEG medicale și de consum pentru a evalua potențialul lor de aplicare în cercetarea clinică și în studiile clinice. Sistemele EEG de consum recent popularizate au fost evaluate datorită costului lor scăzut, accesibilității largi și potențialului pentru studii la domiciliu în populații dificile. Printre aplicațiile populare ale sistemelor EEG de consum se numără meditația și antrenamentul pentru meditație și relaxare, precum și pentru a face față anxietății sau durerii. Cercetări recente au explorat utilitatea acestora dincolo de jocuri: NeuroSky s-a dovedit a fi capabil să detecteze debutul stadiului 1 al somnului (Van Hal et al., 2014) și a existat, de asemenea, un interes pentru evaluarea EEG de consum în cadrul interfețelor creier-calculator (Bialas și Milanowski, 2014; Kim et al., 2015; Taherian et al., 2017). Aplicarea unor sisteme EEG mai simple (cu 6 canale, de exemplu) este, de asemenea, explorată pentru mediile de urgență (Jakab et al., 2014). O evaluare anterioară, deși a utilizat o cască mai complexă, a arătat că sistemele EEG de consum cu mai multe canale disponibile în comerț, cum ar fi casca Emotiv EPOC cu 16 electrozi, pot avea, de asemenea, valoare în evaluarea condițiilor clinice (Schiff et al., 2016).
Acest studiu a furnizat dovezi că datele EEG de o calitate destul de bună pot fi colectate cu succes de la EEG-uri de consum. Cu toate acestea, au existat distincții în ceea ce privește creșterea puterii, reluarea testului și forma vârfului alfa observat la 8-13 Hz. Mindwave a prezentat în general spectre de putere Fp1 similare cu cele ale sistemelor medicale, cu o ușoară creștere în bandă largă față de B-Alert și Enobio. Muse a arătat o creștere în bandă largă a spectrelor de putere, care poate reflecta un artefact în datele dobândite de un electrod uscat.
Sistemele EEG de consum au arătat o configurare semnificativ mai convenabilă și mai rapidă,ceea ce este optim pentru utilizarea lor preconizată în aplicațiile de divertisment și de auto-ajutorare. Cu toate acestea, calitatea datelor lor a fost în general afectată în mod negativ de susceptibilitatea artefactelor asociată cu electrodul uscat. După cum era de așteptat, calitatea datelor a fost diminuată în special în timpul EO. Lipsa capacității de testare a impedanței și aplicarea în regiunea frontală, care este deosebit de predispusă la clipiri ale ochilor și la mișcări musculare cu deschiderea ochilor, au contribuit, de asemenea, probabil, la acest artefact relativ. În plus, evaluarea efectuată de sistemele EEG de consum este, prin natura lor, limitată și limitată la singura regiune anatomică a creierului acoperită de cele câteva canale, ceea ce exclude evaluările multi-rețele.
Electrozii uscați pot fi, de asemenea, mai predispuși să provoace disconfort în timp și prezintă un risc mai mare de poziționare greșită pe frunte, ceea ce duce la o achiziție inexactă a semnalului și la test/retest. Comparativ cu echipamentele de calitate medicală, fiabilitatea testării/retestării a fost mai scăzută în cazul sistemelor EEG de consum. Fiabilitatea a fost măsurată cu o achiziție test-retest pentru toate sistemele (figura 5). În timp ce B-Alert, Enobio și Mindwave s-au comportat rezonabil de bine, Muse a avut o fiabilitate relativ scăzută. Mai mult, în timp ce un vârf alfa clar a fost demonstrat pentru Muse la vizita 2 (figura 4), absența unui vârf alfa la vizita 1 sugerează o lipsă de consistență care se poate datora unui artefact. Măsurătorile coerente și fiabile ale activității cerebrale sunt cruciale în studiile clinice atunci când se monitorizează evoluția bolii și se evaluează eficacitatea unui tratament experimental. În timp ce sistemele de consum ar putea fi utile pentru o evaluare rapidă atunci când timpul este limitat, aceste limitări ale EEG de consum ar putea împiedica aplicațiile acestora în cadrul cercetărilor și al studiilor clinice și se recomandă un sistem de calitate medicală cu o fiabilitate ridicată a testului-retest pentru utilizarea ca punct final farmacodinamic în evaluările clinice.
În cele din urmă, comparația sistemelor EEG medicale și de consum în condiții experimentale a evidențiat diferențierea performanțelor și, în special, limitările specifice de utilizare care ar putea împiedica aplicațiile sistemelor de consum în cadrul cercetărilor și al studiilor clinice. Pe de altă parte, sistemele medicale cu mai multe derivații sunt mai puțin ideale pentru scopuri de divertisment care necesită o configurare și o prelucrare rapidă a datelor de la un număr minim de electrozi. Principala limitare a acestui studiu se bazează în dimensiunea mică a populației de studiu și lipsa de randomizare a ordinii sistemelor utilizate pentru achiziție. Datele au fost achiziționate în aceeași ordine a sistemelor pentru a evita efectele timpului de achiziție care pot avea un impact asupra EEG din cauza ritmurilor circadiene. Cu toate acestea, măsurătorile de putere EEG s-au dovedit a fi foarte fiabile și repetabile pentru indivizi atunci când se utilizează sisteme EEG standard. Din acest motiv, dimensiunea eșantionului selectat a fost considerată informativă.
În concluzie, datele EEG pot fi colectate cu succes de la toate cele patru sisteme testate, inclusiv de la sistemele EEG de consum, cu diferite limitări privind ușurința de utilizare, calitatea datelor și fiabilitatea care ghidează aplicațiile lor optime, inclusiv în cadrul studiilor clinice. Susceptibilitatea la artefacte și variabilitatea fiabilității testului/retestului asociate cu sistemele EEG de consum actuale sugerează utilizarea unui sistem EEG de calitate medicală pentru colectarea robustă a datelor EEG clinice transversale și longitudinale.
Contribuții ale autorilor
ER și AV: au participat la conceperea și proiectarea proiectului, la analiza și interpretarea datelor și la pregătirea manuscrisului. SW, CB și GR: au participat la conceperea și proiectarea proiectului, la executarea acestuia, la analiza și interpretarea datelor și la pregătirea manuscrisului. Toți autorii au fost implicați în redactarea, scrierea și revizuirea manuscrisului și toți au citit și aprobat versiunea finală a manuscrisului.
Finanțare
Acest studiu a fost susținut de Biogen.
Declarație privind conflictul de interese
ER și AV: angajat Biogen. SW și CB: angajat al Advanced Brain Monitoring, Inc. GR: angajat Neuroelectrics.
Recunoștințe
Am dori să mulțumim participanților la studiu pentru timpul și contribuțiile lor la acest studiu. Echipa Biogen a participat la proiectarea studiului, la analiza și interpretarea datelor, la redactarea raportului și la decizia de a trimite articolul spre publicare.
Babiloni, C., De Pandis, M. F., Vecchio, F., Vecchio, F., Buffo, P., Sorpresi, F., Frisoni, G. B., et al. (2011). Sursele corticale ale ritmurilor electroencefalografice în stare de repaus în demența legată de boala Parkinson și boala Alzheimer. Clin. Neurophysiol. 122, 2355-2364. doi: 10.1016/j.clinph.2011.03.029
PubMed Abstract | CrossRef Full Text | Google Scholar
Berka, C., Verma, A., Korszen, S., și Johnson, R. (2014). „Development of EEG biomarkers for Alzheimer’s disease”, în GTC Biomarkers Summit (San Diego, CA).
Bialas, P., și Milanowski, P. (2014). O interfață creier-calculator bazată pe potențialul evocat vizual de înaltă frecvență staționară staționară folosind căști EEG de calitate pentru consumatori. Conf. Proc. IEEE Eng. Med. Biol. Soc. 2014, 5442-5445. doi: 10.1109/EMBC.2014.6944857
PubMed Abstract | CrossRef Full Text | Google Scholar
Caso, F., Cursi, M., Magnani, G., Fanelli, G., Falautano, M., Comi, G., et al. (2012). EEG cantitativ și LORETA: instrumente valoroase în discernerea FTD de AD? Neurobiol. Aging 33, 2343-2356. doi: 10.1016/j.neurobiolaging.2011.12.011
PubMed Abstract | CrossRef Full Text | Google Scholar
Chen, C. C., Hsu, C. Y., Chiu, H. W., Hu, C. J., și ChiehLee, T. (2015). Puterea de frecvență și coerența electroencefalogramei sunt corelate cu severitatea bolii Alzheimer: o analiză multicentrică în Taiwan. J. Formos Med. Assoc. 114, 729-735. doi: 10.1016/j.jfma.2013.07.008
PubMed Abstract | CrossRef Full Text | Google Scholar
Garn, H., Waser, M., Deistler, M., Benke, T., Dal-Bianco, P., Ransmayr, G., et al. (2015). Markerii EEG cantitativi se referă la severitatea bolii Alzheimer în registrul prospectiv al demenței din Austria (PRODEM). Clin. Neurophysiol. 126, 505-513. doi: 10.1016/j.clinph.2014.07.005
PubMed Abstract | CrossRef Full Text | Google Scholar
Goossens, J., Laton, J., Van Schependom, J., Gielen, J., Struyfs, H., Van Mossevelde, S., et al. (2016). Vârful de frecvență dominantă EEG diferențiază între boala Alzheimer și degenerarea lobară frontotemporală. J. Alzheimers Dis. 55, 53-58. doi: 10.3233/JAD-160188
PubMed Abstract |Ref Full Text | Google Scholar
Jakab, A., Kulkas, A., Salpavaara, T., Kauppinen, P., Verho, J., Heikkilä, H., et al. (2014). Nou sistem de electroencefalografie fără fir cu un timp de pregătire minim pentru utilizarea în situații de urgență și în asistența prespitalicească. Biomed. Eng. Online 13:60. doi: 10.1186/1475-925X-13-60
CrossRef Full Text | Google Scholar
Kim, M., Kim, B. H., și Jo, S. (2015). Evaluarea cantitativă a unei interfețe hibride neinvazive low-cost bazate pe EEG și mișcarea ochilor. IEEE Trans. Neural. Syst. Reabilitare. Eng. 23, 159-168. doi: 10.1109/TNSRE.2014.2365834
PubMed Abstract |Ref Full Text | Google Scholar
Kroupi, E., Castellano, M., Ibanez, D., Montplaisir, J., Gagnon, J. F., Postuma, R., et al. (2017). „Deep networks using auto-encoders for PD prodromal analysis”, în Proceedings of 1st HBP Student Conference (Vienna).
Lenartowicz, A., și Loo, S. K. (2014). Utilizarea EEG pentru diagnosticarea ADHD. Curr. Psychiatry Rep. 16:498. doi: 10.1007/s11920-014-0498-0
CrossRef Full Text | Google Scholar
Moretti, D. V., Frisoni, G. B., Binetti, G., și Zanetti, O. (2011). Substratul anatomic și markerii EEG la nivelul scalpului sunt corelați la subiecții cu tulburări cognitive și boala Alzheimer. Front Psychiatry 1:152. doi: 10.3389/fpsyt.2010.00152
PubMed Abstract | Refef Full Text | Google Scholar
Nishida, K., Yoshimura, M., Isotani, T., Yoshida, T., Kitaura, Y., Saito, A., et al. (2011). Diferențe în EEG-ul cantitativ între demența frontotemporală și boala Alzheimer, așa cum reiese din LORET. Clin. Neurophysiol. A 122, 1718-1725. doi: 10.1016/j.clinph.2011.02.011
PubMed Abstract |Ref Full Text | Google Scholar
Pijnenburg, Y. A., Strijers, R. L., Made, Y. V., van der Flier, W. M., Scheltens, P., și Stam, C. J. (2008). Investigarea conectivității funcționale EEG în stare de repaus în degenerarea lobară frontotemporală. Clin. Neurophysiol. 119, 1732-1738. doi: 10.1016/j.clinph.2008.02.024
PubMed Abstract | CrossRef Full Text | Google Scholar
Ruffini, G., David, I.-S., Castellano, M., și Soria-Frisch, A. (2016). „EEG-driven EEG-driven RNN classification for prognosis of neurodegeneration in at-risk patients”, în Internet Corporation for Assigned Names and Numbers (ICANN) (Copenhargen).
Google Scholar
Sarnthein, J., și Jeanmonod, D. (2007). Coerența thalamocorticală ridicată theta la pacienții cu boala Parkinson. J. Neurosci. 27, 124-131. doi: 10.1523/JNEUROSCI.2411-06.2007
PubMed Abstract | CrossRef Full Text | Google Scholar
Schiff, S., Casa, M., Di Caro, V., Aprile, D., Spinelli, G., De Rui, M., et al. (2016). Un sistem de înregistrare electroencefalografică low-cost și ușor de utilizat pentru evaluarea encefalopatiei hepatice. Hepatology 63, 1651-1659. doi: 10.1002/hep.28477
PubMed Abstract | Refef Full Text | Google Scholar
Shani Waninger, S. K., Berka, C., Tan, V., și Johnson, R. (2015). „A novel portable neurocognitive biomarker assessment for Parkinson’s Disease” (O nouă evaluare portabilă a biomarkerilor neurocognitivi pentru boala Parkinson), în GTC Biomarkers Summit (San Diego, CA).
Snyder, S. M., Rugino, T. A., Hornig, M., și Stein, M. A. (2015). Integrarea unui biomarker EEG cu evaluarea ADHD de către un clinician. Brain Behav. 5:e00330. doi: 10.1002/brb3.330
PubMed Abstract | Text integral | Google Scholar
Soria-Frisch, J. M., Ibanez, D., Dunne, S., Grau, C., Ruffini, G., Rodrigues-Brazete, J., et al. (2014). „Machine Learning for a Parkinsons prognosis and diagnosis system based on EEG”, în Proceedings International Pharmaco-EEG Society Meeting IPEG (Leipzig).
Taherian, S., Selitskiy, D., Pau, J., și Claire Davies, T. (2017). Am ajuns deja acolo? Evaluarea interfeței creier-computer de calitate comercială pentru controlul aplicațiilor informatice de către persoanele cu paralizie cerebrală. Disabil. Rehabil. Assist. Technol. 12, 165-174. doi: 10.3109/17483107.2015.1111943
PubMed Abstract | Full CrossRef Text | Google Scholar
Van Hal, B., Rhodes, S., Dunne, B., și Bossemeyer, R. (2014). Detectarea somnului pe bază de EEG cu costuri reduse. Conf. Proc. IEEE Eng. Med. Biol. Soc. 2014, 4571-4574. doi: 10.1109/EMBC.2014.6944641
PubMed Abstract | CrossRef Full Text | Google Scholar
Waninger, S., Stikic, M., Stikic, M., Tatinada, R., și Verma, A. (2016). „Identification of neurophysiological biomarkers of MCI using resting state, EEG” (Identificarea biomarkerilor neurofiziologici ai MCI folosind starea de repaus, EEG), în Conferința internațională a Asociației Alzheimer (Toronto, ON).
Google Scholar
.