Un „mineral” este o substanță anorganică compusă din unul sau mai multe elemente chimice. Prin definiție, un mineral trebuie să fie:
Compoziția chimică a unui mineral este cunoscută sub numele de compoziția sa elementară. Majoritatea mineralelor apar sub formă de compuși (o combinație de mai multe elemente diferite). Cu toate acestea, unele minerale apar ca elemente chimice de sine stătătoare. Acestea sunt cunoscute ca minerale native.
Ce sunt cristalele?
Cristalele sunt o substanță solidă care posedă o structură cristalină organizată care este formată din atomi. Aranjamentul intern al atomilor are deseori ca rezultat fețe plane externe, precum cele observate pe un cristal de cuarț, însă aceasta nu este o cerință pentru a fi clasificat ca un cristal. Cristalele pot fi clasificate diferit de minerale datorită faptului că unele materiale pot fi considerate cristale organice. Deoarece mineralele sunt pur anorganice, un cristal organic nu poate fi un mineral. De exemplu, proteinele și zaharurile sunt solide care pot forma cristale, însă, deoarece sunt substanțe organice, nu pot fi clasificate ca minerale.

Imprejurările din cadrul soluțiilor care formează cristale pot duce la schimbări de culoare, precum și la modificări semnificative ale structurii cristaline. Prea multe impurități în cadrul unei rețele cristaline în timpul cristalizării pot produce cristale cu incluziuni mici sau mari. Aceste incluziuni pot modifica, de asemenea, forma cristalului.
Minerale, cristale sau roci?
Majoritatea mineralelor vor apărea în mod natural sub formă de cristale, însă nu toate cristalele sunt minerale, deoarece cristalele organice nu sunt deloc minerale. Un mineral cu aceeași formulă chimică poate forma mai mult de un tip de cristal. De exemplu, există trei polimorfi (aceeași formulă chimică, structuri cristaline diferite) ai carbonatului de calciu care sunt cunoscuți sub numele de calcit, aragonit și vaterit. Cristalele de calcit apar în sistemul trigonal, cristalele de aragonit aparțin sistemului ortorombic, iar cristalele de vaterit se formează în sistemul hexagonal. Aceste structuri cristaline pot varia în timpul formării ca urmare a mai multor factori care includ impurități care inhibă modelele de creștere, temperatura mediului în timpul formării, saturația mineralelor în cadrul soluției, geometria legăturilor covalente și modificările în mișcarea soluției.
Mineralele au o structură atomică organizată, formată în mod natural, cu o compoziție chimică specifică. Cristalele, în cea mai mare parte, vor împărtăși aceste caracteristici, însă atomii sunt aranjați într-un model repetitiv care are ca rezultat o rețea cristalină, care se prezintă adesea cu fețe cristaline.
De multe ori veți auzi că oamenii numesc mineralele sau cristalele, roci, însă o „rocă” este definită ca un agregat legat de minerale, mineraloizi sau fragmente de alte roci. Cuvântul „legat” înseamnă că agregatul de minerale trebuie să fie într-un fel cimentat împreună. De exemplu, nisipul nu este considerat o rocă, chiar dacă, în cele mai multe cazuri, boabele de nisip sunt agregate împreună. Gresia, de exemplu, a devenit o rocă deoarece boabele de nisip au fost cimentate împreună de minerale cu granulație mai fină și/sau material organic, formând o masă relativ solidă.
Cele trei clasificări majore ale rocilor sunt: ignea, metamorfică și sedimentară.
Rocă igenică – Rocă care s-a format prin răcirea și cristalizarea magmei în interiorul sau deasupra litosferei (scoarța terestră). Cristalele se formează în interiorul magmei pe măsură ce aceasta începe să se solidifice, din care viteza de răcire poate dicta dimensiunea cristalelor care se formează.

O vedere de aproape a granitului porfiric, un tip de rocă ígnea. Granitul porfiric apare atunci când temperatura de răcire a magmei se schimbă rapid. În acest caz, cristalele mari au fost lăsate să se formeze cu o răcire lentă, doar pentru a fi întrerupte de o schimbare bruscă de temperatură descrescătoare care a accelerat procesul de cristalizare, rezultând cristale mai mici.
Rocă sedimentară – Rocă care s-a format ca urmare a depunerii materialelor erodate din rocile formate anterior de-a lungul fundului oceanelor, al paturilor râurilor, al lacurilor etc., împreună cu depunerea de minerale din apă. De-a lungul anilor, aceste depuneri sunt compactate de forțele naturale, pentru ca mai târziu să se solidifice într-o masă solidă (rocă).

Aceasta este o formațiune de rocă sedimentară care face parte din Zabriskie Point, situat în Valea Morții, California. Este compusă din sedimente provenite din lacul Furnace Creek Lake, care a secat în urmă cu aproximativ 5 milioane de ani. Milioane de ani de eroziune au lăsat straturile de sedimente expuse.
Rocă metamorfică – Rocă care a apărut atunci când rocile sedimentare sau igneice existente au fost expuse la presiuni și, în unele cazuri, la schimbări de temperatură care au alterat mineralogia lor originală.

Rocă metamorfică cunoscută sub numele de „gneiss de granit”. Formată din granit metamorfozat.
Cum se formează cristalele anorganice?
Cristalele se pot forma în urma unei varietăți de procese diferite, inclusiv:
Depozite de evaporit – Acestea sunt formațiuni minerale care apar ca urmare a proceselor de la suprafața pământului. Cristalele se formează din soluții care conțin minerale care se concentrează prin deshidratarea/evaporarea unei soluții apoase. Pe măsură ce lichidul este îndepărtat lent prin evaporare, mineralele concentrate se adună și precipită din apă într-un model structurat care se dezvoltă într-un cristal. Un exemplu de depuneri prin precipitare sunt cristalele de halit roz din lacul Seamless Lake din Trona, California.
Depozite de minerale secundare – Acestea se formează prin procesul de expunere a apei la minereuri primare, prin depunere din soluții hidrotermale sau se formează prin cristalizarea magmei.
- Expunere la minereuri primare – Apa care este introdusă în minereurile expuse (de obicei, în interiorul unei cavități) prin percolare descendentă prin roci. Aceasta poate începe procese chimice care descompun minereul și redistribuie mineralele de-a lungul pereților cavității deschise. Azuritul și malachitul sunt exemple bune în acest sens, unde soluțiile apoase s-au deplasat prin zone de minereu primar de cupru și le-au redistribuit sub formă de cristale de azurit și malachit, ale căror cerințe de formare includ apă, carbonați și cupru.
- Depozit de fluide hidrotermale – în cele mai multe cazuri apare pe măsură ce fluidele hidrotermale își croiesc drum în sus prin rocă, preluând în acest proces mineralele din roca înconjurătoare. Atunci când acestor fluide li se prezintă o cavitate deschisă, se poate produce precipitarea mineralelor sub formă de cristale și/sau o masă solidă. Uneori, mineralele din roca înconjurătoare pot fi înlocuite, această apariție fiind cunoscută sub numele de zăcământ de înlocuire.
- Cristalizarea magmei – are loc atunci când magma se răcește și mineralele din magmă încep să se separe în grupuri de minerale asemănătoare și compatibile. În funcție de viteza de răcire, de compoziție și de atmosferă, dimensiunile cristalelor pot varia semnificativ. Uneori, răcirea poate avea loc prea repede, ceea ce duce la lipsa unei structuri elementare, obsidianul (sticla vulcanică) fiind un exemplu în acest sens. Compusă în principal din SiO₂ (cuarț în cele mai multe cazuri), obsidianul are o formulă chimică cu potențialul de a fi un cristal/mineral, însă lipsa structurii cristaline și variabilitatea compoziției duce la clasificarea sa ca mineraloid în schimb.

Mineraloidul, obsidianul.
Clasi de minerale
Compoziția chimică a mineralului dictează modul în care acesta se va prezenta în natură. Unele dintre clasele obișnuite de minerale în funcție de compoziția lor chimică sunt:
Minerale native – Elemente care apar în mod natural cu o structură minerală distinctă și fără combinații cu un alt element. Câteva exemple de elemente despre care se știe că se formează ca minerale native sunt aurul (Au), argintul (Ag), sulful (S), cuprul (Cu), grafitul ((C) – carbon slab împachetat) și diamantele ((C) – carbon dens împachetat – conține de obicei unele impurități).

Diamant natural brut

Argint nativ

Cupru nativ
Oxizi – Clasă de compuși chimici în care un ion oxigen (O2-) se împerechează cu un element, în multe cazuri un metal încărcat pozitiv. Câteva exemple sunt SiO₂ – Cuarț, Fe₂O₃ – Hematită, Cu₂O – Cuprită, etc.
Carbonați – Minerale caracterizate prin prezența unui ion carbonat (CO₃2-). De obicei se leagă de cationi metalici care, în majoritatea cazurilor, formează compuși insolubili (nu pot fi dizolvați în apă). Câteva exemple sunt CaCO₃ – Calcite/Aragonit, FeCO₃ – Siderit, ZnCO₃ – Smithsonit, etc.
Silicați – Minerale dintr-o familie de anioni care conțin atât siliciu (Si), cât și oxigen (O). Aceste săruri formează o componentă majoră a rocilor din întreaga litosferă (scoarța terestră). Câteva exemple de silicați sunt: SiO₂ – Cuarț, AlKO₆Si₂ – Silicat de potasiu și aluminiu, (Fe,Mg)₂SiO₄ – Olivină, etc.
Sulfură (Sulfură) – Anion anorganic de sulf care prezintă formula chimică S^2- și care poate implica reacții considerate destul de complexe. Precipitarea sulfurilor poate include reacții cu metale grele în care se formează precipitate metalice insolubile. Câteva exemple ale acestor metale grele care se formează din ioni de sulfură sunt FeS₂ – Pirita, CuFeS₂ – Calcopirita, PbS – Galena, etc.
Sulfate (Sulfați) – Săruri care se formează atunci când acidul sulfuric (H₂SO₄) reacționează cu o altă substanță chimică. Câteva exemple de sulfați sunt: (Ba,Sr)SO₄ – Barit (Barită), CaSO₄- 2H₂O – Gips, SrSO₄ – Celestina (Celestite), etc.
Fosfați – Minerale caracterizate prin prezența anionului complex (PO₄)^3-., cele mai multe dintre acestea fiind considerate destul de rare în natură. Câteva exemple de fosfați sunt Ca5(PO₄)(OH,F,CL) – Apatita, CuAl₆(PO₄)₄(OH)₈ – 4H₂O – Turcoazul, Fe(II)3(PO4)₂- 8H2O – Vivianita, etc.
Economia cristalelor și mineralelor
În timpurile moderne, pentru ca un mineral să fie considerat că merită să fie exploatat din punct de vedere economic, acesta trebuie să existe ca o concentrație de minerale utile care pot fi prelucrate (exploatate) obținând în același timp un profit. De asemenea, concentrația trebuie să fie suficient de mare pentru ca extracția să fie un proces demn de urmat. Uneori, faptul că mineralul se termină în cadrul minei poate duce la închiderea imediată a acesteia. Din acest motiv, mineritul poate fi o afacere extrem de riscantă din punct de vedere economic.
Metalele sunt în prezent cele mai importante minerale din punct de vedere economic, pentru că sunt folosite pentru o mare varietate de aplicații moderne. Aceste metale sunt extrase din depozite metalifere care constau din minereu (mineralele căutate) și, în cele mai multe cazuri, din mineralele înconjurătoare nedorite, mai puțin economice, cunoscute sub numele de „gangă”.
Terminologie și ilustrații
Element chimic – Un element chimic este o substanță din materie ai cărei atomi conțin toți același număr de protoni, cunoscut sub numele de număr atomic. Tabelul periodic este, într-un anumit sens, o cheie care a fost alcătuită de Dimitri Mendeleev, un chimist rus, pentru a clasifica acești atomi în categorii de elemente pe baza numărului lor de protoni. De exemplu, un atom de hidrogen (H) conține un proton, un atom de heliu (He) conține doi protoni, un atom de litiu (Li) conține trei protoni și așa mai departe.
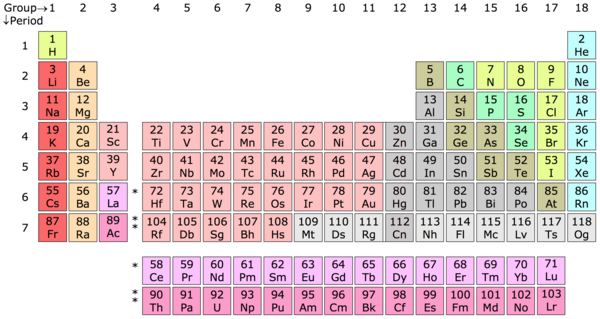
Tabelă periodică
Compus chimic – Format din molecule. Pentru a fi considerată compus chimic, molecula trebuie să fie alcătuită din până la două sau mai multe elemente chimice diferite care sunt legate între ele.
Atom – Cea mai mică unitate a unui element chimic. Un atom este alcătuit din proton(i), electron(i) și neutron(i) care, împreună, determină sarcina atomului. Atomii pot pierde sau câștiga electroni, rezultând sarcini pozitive și negative cunoscute sub numele de ioni.
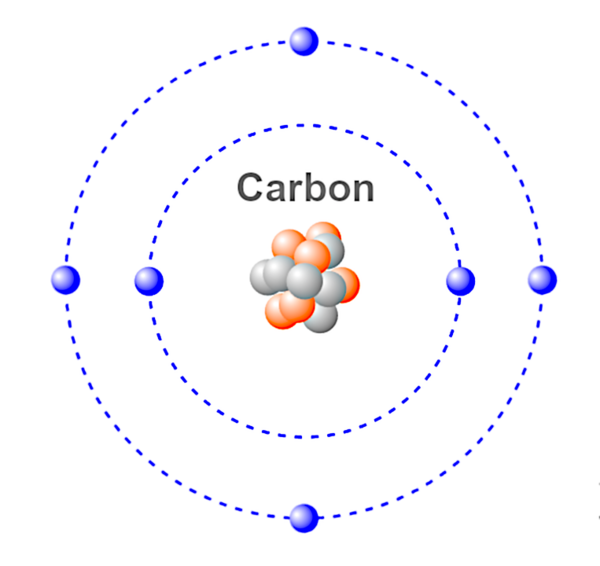
Aceasta este o ilustrație a unui atom de carbon.
Albastru – Electroni.
Roșu & Gri – Neutroni & Protoni.
Ion – Un atom sau o moleculă cu o sarcină electrică care a rezultat în urma pierderii sau câștigării unuia sau mai multor electroni.
Cation – Un ion încărcat pozitiv care este atras de ioni încărcați negativ. Exemplu – Ion de hidrogen H+.
Anion – Un ion încărcat negativ care este atras de ioni încărcați pozitiv. Exemplu – Ionul carbonat este CO₃2-.

Formula chimică a ionului carbonat.
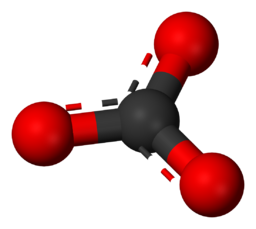
Această imagine ilustrează structura moleculară a unui ion carbonat (CO₃2-) la nivel atomic.
.