(CNN) Se você tiver o azar de ter uma cobra venenosa afundando suas presas em você, sua melhor esperança é um antiveneno, que tem sido feito da mesma forma desde os tempos vitorianos.
Envolve ordenhar veneno de cobra à mão e injectá-lo em cavalos ou outros animais em pequenas doses para evocar uma resposta imunológica. O sangue do animal é retirado e purificado para obter anticorpos que actuam contra o veneno.
Produzir o antiveneno desta forma pode ficar confuso, para não mencionar perigoso. O processo é susceptível a erros, trabalhoso e o soro acabado pode resultar em graves efeitos secundários.
Os especialistas há muito que pedem melhores formas de tratar as mordeduras de cobras, que matam cerca de 200 pessoas por dia.
Agora — finalmente — os cientistas estão a aplicar a pesquisa de células estaminais e o mapeamento do genoma a este campo de pesquisa há muito tempo conhecido. Eles esperam que isso traga a produção de antiveneno para o século 21 e finalmente salve milhares, se não centenas de milhares, de vidas a cada ano.
Pesquisadores na Holanda criaram glândulas produtoras de veneno a partir da Serpente do Cabo Coral e outras oito espécies de cobras no laboratório, usando células-tronco. As toxinas produzidas pelas réplicas em miniatura 3-D das glândulas de cobra são todas menos idênticas ao veneno da cobra, a equipe anunciou quinta-feira.
Em uma descoberta paralela, cientistas na Índia sequenciaram o genoma da cobra indiana, uma das “quatro grandes” cobras do país que são responsáveis pela maioria das 50.000 mortes de mordidas de cobra que a Índia vê por ano.
“Eles realmente mudaram o jogo”, disse Nick Cammack, chefe da equipe de mordidas de cobra da instituição de pesquisa médica britânica Wellcome. “Estes são desenvolvimentos massivos porque está a trazer a ciência de 2020 para um campo que tem sido negligenciado”
De cancro para veneno de cobra
Hans Clevers, o principal investigador do Instituto Hubrecht de Biologia do Desenvolvimento e Investigação de Células Estaminais em Utrecht, nunca esperou estar a usar o seu laboratório para fazer veneno de cobra.
Há uma década atrás, ele inventou a técnica para fazer organóides humanos — órgãos miniatura feitos a partir das células-tronco de pacientes individuais. Eles permitiram aos médicos testar os efeitos específicos das drogas com segurança fora do corpo, algo que revolucionou e personalizou áreas como o tratamento do câncer.
 Os cientistas reproduziram a glândula venenosa da cobra-coral do Cabo, vista aqui no Zoo de Olomouc, República Checa, a 11 de Maio de 2018.
Os cientistas reproduziram a glândula venenosa da cobra-coral do Cabo, vista aqui no Zoo de Olomouc, República Checa, a 11 de Maio de 2018. Então porque é que ele decidiu cultivar uma glândula de veneno de cobra?
Clevers disse que era essencialmente um capricho de três alunos de doutoramento a trabalhar no seu laboratório que se tinham aborrecido de reproduzir ratos e rins humanos, fígados e tripas. “Eu acho que eles se sentaram e se perguntaram qual é o animal mais icônico que podemos cultivar? Não é humano ou rato. Eles disseram que tem de ser a cobra. A glândula venenosa da cobra.”
“Eles assumiram que as cobras teriam células-tronco da mesma forma que os ratos e os humanos têm células-tronco, mas ninguém tinha investigado isso”, disse Clevers.
Após adquirir alguns ovos de cobra fertilizados de um comerciante, os pesquisadores descobriram que eles eram capazes de pegar um pequeno pedaço de tecido de cobra, contendo células-tronco, e alimentá-lo em um prato com o mesmo fator de crescimento que eles usaram para organóides humanos – embora a uma temperatura mais baixa – para criar as glândulas venenosas. E eles descobriram que esses organóides de cobra – pequenas bolas de apenas um milímetro de largura – produziram as mesmas toxinas que o veneno da cobra.
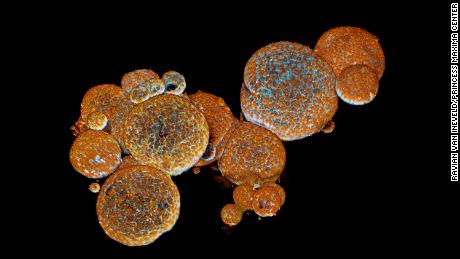 Os organóides das glândulas venenosas das serpentes, vistos sob um microscópio./
Os organóides das glândulas venenosas das serpentes, vistos sob um microscópio./ “Abra-os e terá muito veneno. Tanto quanto podemos dizer, é idêntico. Nós o comparamos diretamente ao veneno da mesma espécie de cobra e encontramos exatamente os mesmos componentes”, disse Clevers, que foi autor do artigo publicado na revista Cell na semana passada.
A equipe comparou o veneno feito em laboratório com o verdadeiro a nível genético e em termos de função, descobrindo que as células musculares pararam de atirar quando expostas ao seu veneno sintético.
 Uma cobra venenosa de óculos, também conhecida como cobra indiana (Naja Naja) ou cobra branca, é vista perto de uma pintura dentro do seu recinto no Jardim Zoológico Kamla Nehru em Ahmedabad em 30 de janeiro de 2019.
Uma cobra venenosa de óculos, também conhecida como cobra indiana (Naja Naja) ou cobra branca, é vista perto de uma pintura dentro do seu recinto no Jardim Zoológico Kamla Nehru em Ahmedabad em 30 de janeiro de 2019. Células e DNA, não cavalos
Os actuais antivenenos disponíveis, produzidos em cavalos não humanos, desencadeiam taxas relativamente altas de reacções adversas, que podem ser leves, como erupções cutâneas e comichão, ou mais graves, como anafilaxia. Também é material caro. A Wellcome estima que um frasco de antiveneno custa $160, e um curso completo geralmente requer múltiplos frascos.
Even se as pessoas que precisam dele podem pagar – a maioria das vítimas de mordidas de cobra vivem em áreas rurais da Ásia e África – o mundo tem menos da metade do estoque de antiveneno que precisa, de acordo com a Wellcome. Além disso, os antivenenos foram desenvolvidos para apenas cerca de 60% das cobras venenosas do mundo.
Neste contexto, a nova pesquisa pode ter consequências de longo alcance, permitindo aos cientistas criar um biobank de organóides de glândulas de cobra das cerca de 600 espécies de cobras venenosas que poderiam ser usadas para produzir quantidades ilimitadas de veneno de cobra em um laboratório, disse Clevers.
“O próximo passo é pegar todo esse conhecimento e começar a investigar novos antivenenos que tenham uma abordagem mais molecular”, disse Clevers.
Para criar um antiveneno, informação genética e tecnologia organóide poderiam ser usados para fazer os componentes específicos do veneno que causam mais danos — e a partir deles produzir anticorpos monoclonais, que imitam o sistema imunológico do corpo, para combater o veneno, um método já usado em tratamentos de imunoterapia para câncer e outras doenças.
“É uma ótima nova forma de trabalhar com o veneno em termos de desenvolver novos tratamentos e desenvolver o antiveneno. As cobras são muito difíceis de cuidar”, disse Cammack, que não estava envolvido com a pesquisa.
Clevers disse que seu laboratório agora planeja fazer organóides de glândulas venenosas dos 50 animais mais venenosos do mundo e eles vão compartilhar esse biobanco com pesquisadores do mundo todo. No momento, Clevers disse que eles são capazes de produzir os organóides a uma taxa de um por semana.
Mas produzir antiveneno não é uma área na qual as empresas farmacêuticas têm tradicionalmente feito questão de investir, disse Clevers
Campeiros muitas vezes descrevem as mordidas de cobra como uma crise de saúde oculta, com mordidas de cobra matando mais pessoas do que câncer prostrado e cólera em todo o mundo, disse Cammack.
“Não há dinheiro nos países que sofrem. Não subestime quantas pessoas morrem. Os tubarões matam cerca de 20 por ano. As cobras matam 100.000 ou 150.000”, disse Clevers.
“Sou um pesquisador de câncer essencialmente e estou chocado com a diferença no investimento na pesquisa do câncer e nesta pesquisa”.
Venom é um coquetel complexo
Um desafio para fazer antiveneno sintético é a pura complexidade de como uma cobra desabilita sua presa. O seu veneno contém vários componentes diferentes que têm efeitos diferentes.
Pesquisadores na Índia sequenciaram o genoma da Cobra indiana, numa tentativa de descodificar o veneno.
Publicado na revista Nature Genetics no início deste mês, é o genoma da cobra mais completo montado e contém a receita genética para o veneno da cobra, estabelecendo a ligação entre as toxinas da cobra e os genes que as codificam. Não é um coquetel simples — a equipe identificou 19 genes de 139 genes de toxinas como os responsáveis por causar danos em humanos.
“É a primeira vez que uma cobra muito importante do ponto de vista médico é mapeada com tanto detalhe”, disse Somasekar Seshagiri, presidente da SciGenom Research Foundation, um centro de pesquisa sem fins lucrativos na Índia.
“Ela cria a planta da cobra e nos ajuda a obter as informações das glândulas venenosas”. A seguir, a sua equipa irá mapear os genomas da víbora em escala de serra, a krait comum e a víbora de Russell — o resto dos “quatro grandes” da Índia. Isto pode ajudar a fazer antiveneno a partir das glândulas, pois será mais fácil identificar as proteínas certas.
Em conjunto, ambos os avanços também tornarão mais fácil descobrir se algumas das moléculas potentes contidas no veneno da cobra valem a pena ser exploradas como drogas — permitindo que as cobras deixem a sua marca na saúde humana de uma forma diferente da pretendida pela natureza — salvando vidas.
O veneno de cobra tem sido usado para fazer drogas que tratam a hipertensão (pressão arterial anormalmente alta) e condições cardíacas como a angina.
“Além de ser assustador, o veneno é incrivelmente útil”, disse Seshagari.