INTRODUÇÃO
Heterozigotosescolesterolemia familiar (FH) é um distúrbio genético comum associado à doença cardiovascular aterosclerótica prematura (ASCVD). Crianças com FH não tratadas correm maior risco de ASCVD prematura após os 20 anos de idade.1 A elevação grave dos níveis de colesterol lipoproteico de baixa densidade (colesterol LDL) começa no feto e leva à exposição sustentada da parede arterial ao colesterol LDL, o que acelera a deposição de colesterol e a inflamação vascular e predispõe ao início precoce da aterosclerose, particularmente nas artérias coronárias e na aorta.
Estatinas e outras terapias para redução de lipídios (LDL) efetivamente reduzem o colesterol LDL, são seguras em crianças e adolescentes, e restauram a função endotelial em idade precoce.2-4 Recentemente, foi proposto o rastreamento universal de crianças a partir dos 2 anos de idade e antes dos 8 anos de idade5,6 para detectar indivíduos que necessitam de tratamento. Entretanto, essa abordagem é baseada em considerações teóricas e não foi comprovada na vida real.
Sem dúvida, pouco se sabe sobre as características dos pacientes com menos de 18 anos de HF, o LBI utilizado nesses pacientes e as metas lipídicas atingidas na vida real. O déficit de informação é ainda maior para os dados de acompanhamento. Os registros nacionais podem ser utilizados para fornecer essa informação crucial, necessária para melhorar os modelos de atendimento da HF, os protocolos terapêuticos e a política de saúde.7,8 O HypErcHolEsterolaemiA CohoRt STudy (SAFEHEART) (NCT02693548) da SpAnish Familial foi projetado para melhorar a percepção dos fatores e mecanismos prognósticos que influenciam o desenvolvimento da ASCVD e da mortalidade em uma população de FH.
Nosso objetivo foi analisar as características dos pacientes e avaliar as metas de LLT e lipídios na inclusão e durante o acompanhamento em pacientes com menos de 18 anos matriculados em SAFEHEART e determinar os fatores que predizem a probabilidade do alcance dessas metas.
METHODSStudy Design and Population
SAFEHEART é um estudo de coorte prospectivo aberto, multicêntrico, nacional e de longo prazo, em uma população de MF definida molecularmente na Espanha. O recrutamento de participantes de famílias de FH começou em 2004 e ainda está em curso. Os critérios de inclusão foram casos de índice com diagnóstico genético de FH e seus familiares com mais de 15 anos com diagnóstico genético de FH, assim como seus familiares sem diagnóstico genético de FH (grupo controle). No entanto, os participantes com menos de 15 anos também foram inscritos, se solicitado por seus pais. Este estudo foi aprovado pelos comitês de ética locais. Todos os indivíduos elegíveis e/ou pelo menos 1 dos seus pais ou tutores legais deram o seu consentimento informado por escrito. Um centro coordenador com sede em Madrid, Espanha, foi responsável pela gestão do acompanhamento dos participantes. Os pacientes e/ou seus pais foram contatados anualmente usando uma chamada telefônica padronizada para registrar mudanças relevantes nos hábitos de vida e medicamentos e quaisquer eventos cardiovasculares ou outros problemas médicos. Os médicos participantes que estavam inscrevendo pacientes e familiares neste registro receberam treinamento, com diretrizes de melhores práticas reforçadas em reuniões anuais com a participação de médicos especialistas na área; além disso, um programa com base eletrônica e aconselhamento telefônico foram usados e um programa de treinamento baseado na web foi implantado para dar suporte ao gerenciamento quando necessário. As decisões de tratamento foram tomadas exclusivamente pelo médico de cada paciente.
Medições clínicas e laboratoriais
As características demográficas e clínicas foram registradas conforme descrito em outros lugares.9 Amostras de sangue venoso foram coletadas após 12 horas de jejum. Amostras de soro, plasma e DNA foram aliquotadas e preservadas a -80°C. Os níveis séricos de colesterol total, triglicérides e colesterol lipoproteico de alta densidade (HDL-C) foram medidos em um laboratório central usando métodos enzimáticos. A concentração sérica de colesterol LDL foi calculada usando a fórmula de Friedewald. O DNA foi isolado do sangue total usando métodos padrão e o FH foi geneticamente diagnosticado usando um microarray de DNA.10 Os objetivos do colesterol LDL foram definidos de acordo com recomendações e objetivos recentes. O colesterol lipoproteico de baixa densidade
mg/dL foi a meta principal.11 Uma meta alternativa para pacientes menores de 14 anos consistia no colesterol LDL mg/dL na ausência de qualquer outro fator de risco cardiovascular (tabagismo, colesterol HDL mg/dL, lipoproteína (a) > 50mg/dL, ou colesterol LDL > 250mg/dL) ou doença cardiovascular prematura nos progenitores ou avós.6 A ASCVD familiar prematura foi definida como a ocorrência de um primeiro evento antes dos 55 anos de idade nos homens e antes dos 65 anos de idade nas mulheres. Classificação da Terapia de Redução de Lipídios
Dose máxima de estatina foi definida como atorvastatina 40 a 80mg/d ou rosuvastatina 20 a 40mg/d, que foram consideradas doses de estatina de alta intensidade. A terapia combinada máxima foi definida como dose máxima de estatina mais ezetimibe 10mg/d. A LLT máxima foi definida como qualquer LLT que se espera produzir pelo menos uma redução de 50% nos níveis basais de LDL-C: sinvastatina 20, 40, ou 80mg/d mais ezetimibe 10mg/d; pravastatina 40mg/d em combinação com ezetimibe 10mg/d; fluvastatina 80mg/d mais ezetimibe 10mg/d; atorvastatina 40 ou 80mg/d com ou sem ezetimibe 10mg/d; atorvastatina 10 ou 20mg/d mais ezetimibe 10mg/d; rosuvastatina 20 ou 40mg/d com ou sem ezetimibe 10mg/d; rosuvastatina 10mg/d mais ezetimibe 10mg/d; e pitavastatina 4mg/d em combinação com ezetimibe 10mg/d.12,13
Análise genética
Mutações do receptor de lipoproteína de baixa densidade do colesterol (LDLR) foram classificadas de acordo com seu efeito conhecido sobre a função da proteína do receptor LDL como nulas (receptor-negativo) e defeituosas (receptor-defectivo), como descrito anteriormente.14 Variantes que levam à completa ausência ou truncamento da proteína (perda da função) demonstrada por análise funcional in vitro ou análise de simulação computadorizada foram classificadas como receptor-negativo. Essas variantes incluíram: a) mutações pontuais que causam um códon de parada prematura; b) mutações de falta de sentido que afetam a quinta repetição rica em cisteína no domínio ligante do gene receptor LDL-C (mutação classe 2A); c) pequenas deleções ou inserções que causam uma mudança de quadro e um códon de parada prematura; e d) rearranjos grandes. As mutações receptor-defectivas foram as restantes mutações de ponto de infravermelho e pequenas deleções e inserções de infravermelho. Todas as mutações sem análise de funcionalidade conhecida por meio de estudos in vitro ou análise de simulação computadorizada foram classificadas como “funcionalidade desconhecida” porque não podíamos ter certeza se o efeito sobre o receptor era negativo ou defeituoso; no entanto, foram consideradas patogênicas porque todos os indivíduos portadores de 1 dessas mutações tinham hipercolesterolemia, enquanto os parentes sem a mutação tinham níveis normais de colesterol.14
Análise Estatística
Análise Estatística foi realizada usando SPSS versão 18.0 (SPSS Inc, Chicago, Illinois, Estados Unidos). A normalidade da distribuição das variáveis foi analisada pelo teste de Kolmogorov-Smirnov. Os dados quantitativos são expressos como mediana e intervalo interquartil (IQR) e os dados qualitativos como número absoluto e percentagem. Duas populações foram definidas: população na entrada (n = 241) e população no acompanhamento (também conhecida como coorte), que incluiu os pacientes que tinham um perfil lipídico plasmático completo no acompanhamento (n = 217). Todas as comparações entre a entrada e o acompanhamento foram realizadas no estudo de coorte. As comparações de frequências entre as variáveis qualitativas foram realizadas utilizando o teste do qui-quadrado. As alterações nas variáveis binárias foram analisadas pelo teste de McNemar. Os valores medianos das variáveis quantitativas foram comparados com o teste não-paramétrico de Mann-Whitney ou com o teste de rank assinado por Wilcoxon pareado, conforme apropriado. Uma análise de regressão logística binária prospectiva foi conduzida no estudo de coorte para determinar as variáveis associadas ao uso de estatinas. Foram incluídas variáveis estatisticamente significativas nas análises univariadas, assim como preditores e confundidores a priori: idade, sexo e acompanhamento em um ambiente primário/especializado. Outra análise de regressão logística binária prospectiva foi realizada no estudo de coorte, excluindo os pacientes que atingiram a meta na entrada, para determinar as variáveis associadas ao alcance da LDL-C
mg/dL. Foram incluídas variáveis estatisticamente significativas nas análises univariadas, assim como preditores e confundidores a priori: idade, sexo, tipo de mutação (nula ou defeituosa), uso de ezetimibe e acompanhamento em um ambiente primário/especializado. As diferenças foram consideradas estatisticamente significativas no P RESULTADOS
Até o momento, 4141 participantes foram inscritos no registro SAFEHEART; 392 são menores de 18 anos. Destes, 241 têm confirmação molecular de FH, sendo 217 acompanhados por um perfil lipídico completo (90,0%) (Figura 1). Vinte e quatro pacientes foram omitidos da análise devido à falta de um perfil lipídico completo no acompanhamento. O acompanhamento foi em um ambiente de cuidados primários para 40 pacientes (18,4%). O tempo médio de seguimento foi de 4,69 anos (IQR, 2,48-6,38 anos).
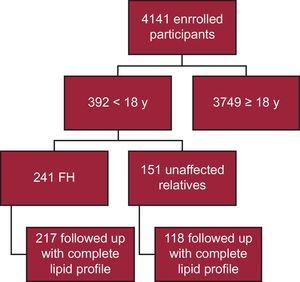
Flowchart esquemático do estudo. FH, hipercolesterolemia familiar.
No momento da inscrição (a população na entrada), 129 pacientes de FH (53,5%) eram do sexo masculino. A mediana da idade foi de 15,0 anos (IQR, 14,0-16,0 anos). Os 2 pacientes mais jovens tinham 8 anos de idade. A história de ASCVD não estava presente em nenhum paciente e a ASCVD familiar precoce estava presente em 40 (16,6%). As características da linha de base estão representadas na Tabela 1. Uma comparação das características basais na inclusão entre os pacientes da coorte e aqueles que não foram acompanhados é mostrada na Tabela 1. Não foram encontradas diferenças significativas entre os 2 grupos. Nenhum paciente tinha histórico de ASCVD, hipertensão arterial ou diabetes mellitus. Uma proporção maior do grupo sem acompanhamento foi gerenciada no contexto da atenção primária, embora a diferença não tenha sido estatisticamente significativa. Na coorte, houve reduções significativas nas concentrações plasmáticas de colesterol total, colesterol LDL, triglicérides e colesterol não-HDL; um aumento significativo no colesterol HDL também foi observado no acompanhamento (Tabela 2).
Baseline Characteristics of the At-entry Population
| Pacientes com seguimento Median (IQR)/no. (%) |
Pacientes FH sem acompanhamento Mediana (IQR)/não. (%) |
P | ||
|---|---|---|---|---|
| Nº. | 217 | 24 | ||
| Sexo (masculino) | 117 (53,9%) | 12 (50%) | .72 | |
| Age, y | 15.0 (14.0-16.0) | 15.0 (13.0-15.8) | .06 | |
| Prematuro ASCVD familiar | 36 (16.6%) | 4 (16.7%) | 1.00 | |
| Fumador de tabaco activo | 13 (6,0%) | 2 (8,3%) | .65 | |
| Xantomas | 1 (0,5%) | 0 (0,0%) | .99 | |
| Corneal arcus | 6 (2,8%) | 1 (4,2%) | .53 | |
| BMI, kg/m2 | 21,09 (19,40-22,80) | 20,79 (17,80-22,70) | .64 | |
| Perímetro da cintura, cm | 72,0 (66,0-78,0) | 72,0 (66,0-75,8) | .94 | |
| Colesterol total, mg/dL | 223,5 (194,0-262.3) | 217,5 (194,5-277,5) | ,76 | |
| LDL-C, mg/dL | 162,6 (133.0-195.8) | 153.9 (13.1-209.3) | .71 | |
| HDL-C, mg/dL | 49.0 (42,8-55,0) | 48,5 (41,5-56,0) | ,96 | |
| TG, mg/dL | 62,0 (49.0-80.3) | 66.0 (42.1-82.3) | .90 | |
| Não-HDL-C, mg/dL | 174.0 (145,8-210,9) | 167,0 (146,5-225,3) | ,74 | |
| Lp (a), mg/dL | 18,80 (7,00-48,50) | 13,45 (9,10-28,10) | .46 | |
| Gerenciado na atenção primária | 40 (22,9%) | 7 (46,7%) | .06 |
ASCVD, doença cardiovascular aterosclerótica; IMC, índice de massa corporal; FH, hipercolesterolemia familiar; HDL-C, colesterol lipoproteico de alta densidade; LDL-C, colesterol lipoproteico de baixa densidade; Lp (a), lipoproteico (a); IQR, intervalo interquartílico; TG, triglicéridos.
Plasma Lipid e Lipoproteínas Concentradas (Cohort)
| Cort na entrada | Cort na entrada | Cort na entrada seguinteup | P | |
|---|---|---|---|---|
| Colesterol total, mg/dL | 221.0 (194.0-260.2) | 203.0 (183.0-233.5) | .001 | |
| LDL-C, mg/dL | 157.7 (132.8-194.5) | 138.0 (116.5-165.4) | .001 | |
| HDL-C, mg/dL | 49.0 (43.0-55.0) | 50.0 (44.0-58.0) | .002 | |
| TG, mg/dL | 62.0 (49.0-80.2) | 70.0 (54.5-91.0) | .004 | |
| Não-HDL-C, mg/dL | 171.0 (145.8-209.2) | 154.0 (132,0-182,5) | .001 |
HDL-C, colesterol lipoproteico de alta densidade; LDL-C, colesterol lipoproteico de baixa densidade; TG, triglicéridos.
Valores são medianos (intervalo interquartílico).
Mutações Funcionais
Identificamos 212 pacientes com mutação nos genes receptores do colesterol LDL (97,7%) e 5 pacientes com mutação nos genes da apolipoproteína B (2,3%). Das mutações nos genes receptores do colesterol LDL, 95 (43,8%) foram classificadas como mutações nulas, 92 (42,4%) como mutações defeituosas, e 25 (11,5%) como mutações de funcionalidade desconhecida.
Terapia Lipide-Lipid-Lipid-Lowering Therapy and Goal Attainment
Tabela 3 mostra o uso de diferentes regimes de LLT na entrada e acompanhamento. Os resultados mostram um aumento significativo no uso de estatinas (44,2% na entrada e 68,2% no acompanhamento), ezetimibe (8,7% na entrada e 15,2% no acompanhamento), dose máxima de estatina (3,3% na entrada e 13,9% no acompanhamento) e LLT máxima (7,9% na entrada e 23,6% no acompanhamento). A estatina mais prescrita na entrada (25,3%) e no acompanhamento (30.5%) foi atorvastatina. A prescrição de atorvastatina aumentou (de 6,0% na inclusão para 20,3% no acompanhamento). A duração mediana da terapia com estatina foi de 7,0 anos (5,0 a 9,0 anos). A idade na menarca foi de 12,0 anos (12,0 a 13,0 anos) para meninas sendo tratadas com estatinas e 12,0 anos (11,0 a 13,0 anos) para meninas não sendo tratadas com estatinas (P = 0,77). Não foi observado aumento de transaminases hepáticas nem de creatina fosfoquinase. Fibratos e seqüestrantes de ácido biliar foram utilizados apenas em 15 pacientes na inclusão (7,0%) e em 3 pacientes no acompanhamento (1,5%). A monoterapia de Ezetimibe sem estatina foi utilizada em 18 pacientes na inclusão (8,3%) e 24 pacientes no acompanhamento (11,1%). Quanto à adesão ao tratamento, 10 pacientes (4,6%) relataram não tomar medicação pelo menos 1 dia a cada mês durante o acompanhamento. Na análise multivariável, nenhuma variável foi associada independentemente ao uso de estatina.
Terapias de redução de lípidos e realização de metas LDL-C (Cohort)
>
| Na entrada/segundo…up- | Na entrada+/follow-up+ | Na entrada+/follow-up- | Na entrada+/follow-up+ | P | |
|---|---|---|---|---|---|
| Patientes sobre estatinas | 60 (27.6%) | 61 (28,1%) | 9 (4,1%) | 87 (40,1%) | .001 |
| Patientes em dose máxima de estatina | 186 (85.7%) | 24 (11,1%) | 1 (0,5%) | 6 (2,8%) | .001 |
| Patientes em ezetimibe | 177 (81,6%) | 21 (9.7%) | 7 (3,2%) | 12 (5,5%) | .013 |
| Patientes em terapia de combinação máxima | 211 (97,2%) | 6 (2,8%) | 0 (0.0%) | 0 (0,0%) | N/A |
| Patientes na LLT máxima | 163 (75,1%) | 37 (17,1%) | 3 (1,4%) | 14 (6,5%) | .001 |
| LDL-C | 111 (51,2%) | 62 (28,6%) | 16 (7.4%) | 28 (12,9%) | .001 |
| LDL-C | 44 (20,3%) | 64 (29.5%) | 19 (8,8%) | 90 (41,5%) | .001 |
LDL-C, colesterol lipoproteico de baixa densidade; LLT, terapia para baixar os lípidos.
Valores são n (%). – = não presente; + = presente.
Ver texto para classificação LLT.
Concentração de CLDL-Plasma diminuiu em média 12,5%, atingindo um valor mediano de 138,0mg/dL no seguimento. As metas de colesterol lipoproteico de baixa densidade, conforme definido pelas recentes recomendações internacionais sobre FH, foram atingidas em 20,3% na entrada e 41,5% no acompanhamento (Tabela 3 e Figura 2). Quando uma meta alternativa de colesterol LDL
mg/dL foi considerada para pacientes menores de 14 anos, 8 de 48 pacientes (16,7%) e 1 de 6 pacientes (16,7%) atingiram a meta na inclusão e no acompanhamento, respectivamente. A única variável independente associada ao alcance da meta do colesterol LDL na análise multivariável foi o uso de estatina (odds ratio, 13,83; intervalo de confiança de 95%, 2,98-64,15). O tipo de profissional de saúde (médico especialista ou clínico geral), idade, sexo, nível de lipoproteína (a) e tipo de mutação não foram associados ao alcance da meta de colesterol LDL.
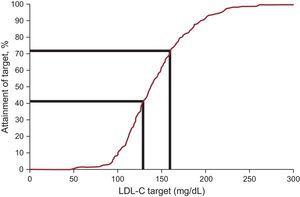
Tratamentos objetivos em pacientes com hipercolesterolemia familiar menores de 18 anos: proporção de pacientes atingindo o objetivo do colesterol LDL. Colesterol LDL, colesterol lipoproteico de baixa densidade.
DISCUSSÃO
Neste estudo, relatamos as características, o uso de LLT e o alcance da meta do colesterol LDL em uma coorte longitudinal de pacientes com menos de 18 anos de idade matriculados no registro SAFEHEART. Este registro único de pacientes com FH é baseado em dados obtidos da vida real na Espanha, tanto em ambientes de cuidados especializados como primários. Nossos resultados mostram que a meta de tratamento do colesterol LDL
mg/dL foi alcançada por apenas 20,3% dos pacientes na inclusão e em 41,5% no acompanhamento, com 68,2% dos pacientes com LDL. O uso de estatina foi o único fator independentemente associado ao alcance da meta do colesterol LDL. Ao nosso conhecimento, nenhum outro trabalho demonstrou atingir a meta em pacientes com insuficiência renal inferior a 18 anos e este estudo é o primeiro a relatá-la em uma grande população.
Recentemente, um registro do Reino Unido15 analisou 207 crianças com insuficiência renal, identificando mutações em 64% das crianças e descobrindo que 48% estavam com LDL; uma redução de 35% foi alcançada no colesterol LDL. Entretanto, os autores não relataram resultados de alcance de metas. Outro relato, que analisou uma pequena amostra de sujeitos (n = 89), mostrou uma redução de 43% no colesterol LDL no acompanhamento a longo prazo.16 Essa maior redução provavelmente se deve ao uso mais frequente de terapia combinada (56%). Não foram mostrados resultados objetivos de realização. Em outro artigo retrospectivo de 207 pacientes na Holanda, apenas 26% dos pacientes estavam com TLB e, mais uma vez, não foram relatados resultados em relação ao alcance da meta de colesterol LDL.17
Este estudo longitudinal mostrou que os níveis de colesterol LDL em pacientes com menos de 18 anos de HF podem mudar com o tempo devido à modificação do TLB e à educação dos médicos. A proporção de pacientes com estatinas, dose máxima de estatina, e LLT máxima aumentou significativamente durante o acompanhamento. Curiosamente, nossos dados indicam que nossa coorte não é tendenciosa porque não houve diferenças estatisticamente significativas entre os pacientes que não foram acompanhados e a coorte.
O diagnóstico e o manejo precoce da HF é essencial, particularmente em crianças e adolescentes, para prevenir o desenvolvimento da ASCVD na vida adulta. A triagem da FH em crianças vale a pena e deve ser realizada antes dos 8 anos de idade, pois crianças com hipercolesterolemia apresentam risco aumentado de ASCVD prematura. Além disso, a triagem pode identificar aqueles que apresentam maior risco e provocar a iniciação de LLT, o que comprovadamente reverte efetivamente o processo aterosclerótico e reduz o risco de ASCVD. Crianças com FH geralmente não apresentam ASCVD clínica. Entretanto, a existência de risco futuro suporta o uso do LBI, sendo as estatinas a pedra fundamental do manejo da HF.18
A segurança e tolerabilidade do LBI na HF pediátrica são sempre controversas, embora sejam relatadas como semelhantes às dos adultos.5,19,20 Recentemente, Ramaswami et al.15 não relataram preocupações de segurança, semelhantes aos nossos resultados. Entretanto, uma supervisão rigorosa é recomendada, especialmente nos pacientes que recebem doses mais altas de estatina. Adolescentes também devem ser aconselhadas a suspender a terapia com estatinas quando estiverem contemplando a gravidez. No entanto, embora sejam necessários mais dados sobre questões de segurança para crianças sob tratamento de longo prazo com LLT, o recente trabalho de acompanhamento de longo prazo mostrou um excelente perfil de segurança.21 Essa constatação é indiretamente apoiada por nossos dados, pois uma alta proporção de pacientes iniciou LLT durante o acompanhamento e houve poucas desistências. Nossos resultados mostram claramente uma porcentagem maior de pacientes usando estatinas, uma dose alta de estatina e o LLT máximo, com uma baixa proporção de pacientes abandonando a medicação. Esses dados confirmam a segurança, aderência e tolerabilidade das estatinas, mesmo quando usadas em altas doses, em pacientes com menos de 18 anos de idade.22 Além disso, nossos resultados concordam com relatos anteriores que não mostram efeitos na maturação sexual.23 Todos esses resultados reafirmam o conceito “quanto mais jovem, melhor” em relação à idade ideal para iniciar estatinas nesses jovens pacientes com insuficiência cardíaca.23
Nossos resultados mostram um número elevado de pacientes com FH menores de 18 anos e, de acordo com estudos anteriores,15,16 sugerem a disposição dos pacientes adultos com FH de incluir seus familiares imediatos nas atividades de triagem e registro. Este fato reflete a seriedade com que estes pacientes levam seu problema e o impacto que os conselhos de seus médicos podem ter na mudança de seu estilo de vida. Tal atitude em pacientes adultos constitui a base de um estilo de vida saudável em seus familiares.24
Embora o objetivo mais comum para pacientes com menos de 18 anos de FH seja um nível de colesterol LDL abaixo de 130mg/dL, uma abordagem alternativa que consiste no colesterol LDL mg/dL pode ser usada em pacientes com menos de 14 anos, não fumantes, com colesterol HDL ≥ 40mg/dL, lipoproteínas (a) mg/dL, colesterol LDL mg/dL, e sem doença cardiovascular prematura em progenitores ou avós.6 Outras diretrizes recentes recomendam uma redução de 50% nos níveis de colesterol LDL a partir do pré-tratamento, mas, para as crianças com idade ≥ 10 anos, especialmente se houver fatores de risco cardiovascular adicionais, incluindo lipoproteínas elevadas (a), a meta de colesterol LDL deve ser mg/dL.11 Nossos resultados também mostram a dificuldade enfrentada por esses pacientes para atingir as metas lipídicas.25 Além disso, a meta de colesterol LDL foi semelhante, quer os pacientes fossem tratados por especialistas ou por médicos da atenção primária. Assim, é possível atingir um nível de cuidados para pacientes pediátricos com HF em um ambiente de cuidados primários que é comparável ao alcançado pelos cuidados especializados. Para esta meta, é importante enfatizar o apoio que os clínicos recebem através de registros e programas de treinamento dedicados. Os registros podem otimizar o manejo de pacientes com FH com menos de 18 anos, possibilitando a integração dos cuidados primários e especializados e podem também apoiar as autoridades de saúde na tomada de decisões.8,26
Limitações e Pontos Fortes
Neste grande estudo de acompanhamento de pacientes com FH com menos de 18 anos, a intervenção não foi alterada em relação à do médico do paciente. Falta um perfil lipídico de base confiável neste registro, pois alguns pacientes já estavam recebendo tratamento quando se inscreveram. Além disso, os resultados podem ter sido alterados por várias condições, como diferentes estilos de vida e uma associação com diferentes fatores de risco cardiovascular que poderiam ter modificado os resultados.
CONCLUSÕES
Dados do registro de FH mostram que uma alta proporção de pacientes com menos de 18 anos de idade têm níveis altos de colesterol LDL e não atingiram as metas recomendadas de colesterol LDL. Encontramos um aumento na intensidade do LDL e uma diminuição significativa nos níveis de colesterol LDL durante o acompanhamento. O uso de estatina foi o único preditor independente do alcance das metas de colesterol LDL. Além disso, não foram detectadas preocupações de segurança durante o acompanhamento. Estes resultados indicam que muitos pacientes com FH não são adequadamente controlados e que ainda há espaço para melhoria do tratamento. Além disso, o acompanhamento desta população de FH pode contribuir para o conhecimento sobre a segurança da LLT ao longo da vida e a idade ideal para o início da terapia para prevenir o desenvolvimento da ASCVD na idade adulta.
FUNDANDO
Este trabalho foi apoiado pelo subsídio G03/181 da Fundación Hipercolesterolemia Familiar, FIS PI12/01289 do Instituto de Salud Carlos III, e subsídio 08-2008 do Centro Nacional de Investigação Cardiovascular.
CONFLITOS DE INTERESSE
Nenhum declarado.
- –
Crianças com hipercolesterolemia familiar heterozigótica não tratada correm maior risco de ASCVD prematura após 20 anos de idade.
- –
Estatinas e outras terapias para baixar os níveis de LDL-C e são seguras em crianças e adolescentes.
- –
Sabe-se pouco sobre as características dos pacientes com menos de 18 anos de FH, as terapias de redução de lipídios usadas nestes pacientes e as metas lipídicas atingidas na vida real.
- –
Este déficit de informação é ainda maior para os dados de acompanhamento.
O QUE ADICIONA ESTE ESTUDO?
- –
Uma elevada proporção de pacientes com menos de 18 anos de FH não consegue atingir as metas recomendadas de colesterol LDL.
- –
Encontramos um aumento na intensidade de LDL e uma diminuição significativa nos níveis de colesterol LDL durante o acompanhamento.
- –
O uso de latina foi o único preditor independente do alcance das metas do colesterol LDL e nenhuma preocupação de segurança foi detectada durante o acompanhamento.
- –
Estes resultados reforçam o conceito de “quanto mais jovem, melhor”.