(CNN) If you’re unlucky enough to have a poisonous snake sink its fangs into you, your best hope is an antivenom, which has been made in the same way since Victorian times.
Polega on na ręcznym dojeniu jadu węża i wstrzykiwaniu go koniom lub innym zwierzętom w małych dawkach, aby wywołać reakcję immunologiczną. Krew zwierzęcia jest pobierana i oczyszczana w celu uzyskania przeciwciał, które działają przeciwko jadowi.
Produkowanie antivenomu w ten sposób może stać się niechlujne, nie wspominając o tym, że niebezpieczne. Proces ten jest podatny na błędy, pracochłonny, a gotowe serum może powodować poważne skutki uboczne.
Eksperci od dawna wzywają do opracowania lepszych sposobów leczenia ukąszeń węży, które zabijają około 200 osób dziennie.
Teraz — wreszcie — naukowcy stosują badania nad komórkami macierzystymi i mapowanie genomu do tej długoignorowanej dziedziny badań. Mają nadzieję, że przyniesie to produkcję antivenomu w XXI wieku i ostatecznie uratuje tysiące, jeśli nie setki tysięcy istnień ludzkich każdego roku.
Badacze z Holandii stworzyli gruczoły produkujące jad z Węża Przylądkowego Koralowego i ośmiu innych gatunków węży w laboratorium, używając komórek macierzystych. Toksyny produkowane przez miniaturowe trójwymiarowe repliki gruczołów węża są identyczne z jadem węża, ogłosił zespół w czwartek.
W równoległym przełomie naukowcy w Indiach zsekwencjonowali genom kobry indyjskiej, jednego z „wielkiej czwórki” węży, które są odpowiedzialne za większość z 50 000 zgonów spowodowanych ukąszeniami węży, które Indie widzą rocznie.
„Oni naprawdę przeniósł grę na”, powiedział Nick Cammack, szef zespołu snakebite w Wielkiej Brytanii badań medycznych charytatywnej Wellcome. „Są to ogromne postępy, ponieważ przynoszą naukę 2020 w dziedzinie, która została zaniedbana.”
Od raka do jadu węża
Hans Clevers, główny badacz w Hubrecht Institute for Developmental Biology and Stem Cell Research w Utrechcie, nigdy nie spodziewał się, że będzie używał swojego laboratorium do robienia jadu węża.
Dziesięć lat temu wynalazł technikę tworzenia ludzkich organoidów — miniaturowych narządów wykonanych z komórek macierzystych poszczególnych pacjentów. Umożliwiły one lekarzom testowanie specyficznych efektów leków bezpiecznie poza organizmem, co zrewolucjonizowało i spersonalizowało obszary takie jak leczenie raka.
 Naukowcy odtworzyli gruczoł jadowy węża koralowego Cape, widzianego tutaj w zoo w Ołomuńcu, Republika Czeska, 11 maja 2018 r.
Naukowcy odtworzyli gruczoł jadowy węża koralowego Cape, widzianego tutaj w zoo w Ołomuńcu, Republika Czeska, 11 maja 2018 r. Dlaczego więc zdecydował się na hodowlę gruczołu jadowego węża?
Clevers powiedział, że był to w zasadzie kaprys trzech doktorantów pracujących w jego laboratorium, którzy znudzili się reprodukcją mysich i ludzkich nerek, wątrób i wnętrzności. „Myślę, że usiedli i zadali sobie pytanie, co jest najbardziej ikonicznym zwierzęciem, jakie możemy hodować? Nie ludzkie czy mysie. Odpowiedzieli, że to musi być wąż. Gruczoł jadowy węża.”
„Założyli, że węże będą miały komórki macierzyste w ten sam sposób, w jaki myszy i ludzie mają komórki macierzyste, ale nikt nigdy tego nie zbadał”, powiedział Clevers.
Po pozyskaniu kilku zapłodnionych jaj węża od dealera, badacze stwierdzili, że byli w stanie wziąć maleńki kawałek tkanki węża, zawierający komórki macierzyste, i pielęgnować go w naczyniu z tym samym czynnikiem wzrostu, którego używali do ludzkich organoidów — choć w niższej temperaturze — aby stworzyć gruczoły jadowe. I odkryli, że te wężowe organoidy — maleńkie kulki o szerokości zaledwie jednego milimetra — produkowały te same toksyny, co jad węża.
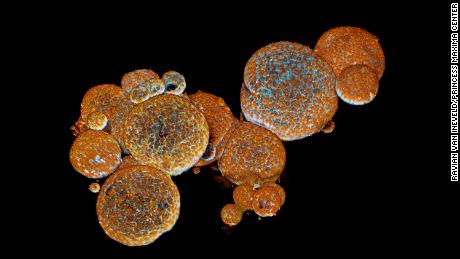 Organoidy gruczołów jadowych węża widziane pod mikroskopem./
Organoidy gruczołów jadowych węża widziane pod mikroskopem./ „Otwórz je i masz dużo jadu. Z tego, co wiemy, jest on identyczny. Porównaliśmy go bezpośrednio do jadu z tego samego gatunku węża i znajdujemy dokładnie te same składniki” – powiedział Clevers, który był autorem pracy opublikowanej w czasopiśmie Cell w zeszłym tygodniu.
Zespół porównał swój laboratoryjny jad z prawdziwą rzeczą na poziomie genetycznym i pod względem funkcji, stwierdzając, że komórki mięśniowe przestały strzelać, gdy zostały wystawione na działanie ich syntetycznego jadu.
 Jadowita kobra okularowa, znana również jako kobra indyjska (Naja Naja) lub kobra biała, jest widziana w pobliżu obrazu wewnątrz swojego wybiegu w Kamla Nehru Zoological Garden w Ahmedabadzie w dniu 30 stycznia 2019 r.
Jadowita kobra okularowa, znana również jako kobra indyjska (Naja Naja) lub kobra biała, jest widziana w pobliżu obrazu wewnątrz swojego wybiegu w Kamla Nehru Zoological Garden w Ahmedabadzie w dniu 30 stycznia 2019 r. Komórki i DNA, nie konie
Obecnie dostępne dla nas antybiotyki, produkowane u koni, a nie u ludzi, wywołują stosunkowo wysokie wskaźniki działań niepożądanych, które mogą być łagodne, jak wysypka i swędzenie, lub bardziej poważne, jak anafilaksja. Jest to również droga rzecz. Wellcome szacuje, że jedna fiolka antivenomu kosztuje 160 dolarów, a pełny kurs zwykle wymaga wielu fiolek.
Nawet jeśli ludzie, którzy go potrzebują, mogą sobie na niego pozwolić – większość ofiar ukąszeń węży żyje w wiejskich rejonach Azji i Afryki – świat ma mniej niż połowę zapasów antivenomu, którego potrzebuje, według Wellcome. Plus antygeny zostały opracowane tylko dla około 60% jadowitych węży na świecie.
W tym kontekście, nowe badania mogą mieć daleko idące konsekwencje, pozwalając naukowcom na stworzenie biobanku organoidów gruczołów węża z 600 lub tak jadowitych gatunków węży, które mogłyby być wykorzystywane do produkcji nieograniczonych ilości jadu węża w laboratorium, powiedział Clevers.
„Następnym krokiem jest wykorzystanie całej tej wiedzy i rozpoczęcie badań nad nowymi środkami przeciwwymiotnymi, które przyjmą bardziej molekularne podejście”, powiedział Clevers.
Aby stworzyć środek przeciwwymiotny, informacje genetyczne i technologia organoidów mogłyby być wykorzystane do stworzenia specyficznych składników jadu, które powodują największe szkody — i na ich podstawie wyprodukować przeciwciała monoklonalne, które naśladują układ odpornościowy organizmu, aby zwalczać jad, metodę już stosowaną w immunoterapii raka i innych chorób.
„To świetny nowy sposób pracy z jadem w zakresie opracowywania nowych metod leczenia i opracowywania antyszczepionki. Węże są bardzo trudne do opieki”, powiedział Cammack, który nie był zaangażowany w badania.
Clevers powiedział, że jego laboratorium planuje teraz zrobić organoidy gruczołów jadowych z 50 najbardziej jadowitych zwierząt na świecie i będą dzielić ten biobank z naukowcami na całym świecie. W tej chwili Clevers powiedział, że są w stanie produkować organoidy w tempie jednego na tydzień.
Ale produkcja antivenomu nie jest obszarem, w który firmy farmaceutyczne tradycyjnie chętnie inwestują, Clevers powiedział
Kampanie często opisują ukąszenia węży jako ukryty kryzys zdrowotny, z ukąszeniami węży zabijają więcej ludzi niż rak prostaty i cholera na całym świecie, Cammack powiedział.
„Nie ma pieniędzy w krajach, które cierpią. Nie lekceważ tego, jak wielu ludzi umiera. Rekiny zabijają około 20 osób rocznie. Węże zabijają 100.000 lub 150.000”, powiedział Clevers.
„Jestem badaczem raka zasadniczo i jestem przerażony różnicą w inwestycjach w badania nad rakiem i te badania.”
Jad to złożony koktajl
Jednym z wyzwań związanych z tworzeniem syntetycznego antivenomu jest sama złożoność tego, jak wąż unieszkodliwia swoją ofiarę. Jego jad zawiera kilka różnych składników, które mają różne efekty.
Badacze z Indii zsekwencjonowali genom kobry indyjskiej, próbując rozszyfrować jej jad.
Opublikowany w czasopiśmie Nature Genetics na początku tego miesiąca, jest najbardziej kompletnym genomem węża i zawiera genetyczny przepis na jad węża, ustanawiając związek między toksynami węża a genami, które je kodują. Nie jest to prosty koktajl – zespół zidentyfikował 19 genów spośród 139 genów toksyn jako te, które są odpowiedzialne za powodowanie szkód u ludzi.
„To pierwszy raz, kiedy bardzo ważny medycznie wąż został zmapowany tak szczegółowo”, powiedział Somasekar Seshagiri, prezes SciGenom Research Foundation, niedochodowego centrum badawczego w Indiach.
„To tworzy schemat węża i pomaga nam uzyskać informacje z gruczołów jadowych.” Następnie jego zespół zmapuje genomy żmii piłokształtnej, kraita zwyczajnego i żmii Russella – reszty indyjskiej „wielkiej czwórki”. Mogłoby to pomóc w stworzeniu antivenomu z gruczołów, ponieważ łatwiej będzie zidentyfikować odpowiednie białka.
W tandemie, oba przełomy ułatwią również odkrycie, czy niektóre z silnych cząsteczek zawartych w jadzie węża są same w sobie warte poszukiwań jako leki — pozwalając wężom odcisnąć swoje piętno na ludzkim zdrowiu w inny sposób niż zamierzała natura — poprzez ratowanie życia.
Jad węża był używany do produkcji leków, które leczą nadciśnienie (nienormalnie wysokie ciśnienie krwi) i choroby serca, takie jak dławica piersiowa.
„Oprócz tego, że jest przerażający, jad jest niesamowicie użyteczny”, powiedział Seshagari.
.