Abstract
左室異状の部位が変化するストレス誘発性心筋症の再発は、珍しい臨床像であり、ストレス誘発性心筋症の様々なサブタイプの発症の基礎となる病態生理メカニズムへの可能性を示唆するものと思われた。
本症例報告では、3週間のうちに逆タコツボ心筋症と頂部タコツボ心筋症を呈した患者を明らかにした。 ストレス誘発性心筋症の左心室局所への関与が多様であることの原因となりうる病態生理的なメカニズムを考察した。
Keywords
ストレス性心筋症、逆タコツボ心筋症、アピカルタコツボ心筋症、S状隔壁、カテコラミン。 非閉塞性心外膜冠動脈
54歳の女性が、発熱、悪寒、血性下痢などの複雑な症状および身体所見を訴えて来院した。 胸部圧迫感、息切れ、びまん性腹痛も認めた。 症状は入院の3日前に始まりました。 入院時、患者はアミオダロン200mg/日を服用し、ビタミンDを補充していた。 カテコールアミンの直接投与やカテコールアミンを急増させる薬物には曝露されていなかった
検査では血圧100/50mmHg、洞性頻脈(レート112)であった。 頸静脈圧は平坦で、頸動脈のアップストロークは脈拍量が少なかった。 収縮期駆出雑音は2/6、第3心音を認めた。 肺の検査では両側底質性crackleを認めた。 末梢浮腫はなかった。
既往歴は、2015年に冠動脈正常、発作性心房細動S/Pアブレーション、喉頭癌S/P喉頭摘出術(気管切開あり)が該当した。 また、放射線治療を受けた脊髄リンパ腫の既往があった。
心電図では洞性頻脈と非特異的ST変化(図1)。 心エコー図ではS状隔壁を有する左心室とLV収縮機能低下(LVEF=35%)を認めた。 局所壁解析ではLV頂部機能の亢進と基部の異栄養を認めた(図2、動画1)。
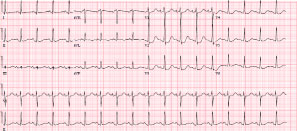 図1:非特異的ST変化を伴う洞性頻脈。 図1
図1:非特異的ST変化を伴う洞性頻脈。 図1
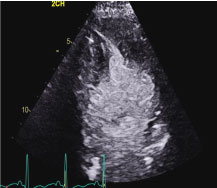 図2:頂部2室収縮末期静止画で、頂部抹消と基部アキネシスが認められる。 図2
図2:頂部2室収縮末期静止画で、頂部抹消と基部アキネシスが認められる。 図2
動画1:心エコー 左心室Apical 2 chamber view with contrast showing left ventricular hyperkinesia (red arrow) and left ventricular basal dyssynergy (yellow arrow)を認める。 心電図上の特徴は、逆たこつぼ心筋症と呼ばれるストレス誘発性心筋症の亜型である。
検査結果はトロポニン7ng/ml、CBC14,000、Hg8.8、クレアチニン2.8であった。 患者の便はヘム陽性であった。 血液培養は陰性であった. 尿比重は10.30であった. 内科的治療として、低用量のBブロッカーとアンジオテンシン変換酵素阻害薬を投与した。 入院後3日目に症状はすべて消失した。 診断名はウイルス性胃腸炎と逆性たこつぼ心筋症の解消であった。 退院後、4週間後に心エコー、血液検査、核ストレス検査、大腸内視鏡検査を行う予定であった。
退院後3週間目に衰弱、低血圧(80/50mmHg)、メラニン便が出現した。 心房細動があり、心室反応は125 bpmと急速であった。 生理食塩水2リットルを投与したところ、自然に正常洞調律に移行し、血圧は110mmHgまで上昇した
身体検査では血圧、心拍数は正常であった。 頸静脈圧は平坦、頸動脈上行は低脈量であった。 聴診では2/6収縮期駆出性雑音とギャロップを認めた。 心電図では洞調律、非特異的なST変化(図3)。 心エコー図では、心尖部と動的基底機能が確認された(図4、動画2)。
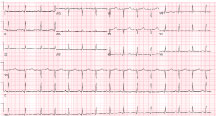 図3:洞調律で非特異的なST変化を認める。 図3
図3:洞調律で非特異的なST変化を認める。 図3
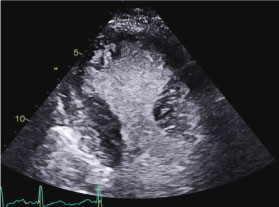 図4:頂部2室収縮末期静止画で頂部アキネジアと底部収縮を確認。 図4
図4:頂部2室収縮末期静止画で頂部アキネジアと底部収縮を確認。 図4
動画2:左心室の心エコー図Apical 2 chamber view with contrastで左心室頂部異状(赤矢印)および左心室底部過緊張(黄矢印)を確認することができる。 心エコー図上の特徴はapical Takotsubo cardiomyopathyと呼ばれるストレス誘発性心筋症の亜型である。
検査所見ではトロポニン2ng/ml、Hg 9.7、WBC 4.4、クレアチニン1.1である。 尿比重は10.20。
経験的抗生物質で治療した。 入院4日目に安定したため、3次医療機関に転院した。 三次救命センターでの評価では、心エコーでLV機能が正常化し、心臓カテーテル検査で冠動脈が正常であった。 大腸内視鏡検査で出血源は発見されなかった. CBCと代謝パネルも正常であった. 最終診断はウイルス性胃腸炎と再発性ストレス誘発性心筋症であった。 ストレス誘発性心筋症(SIC)にはいくつかの解剖学的変異が報告されており、壁運動異常の局所分布に基づいて大きく4つのタイプに分類される。 最も一般的なSIC型は頂部バルーン型であり、広く認知されている形式である。 この10年間でSICの非典型的なタイプが認識されるようになり、midventricular variant、basal variant、focal variantが含まれるようになった。 現在のところ、ほとんどの仮説は、急性の感情的または身体的ストレスの設定におけるカテコールアミンの急増に基づき、カテコールアミン関連の毒性作用が生じるというものである。 最近、カテコールアミンの直接投与やカテコールアミンの急上昇を引き起こす薬剤がしばしばたこつぼ心筋症に関連することを示唆するデータが得られている。 また、化学療法が原因となることもある。
別の説明として、心外膜動脈の血管攣縮、冠動脈の微小血管血流異常などが提案されているが、すべて異論がある。
この症例は、3週間以内に異なるパターンの心室病変を伴うストレス誘発性心筋症を再発した点で稀な症例である。 この患者はS状結節を有しており、S状結節を有する患者のサブセットは、ドブタミン注入時や脱水時に動的な中腔閉塞を発症する可能性があることが示されている. これらの患者は、心内膜下虚血を誘発するのに必要な高レベルのカテコールアミンを経験しないため、心筋症に進行しない可能性が高い。
この患者は、S状中隔により、LVキャビティに2室を形成する動的中洞障害を発症する傾向があった。 全身疾患による脱水とカテコラミンストレスを呈していた。 このような心室形態と全身疾患により、2つの心室の間に勾配が生じたと思われる。
様々な領域のLV病変は、LV空洞が2つの部屋に分離し、中洞の動的閉塞に関連していると思われる。 逆タコツボでは、LVの底部は壁応力の高い高圧室であり、頂部は正常な圧力と壁応力であるため、心筋収縮の異常が観察される。 カテコラミン受容体の活性の違いにより、心内膜下血流が両室で異なる可能性がある。 SICの頂膜型では、LV底部は壁応力の低い低圧室であり、頂膜室は圧力と壁応力が高く、頂膜アキネシスという心筋収縮異常が観察される。
この患者の病気と低液量血のストレスに対するLV形態反応の変化は、様々なタイプのSICの病態生理が多因子であり、LV形態、低液量血、カテコラミン過剰、正常心外膜冠動脈が連動してSICの表現型を決定する可能性を示唆している。
利益相反
著者は本論文の発表に関して利益相反がないことを宣言する
。