Case Report
Omental Massです。
Mascianà G*, Gallo IF, Valeri S and Coppola R
Department of General Surgery, University Campus Bio-Medico, Italy
*Corresponding著者:Mascianà G、Gallo IF、Valei S、Coppola R
。 Mascianà Gianluca, UniversitàCampus Bio-Medico, Via Alvaro delPortillo 21 – 00128 Rome, Italy
Published: 20 Jul, 2017
Cite this article as.を参照のこと。 Mascianà G、Gallo IF、Valeri S、CoppolaR. An Omental Mass: Any Idea? AnnClin Case Rep. 2017; 2: 1406.
Abstract
Pseudomyxoma Extra Peritonei(PE)はまれな所見であり、最も多い原因は虫垂の後腹膜への粘膜破裂である。 本例は52歳女性で,右腹部に腫瘤と漠然とした下腹部痛を訴え,腹腔外被包性腫瘤の切除術を施行された. 病理組織学的検査では,低分化度の粘液性偽粘液腫であった。 8753>
Case Presentation
52歳の女性患者は右腹部の腫瘤と漠然とした下腹部痛のため当院に紹介された。 腹部診察では右肋骨下に大きな固定性腫瘤を認めた。 頸部、腋窩、鼠径部のリンパ節腫脹はなく、腹水の兆候もなかった。 他の検査は正常であったが、CEAの値がわずかに上昇した(8.5ng/ml、正常値:0-2.5)。 胸部と腹部のCT検査で、右脇腹に100mm×70mm×80mmの円形の腫瘤を認め、断端は規則的で、部分的に被膜があり、19mmの内部石灰化と壁在線と高密度中心線条が認められた(Fig. 1)。 USガイド下で腫瘤を吸引したところ、細胞性の物質が検出された。 上下の内視鏡検査は陰性であった。
治療
本症例は集学的チームミーティングにて検討された。 術前診断が困難であったため手術を行い,膵臓,腎臓,腸を含む周囲の構造物から遊離した腹腔外被包性腫瘤を発見した。 この腫瘤は被膜を破ることなく完全に切除された。 病理組織学的解析の結果,低分化度の粘液性偽粘液腫であり,免疫組織化学的にCK20とCK7が陽性であった. 患者は術後4日目に合併症なく退院した。 3年後のフォローアップでは再発の兆候はなかった。
図1
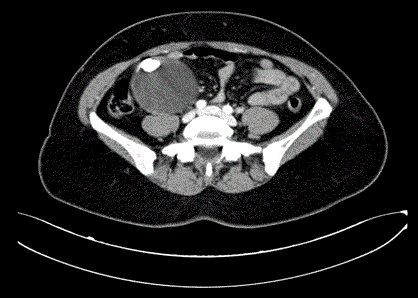
図1
腹部と骨盤のCTスキャン。 右腹部の腫瘤を示す。
表1
ビッグタイトル
| 著者 | 患者(年齢・性別) | 原発腫瘍 | 治療法 | |||||
| Bonnan | 37 M | 1948 | 2段階手術で嚢胞を除去する | |||||
| 初期 | 1968 M | 虫垂粘液嚢 | 腫瘍の摘出 | |||||
| 初期 | 1968 | 付録 | 切除 | |||||
| Brady | 67 M | 1986 | Surgical debulking retroperitoneal chemotherapy | |||||
| Moran | 58 M | 1988 | NA | |||||
| Baker | Rectum | Baker | 44 M 44 M 4241 卵巣摘出術 | |||||
| Snyder | 50 F | 1992 | Excision, omentectomy, 子宮全摘出・卵巣摘出術 | |||||
| Fann | 1993 | NA 切除 | ||||||
| ラドサブリェヴィッチ | 41 M | 1993 | Appendix | 化学療法 | ||||
| シェルトン | 1994 | デバルキングと虫垂切除術 | ||||||
| 玉井 | 1995 | 右半球切除術を行う。 右腸腰筋の切除。 腹膜部分切除術 | ||||||
| ババ | NA | 1995 | 虫垂粘液性嚢胞腺腫 | NA | ||||
| Mor | 65 M | 1996 | デバルキングと盲腸切除 | |||||
| Ben- | 65 M | 1996 | Excision | |||||
| 56 M | 1997 | Download.Pirates | Appendiceal 粘液性腺癌 | Stevens | 65 M | 1996 | Stevens> | 65 M |
| Tsai | 69 M | 1998 | Appendiceal mucinous adenoma | |||||
| Matsuoka | 58 F | 1999 | Mucinous cystadenoma (primary or secondary | NA | ||||
| Koizumi | 46 M | 1999 | 虫垂粘液性腺癌 | 右半月板切除術 | ||||
| エドリーズ | 53 F | 1999 | 虫垂粘液性腺癌 腺癌 | 右半球切除とデバルキング全身化学療法 | ||||
| ピーク | 38 M | 1999 | 切除。 化学療法 | |||||
| 小泉 | 53 M | 1999 | Appendix | NA | ||||
| アルーボゾム | 75 M | 2000 | Appendix | Chemotherapy | ||||
| Kojima | 78 F | 2001 | 右半球切除術 | |||||
| アンゲレスク | NA M | 2001 | NA | |||||
| Liu | 68 F | 2001 | 虫垂切除で粘液のデバルキングを実施。 術中化学療法 全身化学療法 | |||||
| Solkar | 57 M | 2004 | NA | cyst切除 放射線治療 化学療法 | ||||
| 廣川 | 55 F | 2004 | 右半球切除卵巣切除術, 粘液除去 系統的化学療法 A | |||||
| Niwa | 80 F | Appendiceal mucinous adenocarcinoma | Mucous andileum を切除する。 盲腸両卵巣、子宮 | |||||
| Cakmak | Appendiceal mucinous adenocarcinoma | En block resection with partial of Uiliac bone appendectomy, 全身化学療法と放射線療法 | ||||||
| チャミサ | 48 F | 2011 | 脱脂右卵巣摘出術 と化学療法 | |||||
| イオアニディス | 74 M | 2012 | 虫垂粘液腺癌 | デバルキング・ライト 半月板切除術 化学療法 | ||||
| イオアニディス | 68 F | 2012 | 虫垂粘液性腺癌 | Debulking 右半身摘出化学療法 | ||||
| Lim | 2014 | 腹部子宮全摘出術を行う。 両側サルピンゴ卵管切除術、卵管切除術、盲腸切除術、非適正デバルキング | ||||||
| Mavrodin | 2014 | |||||||
| Spyropoulos | 2014 | Appendix | Right hemicolectomy | |||||
| 2014 | 検査・触診で虫垂を認識せず | |||||||
| Joo | 80 F | 2015 | Bilateral salpingooophorectomy with massive adhesiolysis and excision of the 後腹膜腔の腫瘤 | |||||
| Martins | Appendix | 腹腔洗浄を実施。 子宮摘出術、両側卵管卵巣摘出術、卵管切除術、虫垂切除術 |
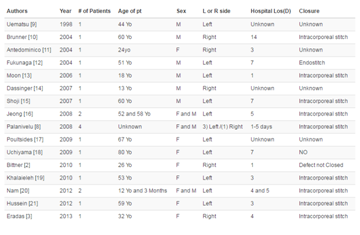
表1. 報告された37例の盲腸
表1
37 件の報告例appendix.
図2
 ×閉じる
×閉じる
![]() ×閉じる
このテキストはjQueryで上書きされます
×閉じる
このテキストはjQueryで上書きされます
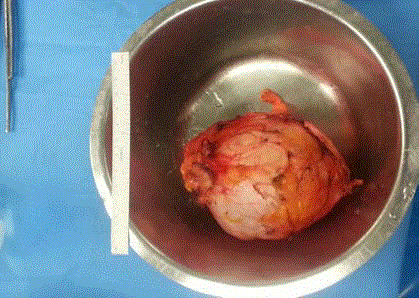
図2
外科用標本。
Discussion

図2
外科用標本。
Werthは1884年に腹膜腔に粘液やゼラチン状の物質が存在するとして腹膜偽粘液腫を初めて報告した。 1948年にBonannが後腹膜のみの偽粘液腫を報告し,その後1950年にCoppiniが表示した。 20年後、Earlyは10リットルの粘液を含む虫垂の後腹膜粘液嚢を報告したが、破裂しなかったため、完全治癒的切除が可能となった;これは1988年にMoranによって腹膜外偽粘液腫(PE)と呼ばれるようになった。 Sheltonらは後にこれを後腹膜偽粘液腫(Pseudomyxoma retroperitonei)と命名した。 後腹膜偽粘液腫は文献上37例しか報告されていない稀な疾患であり、最も多い原因は虫垂の後腹膜への破裂である(表1)。 病理組織学的解析では、異型度や分化度の異なる粘液細胞や上皮細胞の凝集体が認められる。 この細胞は一般にCK20陽性でCK7陰性である。 偽粘液腫は、グレード I または良性播種性腹膜粘液腫症、グレード II または中間亜型、グレード III または悪性腹膜粘液性癌腫症に分類される。 後腹膜偽粘液腫の病因は、ほとんどの場合、腹膜からの漏出で説明される(腹腔内偽粘液腫に伴う後腹膜症状)。 腹膜偽粘液腫がない場合、付録の解剖学的構造の変異(後腹膜の位置)で腹膜外偽粘液腫を説明できるかもしれないが、この仮説はまだ推測にすぎない。術前診断は非常にまれで、疲労、体重減少に伴う食欲低下、触知できる腫瘤の存在、徐々に進行する腹痛または腰痛などの症状が一般的である。 CEAとCA19.9はそれぞれ56%~75%、58%~67%の患者で増加すると報告されている。 超音波検査では腹腔内液としてムチンを検出し、針で吸引して診断することができる。静脈内、経口、直腸造影によるCTでは、密度特性分析によりムチン質を通常の水様液と区別できる(5-20 Hounsfield units formucous vs 0 Hounsfield units for water)。 CTでは、多嚢胞性で隔壁や厚い壁を持つ腫瘤として現れ、隣接する構造物を圧迫する壁在性の石灰化が特徴的であることがある。 手術偽粘液腫の治療は、腹腔内か腹腔外かによって大きく異なる。 腹腔内偽粘液腫に対しては、Sugarbakerらは、粘液性物質の摘出、デバルキング、腹膜切除を含む積極的かつ複雑な外科的処置、および加熱腹腔内温熱化学療法(HIPEC)を用いて、顕微鏡的疾患をできるだけ除去する(細胞還元手術、CRS)ことを推奨している。一方、腹膜外偽粘液腫の推奨される治療法は、良性疾患と同様に、発生部位の切除とそれに続く系統的な化学療法である。 Glehenらは、CRS(完全または不完全)後にHIPECを受けた501例の偽胸腺腫患者の生存期間中央値156カ月、5年および10年生存率はそれぞれ72%と55%であったと報告している。 患者の大部分(約70%)は完全な細胞減量術を受けた。 この均一な治療法により、10年生存率は過去の対照例で記録されたものよりも良好であった。 温熱腹膜透析化学療法の使用に関するデータはないが、再発率が高いため、この治療法を検討すべきである。 手術再発のリスクが高いため、身体検査、CTスキャン、血清マーカーに基づくフォローアップが不可欠である。 後腹膜偽粘液腫の複合治療により、最大70%の患者が20年生存する一方、重要な腹部組織が侵された腹膜内偽粘液腫の生存率はより低い。 Arch Gynaecol。 1884; 24: 100-118.