Nome generico: aciclovir
Forma farmaceutica: crema
Medicamente rivisto da Drugs.com. Ultimo aggiornamento: 1 dic 2020.
- Panoramica
- Effetti collaterali
- Dosaggio
- Professionale
- Interazioni
- Più
- Indicazioni e uso per Zovirax Crema
- Zovirax Cream Dosaggio e amministrazione
- Forme di dosaggio e dosaggi
- 4CONTRAINDICAZIONI
- Avvertenze e precauzioni
- Generali
- Sensibilizzazione di contatto
- Reazioni avverse
- esperienza negli studi clinici
- Esperienza post-marketing
- Interazioni farmacologiche
- USO IN POPOLAZIONI SPECIFICHE
- Riassunto del rischio
- Gravidanza
- Allattamento
- Uso pediatrico
- Uso geriatrico
- Sovradosaggio
- Zovirax Crema Descrizione
- Zovirax Cream – Farmacologia clinica
- Meccanismo d’azione
- Farmacocinetica
- Microbiologia
- Tossicologia non clinica
- Carcinogenesi, mutagenesi, compromissione della fertilità
- Studi clinici
- Soggetti adulti
- Soggetti pediatrici
- Come viene fornito/conservazione e manipolazione
- Informazioni per la consulenza al paziente
- INFORMAZIONE PER I PAZIENTIZOVIRAX (zho-vahy-rex)(aciclovir)Crema
- Pannello espositivo principale – Tubo da 5 g in cartone
- Più informazioni su Zovirax Cream (aciclovir topico)
- Risorse per i consumatori
- Risorse per i professionisti
- Altre formulazioni
- Guide correlate al trattamento
Indicazioni e uso per Zovirax Crema
Zovirax Crema è un analogo deossinucleosidico del virus herpes simplex (HSV) inibitore della polimerasi del DNA indicato per il trattamento di herpes labialis ricorrente (herpes labiale) in adulti immunocompetenti e adolescenti di 12 anni di età e più anziani.
Zovirax Cream Dosaggio e amministrazione
Zovirax Cream deve essere applicato 5 volte al giorno per 4 giorni. La terapia deve essere iniziata il più presto possibile dopo la comparsa di segni o sintomi di herpes labialis, cioè durante il prodromo o quando appaiono le lesioni.
Per gli adolescenti di 12 anni e più, il dosaggio è lo stesso degli adulti.
Forme di dosaggio e dosaggi
Ogni grammo di Zovirax Cream contiene 50 mg (equivalente al 5% p/p) di aciclovir.
4CONTRAINDICAZIONI
Zovirax Crema è controindicato nei pazienti con ipersensibilità conosciuta all’aciclovir, valaciclovir, o qualsiasi componente della formulazione.
Avvertenze e precauzioni
Generali
Zovirax Crema deve essere applicato soltanto sugli aspetti esterni colpiti delle labbra e del viso nei pazienti con herpes labialis. Poiché non ci sono dati disponibili, l’applicazione alle membrane mucose umane non è raccomandata. Zovirax Cream è destinato soltanto all’uso cutaneo e non deve essere usato nell’occhio o dentro la bocca o il naso.
Sensibilizzazione di contatto
Zovirax Cream ha un potenziale per irritazione e sensibilizzazione di contatto.
L’effetto di Zovirax Cream non è stato stabilito in pazienti immunocompromessi.
Reazioni avverse
esperienza negli studi clinici
Perché gli studi clinici sono condotti in condizioni molto diverse, i tassi di reazione avversa osservati negli studi clinici di un farmaco non possono essere direttamente comparati ai tassi negli studi clinici di un altro farmaco e possono non riflettere i tassi osservati nella pratica clinica.
In cinque studi in doppio cieco, controllati con placebo, 1124 pazienti sono stati trattati con Zovirax Cream e 1161 con placebo (veicolo) cream. Le reazioni locali al sito di applicazione sono state riportate dal 5% dei pazienti che hanno ricevuto Zovirax Cream e dal 4% dei pazienti che hanno ricevuto il placebo. Le reazioni avverse più comuni al sito di applicazione topica sono state labbra secche, desquamazione, secchezza della pelle, labbra screpolate, bruciore della pelle, prurito, desquamazione della pelle e bruciore sulla pelle; ogni reazione avversa si è verificata in meno dell’1% dei pazienti che hanno ricevuto Zovirax crema e placebo. Tre pazienti con Zovirax crema e un paziente con placebo hanno interrotto il trattamento a causa di un evento avverso.
Un ulteriore studio, che ha arruolato 22 adulti sani, è stato condotto per valutare la tolleranza dermica di Zovirax crema rispetto al veicolo utilizzando la metodologia del patch test singolo occluso e semi-occluso. Sia Zovirax Cream che il placebo hanno mostrato un potenziale di irritazione elevato e cumulativo. Un altro studio, che ha arruolato 251 adulti sani, è stato condotto per valutare il potenziale di sensibilizzazione da contatto di Zovirax Cream usando una metodologia di patch test a insulto ripetuto. Su 202 soggetti valutabili, possibili reazioni di sensibilizzazione cutanea sono state osservate negli stessi 4 (2%) soggetti sia con Zovirax Crema che con placebo, e queste reazioni sia a Zovirax Crema che a placebo sono state confermate in 3 soggetti su rechallenge. L’ingrediente o gli ingredienti sensibilizzanti non sono stati identificati.
Il profilo di sicurezza nei pazienti da 12 a 17 anni di età era simile a quello osservato negli adulti.
Esperienza post-marketing
In aggiunta agli eventi avversi riportati dagli studi clinici, i seguenti eventi sono stati identificati durante l’uso post-approvazione di aciclovir crema. Poiché sono stati riportati volontariamente da una popolazione di dimensioni sconosciute, non è possibile effettuare stime della frequenza. Questi eventi sono stati scelti per l’inclusione a causa di una combinazione di gravità, frequenza di segnalazione o potenziale connessione causale con aciclovir crema.
Generale: Angioedema, anafilassi.
Pelle: Dermatite da contatto, eczema.
Interazioni farmacologiche
L’esperienza clinica non ha identificato interazioni derivanti dalla somministrazione topica o sistemica di altri farmaci in concomitanza con Zovirax crema. A causa del minimo assorbimento sistemico di Zovirax crema, le interazioni sistemiche con i farmaci sono improbabili.
USO IN POPOLAZIONI SPECIFICHE
Riassunto del rischio
L’aciclovir è minimamente assorbito per via sistemica in seguito a somministrazione topica e non si prevede che l’uso materno comporti un’esposizione fetale a Zovirax crema. L’esperienza con l’uso topico di aciclovir in donne in gravidanza nel corso di diversi decenni, sulla base della letteratura pubblicata, compresi gli studi osservazionali, non ha identificato un rischio associato al farmaco di gravi difetti alla nascita, aborto spontaneo o esiti avversi materni o fetali. Sono stati condotti studi sulla riproduzione animale con esposizione sistemica di aciclovir. Fare riferimento alle informazioni sulla prescrizione di aciclovir per ulteriori dettagli.
Il rischio di fondo stimato di difetti di nascita maggiori e aborto spontaneo per la popolazione indicata non è noto. Tutte le gravidanze hanno un rischio di fondo di difetti alla nascita, perdita o altri esiti avversi. Nella popolazione generale degli Stati Uniti, il rischio di fondo stimato di difetti di nascita maggiori e di aborto spontaneo nelle gravidanze clinicamente riconosciute è dal 2% al 4% e dal 15% al 20%, rispettivamente.
Gravidanza
Riassunto dei rischi
L’aciclovir è minimamente assorbito per via sistemica in seguito a somministrazione topica, e non si prevede che l’uso materno comporti un’esposizione fetale a Zovirax Crema. L’esperienza con l’uso topico di aciclovir in donne incinte nel corso di diversi decenni, basata sulla letteratura pubblicata, compresi gli studi osservazionali, non ha identificato un rischio associato al farmaco di gravi difetti alla nascita, aborto spontaneo o esiti avversi materni o fetali. Sono stati condotti studi sulla riproduzione animale con esposizione sistemica di aciclovir. Fare riferimento alle informazioni sulla prescrizione di aciclovir per ulteriori dettagli.
Il rischio di fondo stimato di difetti di nascita maggiori e aborto spontaneo per la popolazione indicata non è noto. Tutte le gravidanze hanno un rischio di fondo di difetti alla nascita, perdita o altri esiti avversi. Nella popolazione generale degli Stati Uniti, il rischio di fondo stimato di difetti di nascita maggiori e di aborto spontaneo nelle gravidanze clinicamente riconosciute è dal 2% al 4% e dal 15% al 20%, rispettivamente.
Allattamento
Riassunto del rischio
Aciclovir è minimamente assorbito per via sistemica dopo la somministrazione topica, e non si prevede che l’allattamento al seno comporti l’esposizione del bambino a Zovirax Crema. Non ci sono dati sugli effetti di ZOVIRAX sul bambino allattato al seno o sulla produzione di latte. I benefici per lo sviluppo e la salute dell’allattamento al seno devono essere considerati insieme al bisogno clinico della madre per Zovirax Crema e qualsiasi effetto avverso potenziale sul bambino allattato al seno da Zovirax Crema o dalla condizione materna sottostante.
Uso pediatrico
Uno studio in aperto, non controllato con Zovirax Crema è stato condotto in 113 pazienti di età compresa tra 12 e 17 anni con herpes labialis ricorrente. In questo studio, la terapia è stata applicata utilizzando lo stesso regime di dosaggio degli adulti e i soggetti sono stati seguiti per gli eventi avversi. Il profilo di sicurezza è stato simile a quello osservato negli adulti. La sicurezza e l’efficacia nei pazienti pediatrici di età inferiore ai 12 anni non sono state stabilite.
Uso geriatrico
Gli studi clinici di aciclovir crema non hanno incluso un numero sufficiente di soggetti di età superiore ai 65 anni per determinare se essi rispondono diversamente dai soggetti più giovani. Altre esperienze cliniche riportate non hanno identificato differenze nelle risposte tra pazienti anziani e giovani. L’assorbimento sistemico di aciclovir dopo somministrazione topica è minimo.
Sovradosaggio
Il sovradosaggio tramite applicazione topica di Zovirax crema è improbabile a causa della minima esposizione sistemica. Non ci sono informazioni disponibili per il sovradosaggio.
Zovirax Crema Descrizione
ZOVIRAX è il nome commerciale dell’aciclovir, un analogo deossinucleosidico sintetico attivo contro gli herpes virus. Zovirax Cream 5% è una formulazione per somministrazione topica.
Il nome chimico dell’aciclovir è 2-amino-1,9-diidro-9–6H-purin-6-one; ha la seguente formula strutturale:
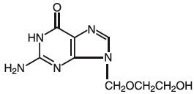
Acyclovir è una polvere bianca, cristallina con la formula molecolare C8H11N5O3 e un peso molecolare di 225. La solubilità massima in acqua a 37°C è di 2,5 mg/mL. I pKa di aciclovir sono 2,27 e 9,25.
Ogni grammo di Zovirax Cream contiene 50 mg (equivalente al 5% w/w) di aciclovir e i seguenti ingredienti inattivi: alcool cetostearilico, olio minerale, poloxamer 407, glicole propilenico, sodio laurilsolfato, acqua e petrolato bianco.
Zovirax Cream – Farmacologia clinica
Meccanismo d’azione
Acyclovir è un farmaco antivirale attivo contro gli α-herpesvirus.
Farmacocinetica
Uno studio di farmacologia clinica è stato eseguito con Zovirax Cream in volontari adulti per valutare l’assorbimento percutaneo di aciclovir. In questo studio, che includeva 6 volontari maschi, la crema è stata applicata su un’area di 710 cm2 sulla schiena dei volontari 5 volte al giorno a intervalli di 2 ore per un totale di 4 giorni. Il peso della crema applicata e l’escrezione urinaria di aciclovir sono stati misurati quotidianamente. La concentrazione plasmatica di aciclovir è stata valutata 1 ora dopo l’applicazione finale. L’escrezione urinaria media giornaliera di aciclovir era circa lo 0,04% della dose giornaliera applicata. Le concentrazioni plasmatiche di aciclovir erano inferiori al limite di rilevamento (0,01 μM) in 5 soggetti e appena rilevabili (0,014 μM) in 1 soggetto. L’assorbimento sistemico di aciclovir da Zovirax crema è minimo negli adulti.
L’assorbimento sistemico di aciclovir in seguito all’applicazione topica della crema non è stato valutato in pazienti <18 anni di età.
Microbiologia
Meccanismo di azione: Acyclovir è un analogo purinico deossinucleosidico sintetico con attività inibitoria in coltura cellulare e in vivo contro le DNA polimerasi dell’HSV di tipo 1 (HSV-1) e 2 (HSV-2). Inibisce la replicazione di HSV-1 e HSV-2 in coltura cellulare e in vivo.
L’attività inibitoria di aciclovir è selettiva a causa della sua affinità per l’enzima timidina chinasi (TK) codificato da HSV. Questo enzima virale converte l’aciclovir in aciclovir monofosfato, un analogo deossinucleotidico. Il monofosfato viene ulteriormente convertito in difosfato dalla guanilato chinasi cellulare e in trifosfato da una serie di enzimi cellulari. Nei saggi biochimici, l’aciclovir trifosfato inibisce la replicazione del DNA virale dell’α-herpes. Questa inibizione si realizza in 3 modi: 1) inibizione competitiva della DNA polimerasi virale, 2) incorporazione e terminazione della catena di DNA virale in crescita, e 3) inattivazione della DNA polimerasi virale.
Attività antivirale
La relazione quantitativa tra la suscettibilità degli herpes virus agli antivirali in coltura cellulare e la risposta clinica alla terapia non è stata stabilita negli esseri umani, e i test di sensibilità ai virus non sono stati standardizzati. I risultati dei test di sensibilità, espressi come la concentrazione di farmaco necessaria per inibire del 50% la crescita del virus nella coltura cellulare (valore EC50), variano notevolmente a seconda di una serie di fattori. Usando test di riduzione della placca su cellule Vero, i valori EC50 di aciclovir contro gli isolati del virus dell’herpes simplex vanno da 0,09 a 59,9 μM (da 0,02 a 13,5 μg/mL) per HSV-1 e da 0.04 a 44,0 μM (da 0,01 a 9,9 μg/mL) per HSV-2.
Resistenza
Nella cultura cellulare
Sono stati isolati ceppi di HSV-1 e HSV-2 resistenti all’aciclovir nella cultura cellulare. HSV resistente all’aciclovir è risultato da mutazioni nei geni virali della timidina chinasi (TK; pUL23) e della DNA polimerasi (POL; pUL30). Frameshifts sono stati comunemente isolati e risultano in troncamento prematuro del prodotto HSV TK con conseguente diminuzione della suscettibilità all’aciclovir. Le mutazioni nel gene TK virale possono portare alla perdita completa dell’attività TK (TK negativo), a livelli ridotti di attività TK (TK parziale), o all’alterazione della capacità del TK virale di fosforilare il farmaco senza una perdita equivalente della capacità di fosforilare la timidina (TK alterato). Nella cultura cellulare sono state osservate le seguenti sostituzioni associate alla resistenza nel TK di HSV-1 e HSV-2 (tabella 1).
|
HSV-1 |
TK |
P5A, H7Q, L50V, G56V, G59A, G61A, K62N, T63A, E83K, P84S, D116N, P131S, R163H, A167V, P173L, Q185R, R216S, R220H, T245M, R281stop, T287M, M322K |
|
HSV-2 |
TK |
L69P, C172R, T288M |
|
HSV-1 |
POL |
D368A, Y557S, E597D, V621S, L702H, N815S, V817M, G841C |
|
HSV-2 |
POL |
In pazienti infettati da HSV
Clinici HSV-1 e HSV-2 isolati ottenuti da pazienti che hanno fallito il trattamento delle loro infezioni da α-herpesvirus sono stati valutati per i cambiamenti genotipici nei geni TK e POL e per la resistenza fenotipica all’aciclovir (Tabella 2). Sono stati identificati isolati HSV con mutazioni frameshift e sostituzioni associate alla resistenza in TK e POL. L’elenco delle sostituzioni in TK e POL di HSV che portano a una ridotta suscettibilità all’aciclovir non è completo e ulteriori cambiamenti saranno probabilmente identificati in varianti di HSV isolate da pazienti che non riescono a seguire regimi contenenti aciclovir. La possibilità di una resistenza virale all’aciclovir dovrebbe essere presa in considerazione nei pazienti che non rispondono o che presentano uno spargimento virale ricorrente durante la terapia.
|
HSV-1 |
TK |
G6C, R32H, R41H, R51W, Y53C/D/H, Y53stop, D55N, G56D/S, P57H, H58/N/R/Y, G59R, G61A, K62N, T63I, Q67stop, S74stop, Y80N, E83K, P84L, Y87H, W88R, R89Q/W, E95stop, T103P, Q104H, Q104stop, H105P, D116N, M121L/R, S123R, Q125H, M128L, G129D, I143V, A156V, D162A/H/N, R163G/H, L170P, Y172C, P173L, A174P, A175V, R176Q/W, R176stop, L178R, S181N, V187M, A189V, V192A, G200C/D/S, T201P, V204G, A207P, L208F/H, R216C/H, R220C/H, R221H, R222C/H, L227F, T245M/P, L249P, Q250Stop, C251G, R256W, E257K, Q261R, T287M, L288Stop, L291P/R, L297S, L315S, L327R, C336Y, Q342Stop, T354P, L364P, A365T |
|
HSV-2 |
TK |
R34C, G39E, R51W, Y53N, G59P, G61W, S66P, A72S, D78N, P85S, A94V, N100H, I101S, Q105P, T131P, D137stop, F140L, L158P, S169P, R177W, S182N, M183I, V192M, G201D, R217H, R221C/H, Q222stop, R223H, Y239stop, R271V, P272S, D273R, T287M, C337Y |
|
HSV-1 |
POL |
K532T, Q570R, L583V, A605V, A657T, D672N, V715G, A719T/V, S724N, F733C, E771Q, S775N, L778M, E798K, V813M, N815S, G841S, I890M, G901V, V958L H1228D |
|
HSV-2 |
POL |
E250Q, D307N, K533E, A606V, C625R, R628C, E678G, A724V, S725G, S729N, I731F, Q732R, M789K/T, V818A, N820S, Y823C, Q829R, T843A, M910T, D912N/V, A915V, F923L, T934A, R964H |
Nota: Possono esistere ulteriori sostituzioni per la resistenza all’aciclovir.
Resistenza incrociata
La resistenza incrociata è stata osservata tra gli isolati HSV che portano mutazioni frameshift e sostituzioni associate alla resistenza, che conferiscono una ridotta suscettibilità a penciclovir (PCV), famciclovir (FCV), e foscarnet (FOS).
|
Resistenza incrociata a PCV/FCV |
HSV-1 TK |
G6C, R32H, R51W, Y53C/H, H58N, G61A, S74Stop, E83K, P84L, T103P, Q104Stop, D116N, M121R, I143V, R163H, L170P, Y172C, A174P, R176Q/W, Q185R, A189V, G200D, L208H, R216C, R220H, R222C/H, T245M, Q250Stop, R256W, R281Stop, T287M, L315S, M322K, C336Y |
|
Resistente a PCV/FCV |
HSV-1 POL |
A657T, D672N, V715G, A719V, S724N, E798K, N815S, G841S |
|
Resistente al PCV/FCV |
HSV-2 TK |
G39E, R51W, Y53N, R177W, R221H, T288M |
|
Resistente a PCV/FCV |
HSV-2 POL |
K533E, A606V, C625R, R628C, S729N, Q732R, M789K/T, V818A, N820S, F923L, T934A |
|
Resistente a FOS |
HSV-1 POL |
D368A, A605V, D672N, L702H, V715G, A719T/V, S724N, L778M, E798K, V813M, N815S, V817M, G841C/S, I890M, |
|
Resistente al FOS |
HSV-2 POL |
K533E, A606V, C625R, R628C, A724V, S725G, S729N, I731F, Q732R, M789K/T, V818A, Y823C, D912V, F923L, T934A, R964H |
Tossicologia non clinica
Carcinogenesi, mutagenesi, compromissione della fertilità
L’esposizione sistemica dopo la somministrazione topica di aciclovir è minima. Non sono stati condotti studi di carcinogenicità cutanea. I risultati degli studi di carcinogenesi, mutagenesi e fertilità non sono inclusi nelle informazioni complete sulla prescrizione di Zovirax Crema a causa delle esposizioni minime di aciclovir che risultano dall’applicazione cutanea. Le informazioni su questi studi sono disponibili nelle informazioni complete di prescrizione per ZOVIRAX Capsule, Compresse e Sospensione e ZOVIRAX per Iniezione.
Studi clinici
Soggetti adulti
Zovirax Crema è stato valutato in due studi in doppio cieco, randomizzati, controllati con placebo (veicolo) per il trattamento di herpes labialis ricorrente. Il paziente medio ha avuto cinque episodi di herpes labiale nei 12 mesi precedenti. Nel primo studio, l’età mediana dei soggetti era di 37 anni (da 18 a 81 anni), il 74% era femmina e il 94% era caucasico. Nel secondo studio, l’età mediana dei soggetti era di 38 anni (da 18 a 87 anni), il 73% era di sesso femminile e il 94% era caucasico. I soggetti sono stati istruiti ad iniziare il trattamento entro 1 ora dalla comparsa di segni o sintomi e a continuare il trattamento per 4 giorni, con l’applicazione del farmaco in studio 5 volte al giorno. In entrambi gli studi, la durata media dell’episodio di herpes labialis ricorrente è stata di circa mezza giornata più breve nei soggetti trattati con Zovirax Crema (n = 682) rispetto ai soggetti trattati con placebo (n = 703) per circa 4,5 giorni contro 5 giorni, rispettivamente. Nessuna differenza significativa è stata osservata tra i soggetti che hanno ricevuto Zovirax Cream o placebo nella prevenzione della progressione delle lesioni da herpes labiale.
Soggetti pediatrici
Uno studio in aperto, non controllato con Zovirax Cream è stato condotto su 113 pazienti di età compresa tra 12 e 17 anni con herpes labialis ricorrente. In questo studio, la terapia è stata applicata utilizzando lo stesso regime di dosaggio degli adulti e i soggetti sono stati seguiti per gli eventi avversi. Il profilo di sicurezza era simile a quello osservato negli adulti.
Come viene fornito/conservazione e manipolazione
Ogni grammo di Zovirax crema contiene 50 mg (equivalente al 5% p/p) di aciclovir in una base di crema acquosa. Zovirax crema è fornito come segue:
NDC 0187-0994-45: tubi da 5 g
Conservare a 25°C (77°F) o al di sotto; escursioni permesse da 15° a 30°C (59° a 86°F).
Informazioni per la consulenza al paziente
Si consiglia al paziente di leggere l’etichettatura approvata dalla FDA (Informazioni per il paziente).
Generale
I pazienti devono essere informati che Zovirax Cream è una crema topica prescritta per il trattamento di herpes labiale (herpes labialis ricorrente) che si verifica sul viso e sulle labbra. Zovirax Cream non è una cura per l’herpes labiale. I pazienti devono essere informati che Zovirax Cream è destinato all’uso cutaneo solo per l’herpes labiale delle labbra e intorno alla bocca. I pazienti devono essere avvisati che Zovirax Cream non deve essere usato nell’occhio, dentro la bocca o il naso, o sui genitali. I pazienti devono essere istruiti per evitare l’applicazione di altri prodotti topici alla zona interessata durante l’utilizzo di Zovirax Cream.
Non utilizzare se siete allergici a Zovirax Cream o uno qualsiasi degli ingredienti in Zovirax Cream. Prima di usare Zovirax Cream, informi il medico se è incinta, sta pianificando una gravidanza o sta allattando.
Istruzioni per l’uso
Il trattamento deve essere iniziato al primo segno o sintomo di recidiva. Istruire i pazienti a lavarsi le mani prima dell’applicazione e assicurarsi che il viso e/o le labbra siano puliti e asciutti. Consigliare ai pazienti di applicare Zovirax Cream topicamente 5 volte al giorno per 4 giorni. Istruire i pazienti di applicare topicamente una quantità di Zovirax Cream sufficiente a coprire l’area interessata, compreso il margine esterno. Consigliare ai pazienti di evitare lo sfregamento non necessario dell’area interessata per evitare di aggravare o trasferire l’infezione. Istruire i pazienti a lavarsi le mani con acqua e sapone dopo aver usato Zovirax Cream. Tenere fuori dalla portata dei bambini.
Possibili effetti collaterali
Comuni effetti collaterali relativi alla pelle che si sono verificati quando Zovirax Cream è stato applicato includono reazioni al sito di applicazione. Zovirax Cream ha il potenziale di irritazione e sensibilizzazione da contatto.
Distribuito da: Bausch Health US, LLC
Bridgewater, NJ 08807 USA
Prodotto da: Bausch Health Companies Inc.
Laval, Quebec H7L 4A8, Canada
Zovirax è un marchio registrato del gruppo di società GlaxoSmithKline e utilizzato su licenza da Bausch Health.
© 2020 Bausch Health Companies Inc. o sue affiliate
9462203
INFORMAZIONE PER I PAZIENTIZOVIRAX (zho-vahy-rex)(aciclovir)Crema
Informazioni importanti: Zovirax Cream è solo per l’uso su herpes labiale sulle labbra e intorno alla bocca. Zovirax Cream non deve essere usato nei vostri occhi, bocca, naso o sui vostri genitali.
Che cosa è Zovirax Cream?
– Zovirax Cream è un farmaco di prescrizione utilizzato per il trattamento di herpes labialis che sono ricorrenti negli adulti e nei bambini 12 anni di età e più anziani, e che hanno un sistema immunitario normale. – Zovirax Cream non è una cura per l’herpes labiale.
Non è noto se Zovirax Crema è sicuro ed efficace nei bambini di età inferiore ai 12 anni.
Non usi Zovirax Crema se è allergico all’aciclovir, al valaciclovir o a uno qualsiasi degli ingredienti di Zovirax Crema. Vedere la fine di questo foglio per un elenco completo degli ingredienti in Zovirax Cream.
Cosa devo dire al mio fornitore di assistenza sanitaria prima di usare Zovirax Cream?
Prima di usare Zovirax Cream, informi il suo fornitore di assistenza sanitaria di tutte le sue condizioni mediche, compreso se lei:
– si ammala molto facilmente (ha un sistema immunitario debole). – sei incinta o hai intenzione di rimanere incinta. Non è noto se Zovirax Cream danneggia il vostro bambino non ancora nato. – stanno allattando o hanno intenzione di allattare al seno. Non è noto se Zovirax Cream passa nel latte materno. Parlate con il vostro fornitore di assistenza sanitaria circa il modo migliore per alimentare il vostro bambino se si utilizza Zovirax Cream.
Informi il suo fornitore di assistenza sanitaria di tutti i farmaci che prende, compresi i farmaci da prescrizione e over-the-counter, vitamine e integratori a base di erbe.
Come devo usare Zovirax Cream?
– Utilizzi Zovirax Cream esattamente come il suo fornitore di assistenza sanitaria le dice di usarlo. – Usa Zovirax Cream appena hai i primi sintomi di un mal di freddo come prurito, rossore, bruciore o formicolio, o quando il mal di freddo appare. – Lavarsi le mani con acqua e sapone prima e dopo l’applicazione di Zovirax Cream. – L’area interessata deve essere pulita e asciutta prima di applicare Zovirax Cream. – Applicare Zovirax Cream alla zona interessata 5 volte al giorno per 4 giorni, compreso il bordo esterno. – Non si deve applicare altri prodotti per la pelle alla zona interessata durante il trattamento con Zovirax Cream. – Evitare lo sfregamento non necessario del mal di freddo perché questo può causare il mal di freddo per diffondere ad altre aree intorno alla bocca o rendere il mal di freddo peggio.
Quali sono i possibili effetti collaterali di Zovirax Cream?
Gli effetti collaterali più comuni di Zovirax Cream sono reazioni cutanee al sito di trattamento e possono includere: labbra secche o screpolate, desquamazione, desquamazione o secchezza della pelle, una sensazione di bruciore o bruciore e prurito.
Questi non sono tutti i possibili effetti collaterali di Zovirax Cream. Chiamate il vostro medico per una consulenza medica sugli effetti collaterali. È possibile segnalare gli effetti collaterali a FDA a 1-800-FDA-1088.
Come devo conservare Zovirax Cream?
– Conservare Zovirax Cream a temperatura ambiente tra 68 ° a 77 ° F (20 ° a 25 ° C).
Tenere Zovirax Cream e tutti i medicinali fuori dalla portata dei bambini.
Informazioni generali sull’uso sicuro ed efficace di Zovirax Cream.
I medicinali sono talvolta prescritti per scopi diversi da quelli elencati in un foglio informativo per il paziente. Non usi Zovirax Cream per una condizione per cui non è stato prescritto. Non dia Zovirax Cream ad altre persone, anche se hanno gli stessi sintomi che ha lei. Potrebbe danneggiarli. Potete chiedere al vostro farmacista o fornitore di assistenza sanitaria per informazioni su Zovirax Cream che è scritto per i professionisti della salute.
Quali sono gli ingredienti in Zovirax Cream?
Ingrediente attivo: aciclovir
Ingredienti non attivi: alcool cetostearilico, olio minerale, poloxamer 407, glicole propilenico, sodio laurilsolfato, acqua e petrolato bianco
Distribuito da: Bausch Health US, LLC
Bridgewater, NJ 08807 USA
Prodotto da: Bausch Health Companies Inc.
Laval, Quebec H7L 4A8, Canada
Zovirax è un marchio registrato del gruppo GlaxoSmithKline utilizzato su licenza da Bausch Health.
© 2020 Bausch Health Companies Inc. o sue affiliate
Per ulteriori informazioni, chiamare il numero 1-800-321-4576.
Questa informazione per il paziente è stata approvata dalla Food and Drug Administration statunitense.
Rivisto: 12/2020
9462203
Pannello espositivo principale – Tubo da 5 g in cartone
ZOVIRAX®
(ACYCLOVIR) CREMA 5%
NDC 0187-0994-45
Peso netto. 5 g
Ogni grammo contiene:
50 mg di aciclovir, alcool cetostearilico, olio minerale, poloxamer 407, glicole propilenico, laurilsolfato di sodio, acqua e petrolato bianco.
Ortho Dermatologics
Rx only
| ZOVIRAX aciclovir crema |
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
Etichettatore – Bausch Health US, LLC (831922468)
| Establishment | |||
| Name | Address | ID/FEI | Operations |
| Bausch Health Companies Inc. | 245141858 | MANUFACTURE(0187-0994) | |
Più informazioni su Zovirax Cream (aciclovir topico)
- Effetti collaterali
- Durante la gravidanza o l’allattamento
- Informazioni sul dosaggio
- Interazioni farmacologiche
- Prezzi & Buoni sconto
- 39 recensioni
- Classe del farmaco: antivirali topici
Risorse per i consumatori
- Informazioni per i pazienti
Risorse per i professionisti
- Informazioni sulla prescrizione
- Unguento Aciclovir (FDA)
Altre formulazioni
- Zovirax
- Zovirax unguento
Guide correlate al trattamento
- Herpes Simplex
- Febbrezza da freddo
Discorso medico