Introduzione
La pericardite costrittiva (CP) è una malattia sempre più riconosciuta con varie cause, caratterizzata da una fibrosi ispessita. A volte, un pericardio calcificato è visto con l’incapsulamento del cuore impedendo il riempimento diastolico. Una diagnosi corretta è difficile da stabilire solo su basi cliniche; la diagnosi provvisoria deve essere confermata da un’imaging multimodale non invasivo che include l’ecocardiografia bidimensionale (2D) e Doppler come tecnica di prima scelta, che può essere integrata dalla tomografia computerizzata (CT) e dalla risonanza magnetica (MRI) in casi selezionati. Le misurazioni emodinamiche invasive diventano utili quando l’imaging non fornisce informazioni diagnostiche adeguate o richiede un’ulteriore caratterizzazione. La cardiomiopatia restrittiva (RCM) è una malattia con varie cause che colpisce la funzione miocardica o per disfunzione primaria dei miociti e/o per infiltrazione extracellulare o fibrosi. Entrambe le condizioni, CP e RCM, portano a un’insufficienza cardiaca diastolica con un riempimento ventricolare anormale e caratteristiche cliniche simili. La differenziazione accurata della CP dalla RCM può essere una sfida diagnostica anche per il clinico esperto, ma è di fondamentale importanza, poiché la CP è una malattia potenzialmente curabile, mentre nella RCM la prognosi è scarsa a causa delle limitate opzioni terapeutiche. Tuttavia, i recenti progressi nell’ecocardiografia e in altre modalità di imaging hanno reso questo compito precedentemente impegnativo molto più facile.
Patofisiologia
Il guscio fibrotico intorno al cuore nella CP influenza l’emodinamica cardiaca in due modi diversi. In primo luogo, c’è una dissociazione tra le pressioni intratoraciche e intracardiache. Di solito, il gradiente di pressione di riempimento del LV (la differenza tra la pressione del cuneo capillare polmonare e la pressione diastolica del LV) rimane costante durante il ciclo respiratorio. Nella CP, la riduzione inspiratoria della pressione intratoracica viene trasmessa alle vene polmonari extracardiache, ma non completamente all’atrio sinistro incassato e al ventricolo, portando a una riduzione del riempimento diastolico del LV con l’ispirazione. In secondo luogo, poiché il volume ematico totale di tutte e quattro le camere cardiache rimane relativamente costante, l’interdipendenza ventricolare è esagerata nella CP. Con la diminuzione inspiratoria in riempimento LV e volume diastolico, riempimento ventricolare destro è aumentato in modo compensatorio. Poiché la vena cava superiore, ma non quella inferiore, è soggetta a variazioni della pressione intratoracica, la maggior parte del flusso verso l’atrio destro ad alta pressione durante l’inspirazione arriva dalla vena cava inferiore che è anche assistita da una maggiore pressione inspiratoria transaddominale. Questo spiega fisiologicamente l’aumento paradossale della pressione venosa giugulare durante l’ispirazione (segno di Kussmaul). Con l’espirazione, si verificano cambiamenti opposti nel riempimento del cuore destro e sinistro. Al contrario, la compliance pericardica è normale nella RCM e la variazione respiratoria delle pressioni intratoraciche viene trasmessa normalmente alle camere cardiache. Con l’inspirazione, la pressione del cuneo capillare polmonare e la pressione diastolica del LV si abbassano allo stesso modo, lasciando così il gradiente di pressione per il riempimento del LV quasi invariato.
Interdipendenza ventricolare
Hatle et al hanno fornito informazioni sulle variazioni respiratorie dinamiche nel riempimento ventricolare e nelle pressioni che si verificano nei pazienti con RCM. Il concetto di interdipendenza ventricolare e i cambiamenti reciproci di pressione respiratoria nel RV e LV al cateterismo cardiaco costituiscono un utile parametro diagnostico. Nei pazienti con CP, di solito c’è un aumento della pressione sistolica del RV durante il picco di ispirazione, un momento in cui la pressione sistolica del LV è più bassa. Al contrario, c’è una diminuzione concordante delle pressioni sistoliche di RV e LV durante il picco di ispirazione nei pazienti con RCM. Interdipendenza ventricolare in CP può anche essere valutato da ecocardiografia Doppler con la curva di velocità di rigurgito tricuspide. Durante l’inspirazione, la pressione sistolica RV aumenta, così come la durata della sistole RV perché è necessario più tempo per espellere un volume RV aumentato.
Ecocardiografia bidimensionale
Lo spessore normale del pericardio è di 2 mm o meno. Un pericardio rigido e/o ispessito è il substrato anatomico responsabile della fisiologia costrittiva. Nonostante i rapporti isolati sull’utilità dell’ecocardiografia M-mode e 2D nel rilevare il pericardio ispessito, l’affidabilità dell’ecocardiografia transtoracica per questo scopo è discutibile a causa delle limitazioni tecniche, come la posizione del trasduttore, il guadagno, le impostazioni della scala di grigio e i riverberi. Inoltre, il CP può essere prevalentemente localizzato in una regione del cuore. La risoluzione superiore raggiunta con l’ecocardiografia transoesofagea permette una migliore definizione del pericardio. Anche la risonanza magnetica e la tomografia computerizzata permettono di misurare accuratamente lo spessore del pericardio. Tuttavia, le informazioni anatomiche non riflettono necessariamente le anomalie fisiopatologiche. Inoltre, la CP e il pericardio ispessito non sono uniformemente associati, perché i pazienti possono avere una CP provata chirurgicamente nonostante uno spessore pericardico normale. Al contrario, il pericardio ispessito può essere presente senza caratteristiche costrittive, soprattutto in pazienti che hanno avuto una radioterapia toracica o un intervento chirurgico a cuore aperto.
La funzione sistolica miocardica valutata dalla frazione di eiezione del LV è conservata nella CP. Il movimento del setto interventricolare respirofasico osservato nell’ecocardiografia M-mode e 2D è indotto da brusche variazioni di volume ventricolare ed è un riflesso della maggiore interdipendenza ventricolare. Con un minore riempimento del ventricolo durante la prima inspirazione, il setto interventricolare si sposta improvvisamente a sinistra. Nell’espirazione, il LV si riempie meglio e il setto ritorna in una posizione normale. Inoltre, c’è spesso un discreto “shudder” settale con ogni battito indipendente dalla respirazione a causa dei tassi di riempimento differenziale di entrambi i ventricoli in diastole. L’allargamento biatriale e la congestione venosa sistemica (pletora della vena cava inferiore) sono risultati non specifici, perché si incontrano sia nella CP che nella RCM.
Ecocardiografia Doppler a onde pulsate
Perché la pressione diastolica del LV è elevata e praticamente tutto il riempimento ventricolare del LV avviene nella diastole precoce, la velocità dell’onda E mitrale è aumentata e il tempo di decelerazione accorciato (di solito <160 ms) con un’onda A piccola o assente che ricorda un modello di afflusso restrittivo che si vede sia nella CP che nella RCM. Hatle et al hanno descritto per la prima volta le caratteristiche del flusso Doppler mitrale e tricuspidale che sono utilizzate per differenziare la costrizione dalla restrizione. Con l’inspirazione, la dissociazione delle pressioni intratoraciche e intracardiache si traduce in una diminuzione della pressione iniziale di guida per il riempimento ventricolare sinistro. Di conseguenza, c’è una diminuzione della velocità dell’onda E mitrale di picco di >25% durante il primo battito dell’ispirazione, così come il prolungamento del tempo di rilassamento isovolumico (di solito >20%). L’interdipendenza ventricolare è responsabile dei cambiamenti reciproci nel modello di afflusso trans-tricuspidale con un aumento inspiratorio della velocità dell’onda E di picco di >40%. I cambiamenti inversi si verificano con l’espirazione in entrambi i ventricoli. Altri investigatori hanno riportato risultati caratteristici per i cambiamenti respiratori nelle vene polmonari e nelle vene epatiche. In termini semplificati, il flusso diastolico al cuore sinistro diminuisce con l’inspirazione, mentre si osservano cambiamenti opposti per il cuore destro. Tuttavia, studi successivi più grandi hanno scoperto l’assenza di variazione respiratoria dell’afflusso mitrale in un terzo dei pazienti con CP.
I risultati Doppler possono essere fuorvianti in alcuni casi. In primo luogo, nei pazienti con qualsiasi ritmo irregolare (ad esempio, la fibrillazione atriale), i cambiamenti respirofasici possono ancora essere visto, ma sono facilmente confusi dalla variazione dell’intervallo RR. In secondo luogo, una pressione atriale sinistra marcatamente elevata può smussare la variazione respiratoria della velocità E mitrale a causa di un gradiente di alta pressione persistente e del ritorno venoso al cuore sinistro. Le manovre che diminuiscono il precarico possono smascherare la caratteristica variazione Doppler respiratoria. In terzo luogo, una considerevole fluttuazione respiratoria nella pressione intratoracica, come quella vista nella broncopneumopatia cronica ostruttiva (BPCO), può imitare la variazione respiratoria nelle velocità di afflusso mitrale e tricuspide incontrata nel CP. Tuttavia, il rapporto E/A è più basso, il tempo di decelerazione è più prolungato e l’interrogazione Doppler della vena cava superiore mostra un marcato aumento del flusso sistolico inspiratorio in avanti, che non è visto nei pazienti con CP.
Tissue Doppler e imaging di deformazione miocardica
L’ecocardiografia 2D di base mostra spesso un anulus mitrale iperdinamico con movimento esagerato nei pazienti con CP. Questo fenomeno può essere riconosciuto a occhio nudo su immagini in scala di grigi, ma è meglio apprezzato dall’imaging Doppler del tessuto. In generale, una velocità anulare mitrale e ‘³8 cm / s rappresenta un punto di taglio discreto ampiezza per distinguere CP da RCM, forse a causa di un maggiore contributo da parte del movimento longitudinale del ventricolo sinistro per il riempimento diastolico e normale rilassamento LV. Inoltre, a causa della legatura del pericardio adiacente fibrotico e cicatrizzato, che influenza la traslocazione laterale dell’anulus mitrale nei pazienti con CP, la velocità e’ laterale è inferiore alla velocità e’ mediale, un fenomeno chiamato anulus reversus, che è presente fino al 75% del CP chirurgicamente provato.
Per lo stesso motivo, la marcata disfunzione epicardica nella CP porta alla compromissione dell’accorciamento circonferenziale (chiamato anche strain), e della meccanica della torsione, mentre la deformazione subendocardica del miocardio (strain longitudinale) è ben conservata nella CP, ma significativamente ridotta nella RCM, interessando prevalentemente le fibre subendocardiche orientate in direzione longitudinale. Questi due modelli distinti nella meccanica longitudinale e circonferenziale del LV sono facilmente valutabili dal 2D speckle tracking, una tecnica relativamente indipendente dall’angolo che traccia le caratteristiche uniche intramiocardiche nelle immagini B-mode in scala di grigi, denominate speckles.
C’è una relazione inversa tra il rapporto tra le prime velocità transmitrali e anulari (E/e’) e le pressioni di riempimento del LV (l’annulus paradoxus e il rapporto E/e’ non dovrebbero essere usati per stimare le pressioni di riempimento del LV nei pazienti con CP). La spiegazione plausibile per questo risultato è il movimento longitudinale esagerato dell’anulus mitrale, nonostante le alte pressioni di riempimento. Come misura secondaria, colore M-mode propagazione del flusso di riempimento del LV può aiutare nella diagnosi differenziale tra CP e RCM. La velocità di afflusso del primo aliasing è di solito normale o marcatamente aumentata (di solito >100 cm/s) in CP, ma significativamente inferiore in RCM.
La fibrillazione atriale è una complicazione di entrambi CP e RCM e rende la valutazione dei cambiamenti respiratori dinamici da ecocardiografia Doppler difficile. La variazione della velocità del flusso mitrale è legata più alla lunghezza del ciclo cardiaco che alla fase respiratoria, ma nelle vene epatiche le inversioni diastoliche del flusso rimangono prominenti durante l’espirazione. Anche le velocità anulari mitrali misurate dal Doppler tissutale rimangono un parametro affidabile.
Recentemente, è stato proposto un algoritmo multiforme con cinque risultati ecocardiografici chiave, tra cui il movimento del setto ventricolare legato alla respirazione, il modello di afflusso mitrale, la velocità anulare mitrale mediale (settale) e’, e l’inversione del flusso diastolico espiratorio della vena epatica, che è applicabile anche ai pazienti in fibrillazione atriale. Le caratteristiche ecocardiografiche chiave sono elencate nella Tabella 1 e i tipici risultati Doppler sono visualizzati nella Figura 1.
Tabella 1. Caratteristiche ecocardiografiche chiave della pericardite costrittiva.
- Spostamento del setto ventricolare (chiamato anche rimbalzo del setto)
- Incremento della velocità dell’onda E mitrale e del rapporto E/A >1.6 (in espirazione)
- Variazione respiratoria del picco dell’onda E(almeno >15%)
- Prominente inversione del flusso diastolico espiratorio nelle vene epatiche
- Velocità diastolica iniziale (e’) dell’anulus mitrale mediale conservata o esagerata (³9 cm/s)
- E’ mediale uguale o maggiore della velocità e’ dell’anulus mitrale laterale (annulus reversus)
- Deformazione miocardica circonferenziale limitata e longitudinale conservata (strain)
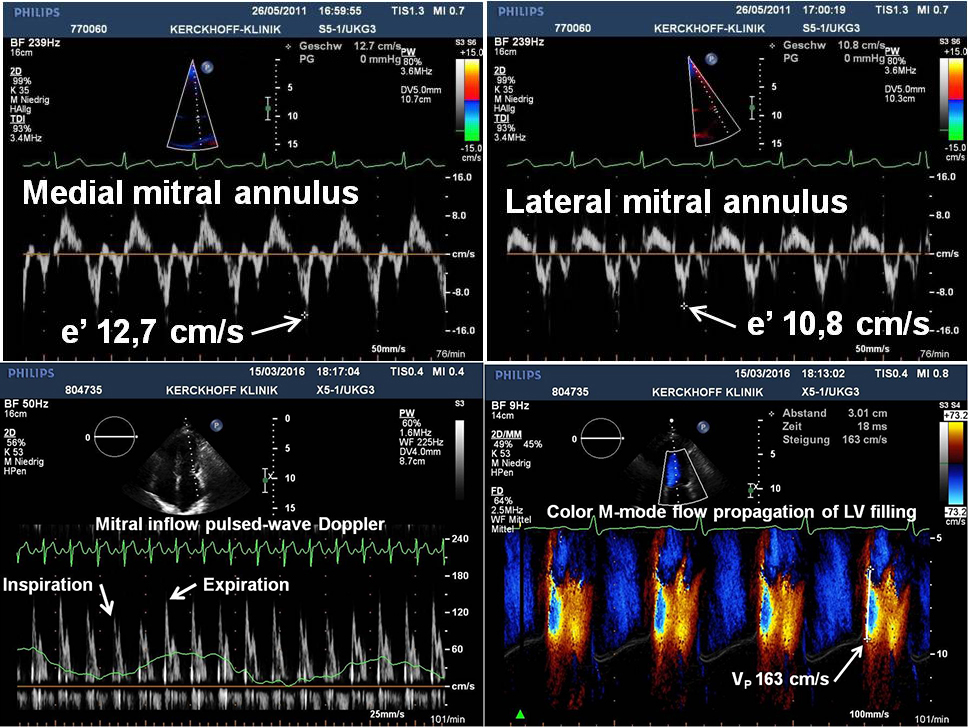
Figura 1. Risultati tipici Doppler da un paziente con pericardite costrittiva chirurgicamente provata. Le velocità diastolica precoce (e’) dell’anulus mitrale mediale (in alto a sinistra) e laterale (in alto a destra) mediante Doppler tissutale mostrano una funzione longitudinale conservata e l’inversione del rapporto usuale (il cosiddetto annulus reversus). Lo spettro Doppler a onde pulsate delle velocità di afflusso mitrale (in basso a sinistra) dimostra una marcata variazione respiratoria della velocità dell’onda E di picco. La propagazione del flusso M-mode Doppler a colori del riempimento del ventricolo sinistro (LV) (in basso a destra) illustra una ripida pendenza (163 cm/s) del primo contorno di velocità di aliasing (linea bianca).
Incertezze diagnostiche: costrizione e restrizione mista
Dopo la radioterapia toracica, possono svilupparsi CP, RCM, malattia valvolare, malattia coronarica prematura o una loro combinazione. Queste caratteristiche sovrapposte rappresentano un’altra sfida nella diagnosi differenziale tra CP e RCM e rendono necessario determinare se le anomalie sono causate dalla costrizione pericardica, dalla restrizione miocardica o da entrambe. Se è presente una concomitante malattia pericardica e miocardica, la decisione di procedere con la pericardiectomia dipende dal grado in cui il pericardio anormale contribuisce all’aumento delle pressioni intracardiache.
Direzioni future
Le tecniche di imaging cardiaco attualmente disponibili hanno la capacità di generare una grande quantità di dati strutturali e funzionali cardiaci, di cui solo una frazione viene utilizzata dal medico interpretante per stabilire una diagnosi e prendere una decisione clinica. Una soluzione potenziale per affrontare questa sfida è quella di applicare un approccio cognitivo di apprendimento automatico per aiutare nella differenziazione di CP da RCM.
Conclusioni
CP è caratterizzato dall’incapsulamento del cuore da un pericardio rigido non flessibile con conseguente compromissione del riempimento diastolico. La comprensione delle anomalie fisiopatologiche caratterizzate dalla dissociazione tra pressione intratoracica e intracardiaca e un’esagerata interdipendenza ventricolare è fondamentale per la diagnosi accurata e la differenziazione dalla RCM. L’ecocardiografia sarebbe considerata la modalità diagnostica di prima linea e lo spostamento del setto ventricolare legato alla respirazione un punto di partenza altamente sensibile. Un movimento anulare mitrale conservato o addirittura accelerato in un paziente con sintomi di insufficienza cardiaca, nonché l’inversione del rapporto tra le velocità Doppler tessuto anulare laterale a mediale (chiamato anche anulus reversus) dovrebbe avvisare il clinico interpretante per la diagnosi di CP. Doppler convenzionale a onde pulsate della velocità di flusso mitrale diastolica di picco iniziale spesso dimostra una marcata diminuzione inspiratoria. Anche se questi risultati Doppler sono di solito diagnostici, entrambi i risultati falsi positivi e falsi negativi esistono, e nessun singolo parametro ecocardiografico dovrebbe essere utilizzato esclusivamente a favore di un approccio multiforme. Inoltre, l’imaging multimodale con CT e CMR può aiutare a delineare lo spessore del pericardio, anche se non dimostrano un significato fisiologico, e un aumento dello spessore pericardico non è una caratteristica diagnostica essenziale della CP. Quando uno studio ecocardiografico transtoracico completo è diagnostico per la costrizione, non dovrebbero essere necessari ulteriori test diagnostici. Nei casi equivoci, in cui la valutazione non invasiva è inconcludente o discordante con i risultati clinici, dovrebbe essere eseguita una valutazione emodinamica mediante cateterizzazione cardiaca.