(CNN) Se sei abbastanza sfortunato da avere un serpente velenoso che affonda le sue zanne in te, la tua migliore speranza è un antiveleno, che è stato fatto nello stesso modo dai tempi vittoriani.
Si tratta di mungere a mano il veleno del serpente e di iniettarlo in cavalli o altri animali in piccole dosi per evocare una risposta immunitaria. Il sangue dell’animale viene prelevato e purificato per ottenere anticorpi che agiscono contro il veleno.
Produrre l’antiveleno in questo modo può diventare disordinato, per non dire pericoloso. Il processo è soggetto a errori, laborioso e il siero finito può provocare gravi effetti collaterali.
Gli esperti hanno a lungo chiesto modi migliori per trattare i morsi di serpente, che uccidono circa 200 persone al giorno.
Ora – finalmente – gli scienziati stanno applicando la ricerca sulle cellule staminali e la mappatura del genoma a questo campo di ricerca a lungo ignorato. Sperano di portare la produzione di antiveleno nel 21° secolo e in definitiva salvare migliaia, se non centinaia di migliaia, di vite ogni anno.
Ricercatori nei Paesi Bassi hanno creato in laboratorio ghiandole produttrici di veleno dal Cape Coral Snake e da altre otto specie di serpenti, usando cellule staminali. Le tossine prodotte dalle repliche in miniatura 3-D delle ghiandole del serpente sono tutte ma identiche al veleno del serpente, il team ha annunciato giovedì.
In una svolta parallela, gli scienziati in India hanno sequenziato il genoma del cobra indiano, uno dei “quattro grandi” serpenti del paese che sono responsabili della maggior parte dei 50.000 morsi di serpente che l’India vede ogni anno.
“Hanno davvero spostato il gioco”, ha detto Nick Cammack, capo del team sui morsi di serpente presso l’ente benefico britannico di ricerca medica Wellcome. “
Dal cancro al veleno di serpente
Hans Clevers, il ricercatore principale dell’Hubrecht Institute for Developmental Biology and Stem Cell Research di Utrecht, non si sarebbe mai aspettato di usare il suo laboratorio per produrre veleno di serpente.
Un decennio fa, ha inventato la tecnica per fare organoidi umani – organi in miniatura fatti dalle cellule staminali di singoli pazienti. Hanno permesso ai medici di testare gli effetti specifici dei farmaci in modo sicuro fuori dal corpo, qualcosa che ha rivoluzionato e personalizzato aree come il trattamento del cancro.
 Gli scienziati hanno riprodotto la ghiandola del veleno del serpente corallo del Capo, visto qui nello zoo di Olomouc, Repubblica Ceca, l’11 maggio 2018.
Gli scienziati hanno riprodotto la ghiandola del veleno del serpente corallo del Capo, visto qui nello zoo di Olomouc, Repubblica Ceca, l’11 maggio 2018. Perché dunque ha deciso di coltivare la ghiandola del veleno di un serpente?
Clevers ha detto che è stato essenzialmente un capriccio di tre studenti di dottorato che lavorano nel suo laboratorio che si erano annoiati di riprodurre reni, fegati e budella di topi e umani. “Penso che si siano seduti e si siano chiesti qual è l’animale più iconico che possiamo coltivare? Non l’uomo o il topo. Hanno detto che deve essere il serpente. La ghiandola del veleno del serpente”.
“Hanno supposto che i serpenti avessero cellule staminali nello stesso modo in cui i topi e gli esseri umani hanno cellule staminali, ma nessuno aveva mai indagato su questo”, ha detto Clevers.
Dopo aver trovato alcune uova di serpente fecondate da un rivenditore, i ricercatori hanno scoperto che erano in grado di prendere un piccolo pezzo di tessuto di serpente, contenente cellule staminali, e nutrirlo in un piatto con lo stesso fattore di crescita che hanno usato per gli organoidi umani – anche se ad una temperatura inferiore – per creare le ghiandole del veleno. E hanno scoperto che questi organoidi di serpente – piccole sfere larghe appena un millimetro – hanno prodotto le stesse tossine del veleno di serpente.
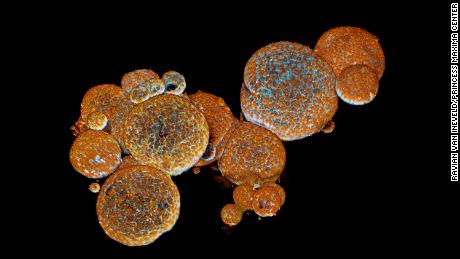 Gli organoidi delle ghiandole del veleno del serpente visti al microscopio./
Gli organoidi delle ghiandole del veleno del serpente visti al microscopio./ “Aprili e avrai molto veleno. Per quanto possiamo dire, è identico. Lo abbiamo confrontato direttamente con il veleno della stessa specie di serpente e troviamo esattamente gli stessi componenti”, ha detto Clevers, che era un autore del documento che ha pubblicato sulla rivista Cell la scorsa settimana.
Il team ha confrontato il loro veleno di laboratorio con quello reale a livello genetico e in termini di funzione, scoprendo che le cellule muscolari hanno smesso di sparare quando esposte al loro veleno sintetico.
 Un velenoso cobra dagli occhiali, noto anche come cobra indiano (Naja Naja) o cobra bianco, è visto vicino a un dipinto all’interno del suo recinto al Kamla Nehru Zoological Garden di Ahmedabad il 30 gennaio 2019.
Un velenoso cobra dagli occhiali, noto anche come cobra indiano (Naja Naja) o cobra bianco, è visto vicino a un dipinto all’interno del suo recinto al Kamla Nehru Zoological Garden di Ahmedabad il 30 gennaio 2019. Cellule e DNA, non cavalli
Gli attuali antiveleni a nostra disposizione, prodotti nei cavalli non negli esseri umani, innescano tassi relativamente alti di reazioni avverse, che possono essere lievi, come eruzione cutanea e prurito, o più gravi, come l’anafilassi. È anche roba costosa. Wellcome stima che una fiala di antiveleno costa 160 dollari, e un corso completo di solito richiede più fiale.
Anche se le persone che ne hanno bisogno possono permetterselo – la maggior parte delle vittime di morsi di serpente vivono in Asia e Africa rurale – il mondo ha meno della metà dello stock di antiveleno di cui ha bisogno, secondo Wellcome. Inoltre gli antiveleni sono stati sviluppati solo per circa il 60% dei serpenti velenosi del mondo.
In questo contesto, la nuova ricerca potrebbe avere conseguenze di vasta portata, permettendo agli scienziati di creare una biobanca di organoidi di ghiandole di serpente dalle circa 600 specie di serpenti velenosi che potrebbero essere usati per produrre quantità illimitate di veleno di serpente in un laboratorio, ha detto Clevers.
“Il prossimo passo è quello di prendere tutta questa conoscenza e iniziare a studiare nuovi antiveleni che hanno un approccio più molecolare”, ha detto Clevers.
Per creare un antiveleno, le informazioni genetiche e la tecnologia degli organoidi potrebbero essere usate per fare i componenti specifici del veleno che causano più danni – e da loro produrre anticorpi monoclonali, che imitano il sistema immunitario del corpo, per combattere il veleno, un metodo già usato nei trattamenti di immunoterapia per il cancro e altre malattie.
“È un grande nuovo modo di lavorare con il veleno in termini di sviluppo di nuovi trattamenti e di sviluppo di antiveleno. I serpenti sono molto difficili da curare”, ha detto Cammack, che non era coinvolto nella ricerca.
Clevers ha detto che il suo laboratorio ora progetta di fare organoidi di ghiandole velenifere dai 50 animali più velenosi del mondo e condivideranno questa biobanca con i ricercatori di tutto il mondo. Al momento, Clevers ha detto che sono in grado di produrre gli organoidi al ritmo di uno alla settimana.
Ma la produzione di antiveleno non è un’area in cui le aziende farmaceutiche sono state tradizionalmente desiderose di investire, ha detto Clevers
Gli attivisti spesso descrivono i morsi di serpente come una crisi sanitaria nascosta, con morsi di serpente che uccidono più persone del cancro alla prostata e del colera in tutto il mondo, ha detto Cammack.
“Non ci sono soldi nei paesi che soffrono. Non sottovalutare quante persone muoiono. Gli squali ne uccidono circa 20 all’anno. I serpenti ne uccidono 100.000 o 150.000”, ha detto Clevers.
“Sono un ricercatore sul cancro essenzialmente e sono inorridito dalla differenza di investimento nella ricerca sul cancro e questa ricerca”.
Il veleno è un cocktail complesso
Una sfida per fare l’antiveleno sintetico è la pura complessità di come un serpente disabilita la sua preda. Il suo veleno contiene diversi componenti che hanno effetti diversi.
Ricercatori in India hanno sequenziato il genoma del cobra indiano, nel tentativo di decodificare il veleno.
Pubblicato sulla rivista Nature Genetics all’inizio di questo mese, è il genoma di serpente più completo assemblato e contiene la ricetta genetica per il veleno del serpente, stabilendo il legame tra le tossine del serpente e i geni che le codificano. Non è un cocktail semplice – il team ha identificato 19 geni su 139 geni di tossine come quelli responsabili di causare danni agli esseri umani.
“È la prima volta che un serpente molto importante dal punto di vista medico è stato mappato in modo così dettagliato,” ha detto Somasekar Seshagiri, presidente della SciGenom Research Foundation, un centro di ricerca no-profit in India.
“Crea il modello del serpente e ci aiuta a ottenere le informazioni dalle ghiandole del veleno.” Successivamente, il suo team mapperà i genomi della vipera a squame, del krait comune e della vipera di Russell – il resto dei “quattro grandi” dell’India. Questo potrebbe aiutare a fare l’antiveleno dalle ghiandole in quanto sarà più facile identificare le proteine giuste.
In tandem, entrambe le scoperte renderanno anche più facile scoprire se alcune delle potenti molecole contenute nel veleno di serpente sono esse stesse degne di essere studiate come farmaci – permettendo ai serpenti di lasciare il segno sulla salute umana in un modo diverso da quello previsto dalla natura – salvando vite.
Il veleno di serpente è stato usato per produrre farmaci che trattano l’ipertensione (pressione sanguigna anormalmente alta) e condizioni cardiache come l’angina.
“Oltre ad essere spaventoso, il veleno è incredibilmente utile”, ha detto Seshagari.