Thomas A. Oetting, MS, MD
La conversione all’estrazione della cataratta extracapsulare (ECCE) arriva spesso in un momento difficile. La lente sta per cadere a sud, il vitreo è prolassato e il chirurgo è stressato. Comprendere le fasi e il processo di conversione all’ECCE è essenziale e studiare prima della crisi aiuterà a calmare lo stress quando questo processo inevitabile si verifica. Tratteremo diverse aree: identificazione dei pazienti a rischio per la necessità di conversione all’ECCE, indicazioni per la conversione, conversione da topica a sub-Tenon’s, preparazione della ferita, espressione del materiale della lente, chiusura della ferita, posizionamento della IOL, questioni post-operatorie e una breve sezione sulla vitrectomia anteriore.
Pazienti a rischio di conversione all’ECCE: Una delle parti più importanti del processo pre-operatorio per i pazienti con cataratta è quella di valutare i fattori che aumentano le difficoltà chirurgiche che possono portare alla conversione all’ECCE o complicare in altro modo la procedura. Si può decidere di passare a una ferita limbare superiore che faciliti la conversione all’ECCE piuttosto che a un’incisione corneale chiara temporale. Potreste voler fare un blocco retrobulbare piuttosto che un’anestesia topica, poiché il caso può durare più a lungo o ha maggiori probabilità di diventare complicato. In alcune situazioni, i fattori di rischio pre-operatori fanno considerare la possibilità di invitare qualcuno più esperto per eseguire il caso.
Fattori di difficoltà (in ordine decrescente di importanza)1
- Lassità zonulare (pseudoesfoliazione-PXF, storia di trauma, sindrome di Marfan, etc.)
- Lente dura come la roccia (lente rossa o nera)
- Dimensioni della pupilla (perché è piccola? PXF, diabete s/p laser, sinechia centrale posteriore – CPS, floscio da tamsulosina/Flomax)
- Non può rimanere piatta per molto tempo (es. broncopneumopatia cronica ostruttiva – COPD, claustrofobia, tremore, obesità grave)
- Grande fronte che limita l’accesso superiore
- Angolo stretto che limita lo spazio della camera anteriore (AC)
- Predisposizione allo scompenso corneale: (es. Distrofia di Fuch o guttata corneale, PPMD, nucleo duro)
- Cataratta bianca/nera con scarso riflesso rosso che rende difficile la capsuloresi curvilinea continua (CCC)
- Predisposizione all’esposizione: es: botox, trauma palpebrale passato, diabete mellito (DM)
- Anticoagulanti (es.g., warfarin/Coumadin, asparina)
- Paziente monoculare
| Fattore | Tempo | Apparecchiatura/Anestesia |
|---|---|---|
| Lassità zonali | Doppia |
|
| Lente dura come la roccia | Aggiungi il 50% |
|
| Pupilla piccola | Aggiungi 50% |
|
| Flomax | Aggiungi 50% |
|
| Riflesso rosso scarso | Aggiungi 50% |
|
| Big Brow | Aggiungi 25% |
|
| Angolo stretto | Aggiungi 25% |
|
| Predisposizione allo scompenso corneale | 0% |
|
| Bocchetta da trabeculectomia esistente | 0% |
|
| Vitrectomia precedente (PPVx) | 0% |
|
| Non può stare disteso | 0% |
|
| Anticoagulante usare | 0% |
|
| Paziente monoculare | 0% |
|
| (modificato da Oetting, Cataract Surgery for Greenhorns, http://medrounds.org/cataract-surgery-greenhorns) | ||
Indicazioni per la conversione: La conversione all’ECCE è indicata quando la facoemulsificazione sta fallendo. A volte questo è dovuto a una lente molto dura che non si sottopone agli ultrasuoni o a una lente che è abbastanza dura che il chirurgo è preoccupato che l’energia ultrasonica richiesta possa danneggiare una cornea provvisoria (per esempio la distrofia endoteliale di Fuchs o la distrofia polimorfa posteriore). A volte si convertirà all’ECCE quando una capsuloresi errante diventa radiale, specialmente con un cristallino duro, quando il chirurgo è preoccupato che il rischio di far cadere la lente sia troppo grande con la facoemulsificazione continua. Un chirurgo può scegliere di convertire all’ECCE quando la capsula anteriore è difficile da vedere e la capsuloresi deve essere completata con la tecnica dell’apriscatole (tuttavia, con l’uso del Trypan Blue stain questo è meno comunemente indicato). Più spesso la conversione è indicata quando il cristallino è allentato da zonuli deboli o da una lacerazione della capsula posteriore che rendono la facoemulsificazione meno sicura dell’estensione della ferita e della rimozione del materiale della lente residua. Le indicazioni per la conversione all’ECCE includono:
- Lente cristallino duro o endotelio instabile
- Rottura radiale nella capsula anteriore con lente dura
- Visualizzazione scarsa nonostante il colorante Trypan
- Rottura capsulare posteriore
- Dialisi zonulare
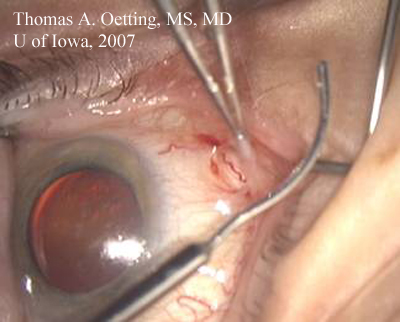
Conversione in anestesia sub-Tenon. Spesso convertiamo i casi dalla cornea chiara topica all’ECCE. Anche se l’ECCE può essere fatto sotto topica, di solito è più comodo e più sicuro dare un anestetico aggiuntivo che è tipicamente un’iniezione sotto tenone di bupivicaina e lidocaina. Questo fornirà una certa acinesia e un’anestesia aggiuntiva. Di solito c’è un’emorragia sottocongiuntivale e se l’iniezione è fatta troppo in avanti può causare chemioisi e gonfiore della congiuntiva. Le fasi dell’iniezione sottogengivale sono descritte di seguito:1
- Preparare una siringa da 3cc con parti uguali di lidocaina al 2%/0.75% di bupivacaina
- Posizionare la canula lacrimale (o la canula di Masket) con una leggera curva per approssimare quella del globo
- Scegliere un quadrante per il blocco (meglio andare per un quadrante laterale per evitare i muscoli obliqui)
- Far guardare il paziente dal quadrante scelto per aumentare l’esposizione
- Utilizzare .12 forcipe per ritrarre la congiuntiva
- Fare una piccola incisione fino alla sclera con le forbici di Wescott
- Rivolgere le forbici di Wescott con la curva verso il basso e sezionare senza mezzi termini attraverso il quadrante
- Secondare l’equatore (simile all’uso delle forbici per tenotomia Stevens in pediatria/retina)
- Usare .12 Forcipe per la controtrazione
- Posizionare la canula attraverso l’incisione e dirigere oltre l’equatore prima di iniettare
- L’anestetico locale dovrebbe fluire facilmente e causare poca chemosi — Se no, ridissezionare con le forbici di Wescott per arrivare più posteriormente
- Utilizzare 2-3 cc di miscela locale
Forza che tiene aperto il lembo posteriore della dissezione nello spazio sottotenoni. Canula lacrimale con curva dolce che approssima la curva del globo pronta per inserire l’anestetico locale.
Conversione della ferita: Il passo principale verso la conversione all’ECCE è quello di estendere la ferita esistente o chiudere e farne un’altra. L’ECCE richiede una grande incisione di 9-12 mm che viene chiusa con sutura. La decisione di estendere la ferita esistente o fare una nuova ferita dipende da diversi fattori: la posizione della ferita originale, le dimensioni del sopracciglio, la storia chirurgica passata e la possibile necessità di un intervento futuro.
| Ferita originale | Svantaggi di fare una nuova ferita per l’ECCE | Svantaggi di estendere la ferita esistente per l’ECCE |
|---|---|---|
| Temporale |
|
|
| Supero-temporale (occhio sinistro) |
|
|
| Infero-temporale (occhio destro) |
|
|
| Superiore |
|
|
Fare una nuova incisione durante la conversione è identico a quello per un ECCE pianificato. L’incisione originale viene chiusa con una sutura in nylon 10-O. Il chirurgo e il microscopio sono ruotati in quanto il chirurgo deve sedersi superiormente. I passi per fare una nuova incisione superiore sono:
- Peritomia congiuntivale di circa 170 gradi
- Uso lama 64 o mezzaluna per fare il solco limbare con una lunghezza della corda di 11 mm
- Cauterizzazione bipolare per l’emostasi
- Utilizzare il cheratomo per fare l’incisione iniziale a partire dal solco nel CA
- Estendere l’incisione iniziale a tutta la lunghezza del solco (con forbici o coltello)
- Suture di sicurezza sono preposizionate (solitamente 7-0 Vicryl)
.
Estendere un’incisione esistente può essere difficile e la tecnica è diversa per i tunnel sclerali rispetto alle incisioni corneali chiare. Tuttavia, in entrambi i casi, l’estensione originale viene portata al limbus. Nel caso di un’incisione sclerale originale, l’incisione viene portata anteriormente per unirsi al limbus su entrambe le estremità prima di estendersi lungo il limbus per una lunghezza di circa 11 mm. Nel caso di un’incisione corneale esistente, l’incisione corneale viene portata posteriormente verso il limbus prima di estendere la ferita lungo il limbus per una lunghezza della corda di circa 11 mm. Quando gli uncini dell’iride vengono utilizzati in una configurazione a diamante, la ferita può essere estesa per preservare l’uncino sub-incisionale e la grande pupilla.2
- Peritomia congiuntivale di circa 170 gradi
- Utilizzare la lama 64 o a mezzaluna su entrambi i lati della ferita esistente per fare un solco limbare con una lunghezza della corda di 11mm
- Cauterizzazione bipolare per emostasi
- Utilizzare lama a mezzaluna per portare la ferita sclerale esistente anteriormente o la ferita corneale esistente posteriormente per unire il limbus
- Estendere l’incisione iniziale per tutta la lunghezza del solco (con forbici o coltello)
- Suture di sicurezza sono preposizionate (solitamente 7-0 Vicryl)
Rimozione della lente: Si deve essere molto più attenti quando si rimuove il nucleo durante la tipica conversione all’ECCE che viene insieme alla perdita di vitreo. In primo luogo la capsula anteriore deve essere abbastanza grande da permettere al nucleo di esprimersi, il che può richiedere incisioni rilassanti in alcuni casi. Quando le zonule sono deboli o la capsula posteriore è lacerata, il cristallino non può essere espresso con un fluido o con una pressione esterna come viene spesso fatto con un ECCE pianificato con capsula/zonule intatte. Dopo la rimozione del vitreo (vedi sotto), la lente deve essere estratta con attenzione dalla camera anteriore con una pressione minima sul globo. Se la capsula posteriore e le zonule sono intatte, allora la lente può essere espressa come descritto con un ECCE pianificato.
Rimozione della lente con complesso capsulare intatto:
- Mobilizzare la lente (fisicamente con cistotomo o con idrodissezione – fare attenzione)
- Lente rimossa con ansa per lente o con tecnica di contropressione
- La ferita viene chiusa con suture di sicurezza e un’ulteriore sutura Vicryl centrale
- Il materiale corticale viene rimosso utilizzando un dispositivo I/A (automatico o manuale)
- Il dispositivo viscoelastico oftalmico (OVD)
- La lente viene posta nella camera posteriore
- La ferita viene chiusa con nylon 10-O e le suture Vicryl vengono rimosse.
- Viene rimosso ilOVD
Rimozione della lente con vitreo presente:
- Mobilizzare la lente con Viscoat canulla (punta la lente in modo che il lato della ferita sia anteriore)
- Far scivolare l’anello sotto la lente, “puntare in alto” lo strumento, rimuovere la lente
- La ferita viene chiusa con suture di sicurezza e un’ulteriore sutura centrale in vicryl
- Vitrectomia anteriore (vedi sotto)
- Il materiale corticale viene rimosso utilizzando o vitrector anteriore
- Dispositivo oftalmico viscoelastico (OVD)
- La lente viene posizionata nel solco o nel canale anteriore
- La ferita viene chiusa con 10-O nylon e le suture Vicryl vengono rimosse
- IlOVD viene rimosso
Posizionamento della IOL: La scelta della IOL con conversione ECCE dipende dal complesso capsulare residuo.3,4 La chiave per la centratura della IOL è ottenere entrambe le aptiche nello stesso posto: o entrambe nel sacco o entrambe nel solco.
- Quando la capsula posteriore è intatta dopo una conversione all’ECCE, l’apertura capsulare anteriore è di solito poco definita, il che può rendere difficile il posizionamento del sacco. Se la capsula anteriore e quindi la sacca è ben definita, allora posizionare una IOL acrilica in un unico pezzo senza piegarla direttamente e delicatamente nella sacca utilizzando la pinza Kelman.
- Quando la capsula posteriore è intatta e la capsula anteriore è poco definita, allora posizionare una IOL in 3 pezzi nel solco, come una grande IOL in silicone o la MA50 acrilica, posizionandole direttamente e dispiegate nel solco con le pinze Kelman. Assicurarsi che entrambe le aptiche siano nel solco.
- Quando la capsula posteriore è danneggiata, se è rimasta abbastanza capsula anteriore e posteriore per sostenere la IOL, definire il solco con viscoat e posizionare la IOL direttamente nel solco. Assicurarsi che entrambe le aptiche siano nel solco. Se la IOL non sembra stabile, posizionare le suture McCannel per fissare la IOL all’iride o rimuoverla e sostituirla con una AC IOL (non dimenticare di effettuare un’iridectomia posteriore con il vitrector).
- Quando la capsula è gravemente danneggiata e non può sostenere una IOL, posizionare la IOL nella camera anteriore. Utilizzare la pinza Kelman per posizionare la IOL, poi fissare la camera e utilizzare un gancio Sinskey per posizionare la IOL AC nella sua posizione finale. (non dimenticare di posizionare un’iridectomia periferica con il vitrector).
Questioni post-operatorie: La cura post-operatoria per i pazienti dopo la conversione da faco a ECCE è un po’ più complicata e si concentra sulla prevenzione dell’edema maculare cistoide (ECM) e sulla limitazione dell’astigmatismo indotto. Spesso la cura è molto simile a quella di un ECCE pianificato con circa 3 visite post-operatorie (una il giorno stesso o il giorno successivo, una settimana dopo, e una circa 5-6 settimane dopo). A seconda della quantità di astigmatismo, il paziente può richiedere diverse visite per rimuovere sequenzialmente le suture eliminando l’astigmatismo indotto.
Prima visita post-operatoria: Questa visita è spesso il pomeriggio stesso (4-6 ore dopo l’intervento) o la mattina successiva con l’obiettivo principale di controllare la IOP, cercare le perdite della ferita, ed esaminare il materiale della lente residua o il vitreo nella camera anteriore. Certamente la maggior parte delle perdite della ferita dovrebbe essere suturata, ma se l’AC non è formato la chiusura è obbligatoria. Il materiale nucleare residuo dovrebbe essere rimosso nei giorni successivi, se presente, ma il materiale corticale residuo spesso si dissolve con poca infiammazione. Ci si deve aspettare una visione scadente nel range 20/200 a causa dell’astigmatismo e dell’edema. La camera anteriore dovrebbe essere formata e tipicamente ha una cellula moderata (10-20 cellule/hpf con fascio di 0,2 mm). Se la IOP è inferiore a 10 mmHg, ricercare attentamente con un alto indice di sospetto una perdita utilizzando il test di Seidel. Se la IOP è nell’intervallo 10-29, allora tutto è probabilmente a posto, a meno che il paziente non sia un vasculopatico, nel qual caso il limite superiore di tolleranza della IOP dovrebbe essere abbassato. Se la IOP è nell’intervallo 30-39, considerare la soppressione acquosa. Se la IOP è >40, considerare la soppressione acquosa e il “rutto” o lo “spurgo” della IOP attraverso la paracentesi o un prelievo dalla camera anteriore. La IOP dovrebbe essere ricontrollata 60-90 minuti dopo per assicurare il successo del trattamento. Guardare il fundus per escludere il distacco di retina (RD) e il versamento o l’emorragia coroideale. Di solito i pazienti sono messi su prednisolone acetato 1% 1 goccia 4 volte al giorno (QID), cyclogyl 1% 1 goccia 2 volte al giorno (BID), e un antibiotico 1 goccia QID per la prossima settimana.
Visita post-operatoria alla prima settimana: La visione e la pressione dovrebbero migliorare drasticamente nei pazienti nel corso della settimana successiva dopo un caso che è stato convertito in ECCE. La visione dovrebbe essere nell’intervallo 20/100 con un miglioramento pinhole a circa 20/50. La visione è solitamente limitata dall’edema residuo e dall’astigmatismo. In uno studio dei nostri casi ECCE, abbiamo trovato circa 7,0 diottrie di cilindro alla visita di una settimana. Dovreste aspettarvi un’infiammazione molto ridotta e documentare l’assenza di RD. Cercate materiale di lenti residue nel segmento anteriore e nel polo posteriore. Potete sospendere il ciclogeno e l’antibiotico. Diminuire lentamente il prednisolone acetato (ad esempio, 1 gtt QID per altri 7 giorni, poi 1 gtt tre volte al giorno per 7 giorni, poi 1 gtt BID per 7 giorni, poi 1 gtt QD per 7 giorni), quindi interrompere. Se il paziente è a rischio di edema maculare cistoide (ECM), come è possibile con la perdita di vitreo, allora si dovrebbe mantenere il prednisolone alla frequenza più alta (ad esempio, QID) e iniziare un non steroideo (come il ketorolac topico o equivalente 1 gtt QID) fino alla prossima visita 4 -6 settimane dopo.
Visita post-operatoria alla quinta settimana: La visione dovrebbe continuare a migliorare man mano che l’astigmatismo si assesta e la cornea si libera ulteriormente. L’occhio dovrebbe essere confortevole. La visione dovrebbe essere nel range 20/80, migliorando a 20/40 con il pinhole. Nel nostro studio l’astigmatismo indotto dalle suture ECCE era di circa 5,0 diottrie all’incisione. Il segmento anteriore dovrebbe essere tranquillo e la IOP normale (a meno che il paziente non sia un “responder agli steroidi”). Considerare l’ECM come una possibilità nei pazienti in cui è stata necessaria una conversione, poiché questi casi sono spesso lunghi e possono comportare una perdita di vitreo. Valutare come indicato clinicamente dall’esame o dall’anamnesi con la tomografia a coerenza ottica (OCT) o l’angiografia con flouresceina (FFA).
A questo punto del recupero, il problema principale è il controllo astigmatico con la rimozione della sutura. Utilizzare la cheratometria, la rifrazione, la retinoscopia a strisce o la topografia per guidare la rimozione della sutura. Se la cheratometria è 45.00 @ 90, e 40.00 @ 180, allora cercate suture strette a circa 90 gradi (ore 12) che stanno causando 5 diottrie di cilindro. Si può togliere solo una sutura a 5 settimane, ma per la valutazione di 8 settimane, si potrebbe considerare la rimozione di 2 suture alla volta. Il piano è quello di rimuovere una sutura e vedere come la cornea si assesta. Quando l’astigmatismo è inferiore a circa 1,0-1,5 diottrie si dovrebbe interrompere la rimozione della sutura e correggere qualsiasi astigmatismo residuo con la rifrazione. Usare gocce antibiotiche in modo profilattico per alcuni giorni dopo ogni rimozione di sutura. Dopo questa visita dovreste considerare le seguenti scelte ad ogni visita (non perdete troppo tempo a pensare ad altre possibilità e ricordate che non tutti saranno 20/20):
- tirare un punto (cioè il cilindro all’asse del punto è maggiore di 1,0-1,5 diottrie sulla rifrazione manifesta)
- dare gli occhiali (cioè nessun punto da tirare o il cilindro è meno di 1 sulla RM)
- ottenere FFA o OCT perché si sospetta CME
Vitrectomia anteriore. La conversione in ECCE è quasi sempre accompagnata dal vitreo. A volte la conversione arriva quando la lente è troppo dura e la capsula è intatta, ma più spesso sembra che la conversione arrivi quando le zonule o la capsula rilasciano il vitreo nelle mani riluttanti del chirurgo del segmento anteriore. Tratteremo le cause e i segni del prolasso del vitreo e i principi della vitrectomia anteriore in varie situazioni.
Cause del prolasso del vitreo. Il vitreo arriva intorno alle zonule o attraverso una lacerazione della capsula posteriore. Le lacerazioni capsulari posteriori sono comunemente causate da 1) lacerazione anteriore che si estende posteriormente – la più comune, 2) lacerazione posteriore – secondaria all’ago faco o al chopper troppo profondo, 3) durante la manipolazione con lo strumento I/A, o 4) una lesione preesistente (ad esempio, cataratta polare posteriore, iatrogena da PPVx, o da trauma penetrante della lente). I problemi zonali sono spesso preesistenti (ad esempio, da trauma, PXF, o sindrome di Marfan), ma possono anche essere iatrogeni da una rotazione forzata della lente o dalla trazione della capsula durante l’I/A.
Segni di prolasso del vitreo. Il primo segno di prolasso del vitreo è la negazione. Sembra che ci sia qualcosa che non va, ma non si riesce ad individuare con precisione il problema. All’inizio si nega l’esistenza di un problema, ma presto diventa chiaro. Altri segni rivelatori del prolasso del vitreo includono 1) l’approfondimento della camera, 2) l’allargamento della pupilla, 3) il materiale della lente non più centrato, 4) le particelle della lente non arrivano più alla faco o alla I/A e 5) la lente non ruota più liberamente. Quando si sospetta un prolasso del vitreo, si dovrebbe inserire un OVD dispersivo nell’occhio prima di rimuovere l’ago faco o l’I/A e si può controllare la ferita con un Weck-Cel (o una spugna a freccia simile) per il vitreo.
Principi di base della vitrectomia anteriore. La chiave per una vitrectomia anteriore di successo è il controllo della fluidica dell’occhio. Il primo passo è chiudere la camera. Questo è spesso difficile quando ci si è convertiti a un ECCE perché la ferita è grande. Tuttavia, è necessario chiudere la ferita in modo che l’unico punto di uscita del fluido sia il dispositivo di aspirazione/taglio. Separare il dispositivo di irrigazione dal dispositivo di aspirazione/taglio in modo da creare un differenziale di pressione tale che il vitreo sia incoraggiato ad andare all’aspirazione/taglio. L’ultimo punto importante è tagliare basso e irrigare alto. Se si riesce a posizionare il dispositivo di irrigazione nella camera anteriore sopra il dispositivo di aspirazione/taglio in basso vicino al piano della capsula posteriore, il vitreo lascerà la camera anteriore.
|
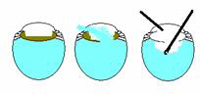 |
In generale l’altezza della bottiglia dovrebbe essere bassa – appena alta abbastanza per mantenere l’AC formato e non così alta da spingere il fluido e forse il vitreo fuori dall’occhio. La velocità di taglio dovrebbe essere la più alta possibile quando si taglia il vitreo e bassa quando si taglia il materiale della lente corticale. Discuteremo separatamente la perdita di vitreo precoce, media e tardiva in seguito.
Il vitreo si presenta all’inizio del caso – quando la maggior parte del cristallino è nell’occhio: Questo è il momento peggiore per il prolasso del vitreo e si dovrebbe considerare fortemente la conversione all’ECCE. I passi da considerare sono delineati di seguito:1
- Se topico fare iniezione sub-Tenons (come descritto sopra)
- Considerare di chiudere l’incisione temporale con 10-0 e fare incisione separata con peritomia soprattutto superiormente (come discusso sopra)
- Utilizzare viscoelastico dispersivo per sollevare lente vicino alla ferita e per spostare vitreo più posteriore.
- Può essere necessaria una vitrectomia Weck-Cel per pulire se il vitreo è molto prolassato
- Utilizzare l’ansa per rimuovere la lente (come descritto sopra)
- Avere le forbici Wescott pronte quando si tira fuori la lente per tagliare il vitreo
- Chiudere con 3 suture di sicurezza Vicryl 7-0 (una al centro e una su ogni lato a 3 mm di distanza, permettendo la rimozione della sutura centrale per posizionare la IOL da 6 mm)
- Può essere necessario aggiungere del nylon 10-0 ai bordi della ferita per essere sicuri che sia a tenuta stagna
- Vitrectomia anteriore (come discusso sopra, separare l’aspiratore/taglio dall’irrigatore)
- Rimozione a secco del materiale corticale residuo con siringa su cannula da 27 gauge
- Utilizzare la cannula J-o paracentesi se necessario per materiale sub-incisionale
- Considerare la colorazione con Kenalog (vedi sotto)
- Posizionare la IOL se possibile nel solco (regolare la potenza) o usare una AC IOL (non dimenticare l’iridotomia periferica)
- Miochol per portare la pupilla in basso-sede sul solco IOL, la pupilla picchiata aiuta a rilevare il vitreo
Vitreo che si presenta a metà caso – durante la rimozione del materiale corticale: Questo sembra essere il momento più comune per la perdita di vitreo. Spesso si otterrà la capsula posteriore proprio mentre viene prelevato l’ultimo frammento nucleare. Naturalmente non c’è motivo di convertirsi all’ECCE in questo caso. I seguenti passi sono utili:1
- Posizionare il viscoat nell’area della lacerazione o della dialisi prima di rimuovere gli strumenti
- Fare un’incisione separata di 1 o 1.5 mm di incisione per la vitrectomia anteriore
- Irrigazione separata (tramite paracentesi) e aspirazione/taglio (tramite paracenesi più grande)
- Può essere necessario suturare la ferita originale per mantenere la camera formata
- Irrigazione alta e taglio/aspirazione bassa – crea un gradiente di pressione per spingere il vitreo indietro
- Impostazioni vuoto basso 100 gamma, altezza bottiglia bassa 50 gamma, velocità di taglio massima
- Cercare di ottenere un po’ del materiale corticale residuo
- Rimozione a secco del materiale corticale residuo con siringa su cannula 27 gauge
- Utilizzare cannula J-o paracentesi se necessario per il materiale subincisionale
- Considerare la colorazione con kenalog (vedi sotto)
- Posizionare la IOL se possibile nel solco o nell’AC (se AC non dimenticare l’iridotomia periferica)
- Miochol per abbassare la pupilla
Come trattare il vitreo che si presenta tardi nel caso – durante il posizionamento della IOL: Questo è il momento meno problematico e meno comune per perdere il vitreo. Il problema principale è assicurarsi che la IOL sia stabile mentre ci si occupa del vitreo e poi fissare una IOL adeguata nel CA, nel solco o nel sacco:1
- Posizionare il viscoat nell’area della lacerazione o della dialisi prima di rimuovere gli strumenti
- Fare un’incisione separata di 1 o 1.5 mm per la vitrectomia anteriore
- Irrigazione separata (tramite paracentesi) e aspirazione/taglio (tramite paracenesi più grande)
- Può essere necessario suturare la ferita originale per mantenere la camera formata
- Irrigazione alta e taglio/aspirazione bassa – crea un gradiente di pressione per spingere il V indietro
- Impostazioni vuoto basso 100 gamma, altezza bottiglia bassa 50, velocità di taglio massima
- Se il solco può sostenere una IOL, allora
- Spostare la IOL 3 pezzi esistente nel solco
- Sostituire una IOL monopezzo esistente con-IOL in 3 pezzi nel solco
- Considerare la cattura della capsula anteriore dell’ottica se la CCC è rotonda e centrata
- Se la lacerazione della capsula posteriore è rotonda e sicura
- Posizionare il viscoat nel foro
- Mettere delicatamente la IOL in un unico pezzo nella borsa (fare molta attenzione con la lente in 3pezzo nel sacchetto)
- Miochol per abbassare la pupilla
Colorazione del vitreo con Kenalog: Scott Burk di Cincinatti Eye ha descritto l’uso di Kenalog off-label per colorare il vitreo che era prolassato nella camera anteriore5 (seguire il link al video di Facebook). Poiché il Kenalog non è approvato dalla FDA per questa indicazione e poiché alcuni chirurghi retinici hanno avuto un’endoftalmite sterile (e persino infettiva) dall’uso del Kenalog, il suo uso è controverso. Tuttavia è un’aggiunta molto utile alla vitrectomia anteriore. Il metodo per mescolare il triamcinolone (Kenalog) da diluire 10:1 e per lavare via il conservante è il seguente:
- Siringa TB per prelevare 0.2 ml di triamcinolone ben agitato (40mg/ml)
- Rimuovere l’ago e sostituirlo con un filtro per siringa da 5 (o 22) micron (Sherwood Medical)
- Forzare la sospensione attraverso il filtro e scartare il veicolo pieno di conservante
- Il Kenalog sarà intrappolato sul lato siringa del filtro
- Trasferire il filtro in una siringa da 5 ml riempita con soluzione salina bilanciata (BSS)
- Forzare delicatamente la BSS attraverso il filtro per risciacquare ulteriormente il conservante
- Ripetere il risciacquo alcune volte
- Posizionare un ago da 22 gauge sull’estremità distale del filtro
- Prelevare 2 ml di BSS nella siringa attraverso il filtro per risospendere il Kenalog
- Il Kenalog (ora senza conservante e diluito 10:1) macchierà di bianco i filamenti vitreali
- Oetting, TA, Cataract Surgery for Greenhorns, disponibile presso http://medrounds.org/cataract-surgery-greenhorns. accessed September 9, 2007
- Dupps WJ Oetting TA, Diamond iris retractor configuration for small-pupil extracapsular or intracapsular cataract surgery. J Cataract Refract Surg Vol 30(12):2473-2475.
- Chang DF, Oetting TA, Kim T, Curbside Consultations in Anterior Segment Surgery, Slack Inc, Thorofare NJ, 2007.
- Henderson BA, Essentials of Cataract Surgery, Slack Inc, Thorofare NJ, 2007.
- Burk SE, Da Mata AP, Snyder ME, Schneider S, Osher RH, Cionni RJ. Visualizzazione del vitreo utilizzando Kenalog sospensione J Cataract Refract Surg. 2003 Apr;29(4):645-51.