MIT jelent a kongenitális koszorúér-anomália?
Folyamatos vita folyik arról, hogy mi tekinthető normálisnak, és mi tekinthető koszorúér-anomáliának (CAA). Angelini szerint1 a CAA-t kizárással diagnosztizálják, ami azt jelenti, hogy azokban az esetekben, ahol a koszorúér-morfológia nem normális, a normalitás meghatározása statisztikai kritériumok alapján történik (az átlagérték plusz vagy mínusz 2 standard eltérés közötti intervallum). Így CAA lenne az a koszorúér-morfológia, amelyet az általános populáció kevesebb mint egy százalékában figyelnek meg.1,2 A CAA normális vagy kóros kardiogenezis során keletkezhet: az első esetben izolált CAA lenne az eredmény, amelyre ebben a cikkben koncentrálunk, míg a második esetben más szívfejlődési rendellenességekhez társulnának.
KLASZIFIKÁCIÓ
Más osztályozás létezik.1-3. A közelmúltban javasoltak egy újat, amely a diagnosztikai kritériumokat próbálja egységesíteni, és a CAA-t 7 kategória szerint csoportosítja4 (1. táblázat).


Nemzetközi csoportok olyan nyilvántartásokat szorgalmaznak, amelyek legalább azokat az anomáliákat tartalmazzák, amelyek a CAA-nak tulajdonított klinikai események (hirtelen halál és myocardialis ischaemia) többségét okozzák,5-7, amelyek a kontralaterális vagy “rossz” Valsalva-szinuszból erednek. Ebbe a csoportba tartoznak az egyérű koszorúerek (“hiperdominancia” a Rigatelli és munkatársai4 osztályozásában), mivel ezeknek egyetlen koszorúér-osztiumból kiindulva kell ellátniuk a szívizmot vérrel, és olyan útvonalakat kell kialakítaniuk, amelyek esetenként hasonlóak a rossz Valsalva-szinuszból kiinduló CAA-éhoz (1. ábra).

1. ábra. Koszorúér-arteriográfia bal elülső ferde vetületben, amely egyérű jobb oldali koszorúeret mutat.
INKIDENCIA
A különböző definíciók vagy osztályozások, valamint mind az angiográfiás8,9 és boncolási sorozatok10 , illetve az utóbbi években az echokardiográfiás sorozatok11 elemzése alapján a CAA bejelentett előfordulása 0,1% és 8,4% között mozog,1,8,11 így nehéz megállapítani a probléma pontos nagyságrendjét, amelyet ezek képviselnek. Összességében az incidencia meglehetősen hasonló lehet más olyan betegségekhez, amelyeket pontosabban tudtunk meghatározni, mint
a hipertrófiás kardiomiopátia (0,2%)12 vagy a Wolff-Parkinson-White-szindróma (0,1%-0,3%).13
A rossz sinusból eredő anomális koszorúerek és az egyérű koszorúerek incidenciája a koszorúér-angiográfiás vizsgálatokban 0,2% között mozog.28% és 1,74% között mozog.2,3,8,9,14-16 Tekintettel klinikai jelentőségükre, áttekintésünket ezekre az anomáliákra összpontosítjuk.
KLINIKAI ELŐZETEK
Eredetileg ezeket az anomáliákat billentyűbetegségben vagy ischaemiás szívbetegségben szenvedő betegeknél végzett koszorúér-angiográfia során diagnosztizálták, és úgy vélték, hogy nincs klinikai jelentőségük. Később kezdtek beszámolni olyan fiatal sportolók hirtelen haláláról, akiknél a betegség egyetlen jele a koszorúerekből eredő anomália volt.8,17
A klinikai spektrum a megjelenéskor változó: míg egyes betegek tünetmentesek, másoknál angina, dyspnoe, syncope, akut myocardialis infarktus, szívelégtelenség és hirtelen halál jelentkezik.1,2,5,8,17-20 Jelenleg a CAA-t tekintik a hirtelen halál második leggyakoribb okának sportolók körében az Egyesült Államokban.21
Ez azt jelenti, hogy minden CAA-t magas kockázatot jelzőnek kell tekinteni? Egyáltalán nem, de stratégiai szempontból “potenciálisan rosszindulatúnak” kell tekinteni őket, amíg további vizsgálatokat nem végeznek az anomália által kiváltott myocardialis ischaemia kizárására.
A legnagyobb gondot annak meghatározása jelenti, hogy mely CAA jelentkezhet hirtelen halállal. Ma már tudjuk, hogy azok, amelyek interarteriális (vagy intramurális) lefolyást követnek, azok, amelyekben az anomáliás koszorúér a domináns, és azok, amelyek 30 vagy 35 évnél fiatalabb betegeknél klinikai tüneteket produkálnak, azok, amelyekben a hirtelen halál előfordulása a legmagasabb.22-26
Ezért a CAA-hoz való hozzáállásunknak a beteg életkorától függően eltérőnek kell lennie. A fiatal, 35 év alattiaknál a hirtelen halál megelőzésére “koncentrálunk”, míg a 35 év felettieknél a fő cél a myocardialis ischaemia kezelése (2. ábra).
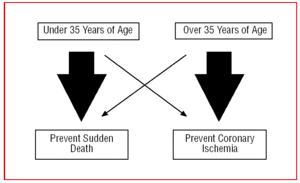
2. ábra. Eltérő megközelítés a beteg életkora szerint.
Eredetük és anomáliás lefolyásuk miatt a CAA esetenként sérülhet a billentyűcsere műtétje során, de ez előfordulhat a perkután foramen ovale zárása során is. Emiatt az ilyen típusú beavatkozások előtt ki kell zárni a CAA jelenlétét.27-30
PATHOPHYZIOLÓGIA AZ ISCHÉMIA KORONARIS ANOMALIÁBAN
Számos elmélet31 létezik a CAA-ban fellépő iszkémiát kiváltó mechanizmusok magyarázatára, de egyiket sem sikerült egyértelműen bizonyítani. Az egyikben az okot az anomáliás artéria kifejezett szögletében látják, ahol az aortából kilép. A normális koszorúérrel ellentétben, amely eredési helyén merőleges az aortára, az anomális koszorúérnek magára kell hajolnia, hogy az ellentétes Valsalva-szinuszból elérje a normális ellátási területét. Emiatt az anomális koszorúér ostiuma a normális kör alakú ostiumhoz képest kisebb lenne, szelepszerű bordákkal, és összenyomódhatna az aorta kifejezett tágulása esetén, mint amilyen például a megerőltető testmozgás során megfigyelhető.32
Egy másik elmélet a CAA kezdeti lefolyására vonatkozik. Ha interarteriális, az aorta és a tüdőartéria között van, akkor a terhelés során a két érben fellépő nyomásnövekedés az anomális koszorúér kompresszióját eredményezné.33 Továbbá, ha a kezdeti útvonal intramurális, az elzáródás fokozódhat, mivel a koszorúér a magas vérnyomás időszakában deformálódhat az aorta falán belül.34
Egyes szerzők úgy vélik, hogy az iszkémiához vezető mechanizmus az anomális koszorúérben az anomális pálya által okozott endothelkárosodás következtében görcs keletkezik,35 mások szerint pedig a CAA proximális részének az aortafalban történő intuszuszcepciója jönne létre.31
Végezetül, a tárgyalt mechanizmusok mindegyike akut vagy krónikus iszkémiát (kisebb iszkémiás eseményeket) okozhat, amelyek szívizomfibrózist idéznek elő, ami viszont a halálos aritmiák kialakulásának oka lehet.36
HOGYAN DIAGNOSZTIK A KORONARIA ANOMALIÁT?
A diagnózis felállításához magas gyanúindexre van szükség, és bizonyos körülmények között meg kell állapítani a jelenlétét. Mint fentebb említettük, a legtöbb CAA-t véletlenszerűen fedezik fel a szívbillentyűcsere műtétjét megelőzően ischaemiás szívbetegségben vagy billentyűbetegségben szenvedő betegeknél végzett koszorúér-angiográfia során, akiket e vizsgálatnak vetnek alá.
A legnagyobb diagnosztikai kihívást azok a fiatalok jelentik, akiknél nincsenek koszorúér-kockázati tényezők vagy társuló billentyűbetegség. CAA-ra kell gyanakodnunk terheléses syncope, dyspnoe vagy anginára utaló mellkasi fájdalom esetén.24,26,35 Nyilvánvaló, hogy az első diagnosztikus vizsgálat, amelyet mindannyian elvégezünk, a standard ergometria. Ez azonban nem bizonyult túl hasznosnak az ilyen típusú betegeknél, mivel általában negatív, ami arra utal, hogy a CAA okozta iszkémia csak alkalmanként jelentkezik.35,36
Ezért, mivel a “funkcionális” tesztek nem sokat segítenek, képalkotó vizsgálatot kell választanunk, amely lehetővé teszi a koszorúerek anatómiájának vizsgálatát. A kezdetben ajánlott noninvazív vizsgálat a transthoracalis echokardiográfia (TTE).7,26,37-40 E betegek többségénél az egyszerű TTE elvégzése parasternalis rövidtengelyű vetületben, az aorta gyökér síkjában lehetővé teszi a két koszorúér-ostia megkülönböztetését, sőt a CAA kezdeti lefolyásának meghatározását is. Pellicia és munkatársai 1360 élsportolót vizsgáltak echokardiográfiával, és az esetek 97%-ában a bal fő koszorúér ostiumát és proximális szakaszát, 80%-ában pedig a jobb fő koszorúeret tették láthatóvá.41
A közelmúltban Frommelt és munkatársai34 echokardiográfiát végeztek minden olyan gyermek és serdülő (életkoruk 3 hónap és 20 év között) esetében, akiket szívizom iszkémia tüneteivel, veleszületett szívbetegség gyanújával vagy mozgásszervi fájdalommal utaltak be kórházukba (1997-2002). Mindannyian hagyományos TTE-n estek át, a véráramlás irányának meghatározására szolgáló színes Doppler-áramlástérkép segítségével. 10 olyan beteget azonosítottak, akiknél a koszorúér anomális eredete a rossz sinusban volt (6 betegnél a bal koszorúér a jobb sinus Valsalva-ból, 4 betegnél pedig a jobb koszorúér a bal sinus Valsalva-ból eredt). Színes Doppler-technikával végzett TTE-vel kilenc betegnél az aorta falán belüli intramurális, a fennmaradó betegnél pedig intramyocardialis lefolyást figyeltek meg. Ha a rossz sinusból kiinduló CAA lefolyása intramurális, úgy tűnhet, mintha a normál ostiumból lépne ki. Ezért a szerzők a színes Doppler alkalmazását javasolják az áramlási irány meghatározására, ha ki kell zárni az anomália jelenlétét.
Az echokardiográfiás képalkotó technikák fejlődése lehetővé teszi, hogy a betegek bizonyos csoportjaiban meghatározzuk a CAA eredetét és kövessük a kezdeti lefolyását. Gyermekeken, serdülőkön és élsportolókon végeztek vizsgálatokat, de a normál felnőtt populációt érintő nagy sorozatokat még nem vizsgálták. Ezért az ilyen tünetegyüttesben szenvedő fiatal betegeknél a koszorúér-ostiumok azonosítását szisztematikusan el kell végezni a TTE-vizsgálat során.7,26
A rossz echokardiográfiás ablakkal rendelkező betegeknél, vagy ha a klinikai indikációk ellenére továbbra is fennáll a diagnosztikus kétség, a CAA eredetének és kezdeti lefolyásának láthatóvá tétele érdekében transoesophagealis echokardiográfia (TEE),7,26,42,43 komputertomográfia (CT)26,44-46–elektronnyalábbal vagy többszögesen–(3. ábra) vagy szívmágneses rezonanciás képalkotás (CMRI)26,47,48 végezhető (4. ábra).

3. ábra. Multidetektoros komputertomográfiás felvétel, melyen a jobb koszorúérből (CD) kiinduló, retroaortás irányt követve a circumflex koszorúér (Cx) látható, hogy normál elosztási területére érkezzen. Ao az aortát jelöli; AP a tüdőartériát. Dr. Gabriel C. Fernández, Servicio de Radiología, Hospital Povisa, Vigo, Spanyolország, jóvoltából.
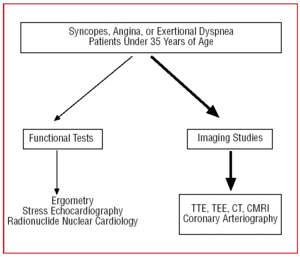
4. ábra. A 35 év alatti, koszorúér-anomáliára gyanús betegeknél javasolt diagnosztikai protokoll. A CMRI a szív mágneses rezonanciás képalkotását jelöli; CT, komputertomográfia; TEE, transoesophagealis echokardiográfia; TTE, transthoracalis echokardiográfia.
Melyik technikát és milyen sorrendben alkalmazzuk? Erre a kérdésre minden orvoscsoportnak a rendelkezésre álló technikáknak és tapasztalatának megfelelően kell válaszolnia. Azt kell tennünk, hogy a CAA-t és annak kezdeti lefolyását a rendelkezésünkre álló legkevésbé invazív technikával azonosítjuk. Bár a TEE-t már alkalmazták néhány CAA diagnózisában és kezdeti lefolyásának azonosításában, úgy véljük, hogy félig invazív jellege miatt csak más technikák sikertelensége után szabad alkalmazni. Napjainkban, az egyre szélesebb körű hozzáférhetőségnek és a kiváló háromdimenziós képalkotásnak köszönhetően bölcs döntésnek tűnik a multidetektoros CT (5. ábra) vagy a CMRI alkalmazása.49,50 A standard koszorúér-arteriográfia akkor javallott, ha a többi vizsgálat nem vezet végleges diagnózishoz. E tekintetben a 2005 áprilisában közzétett 36. Bethesda Konferencia51 a kardiovaszkuláris anomáliákkal küzdő versenysportolók kiválasztására vonatkozó ajánlása: “A koszorúér-anomáliákat meg kell fontolni olyan sportolóknál, akiknél terheléses ájulás vagy tüneteket okozó kamrai ritmuszavar fordul elő, és megfelelő vizsgálatokkal, például echokardiográfiával, CMR-rel vagy ultragyors komputertomográfiás képalkotással kell kivizsgálni. A koszorúér-angiográfia akkor javallott, ha más vizsgálatok nem diagnosztizálnak.” Röviden, nem döntenek 1 diagnosztikus vizsgálat vagy más mellett.”
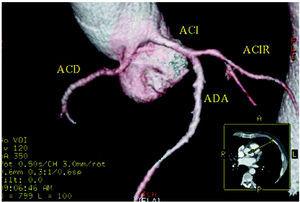
Figura 5. Multislice komputertomográfia (16 szelet); háromdimenziós renderelt rekonstrukció, amely a bal sinus Valsalvából kiinduló jobb koszorúeret (ACD) mutatja. ACI indiactes bal koszorúér; ACIR, circumflex koszorúér; ADA, elülső leszálló koszorúér. Dr. Joaquín Alonso, Servicio de Cardiología y Servicio de Diagnóstico por Imagen, Hospital de Fuenlabrada, Madrid, Spanyolország, jóvoltából.
A 35 év feletti, angina pectoris klinikai tüneteivel vagy ismételt syncopéval jelentkező betegeknél a funkcionális vizsgálat (ergometria, terheléses echokardiográfia stb.) után általában katéterezést végeznek, mivel az ateroszklerózis nagyobb előfordulása miatt felmerül a koszorúérbetegség gyanúja. Bizonyos, a technológiával felszerelt központokban az atipikus klinikai képpel rendelkező betegek kezdeti szűrése multidetektoros CT-vel vagy CRMI-vel történhet. Mindkét esetben a CAA lenne a lelet (6. ábra).
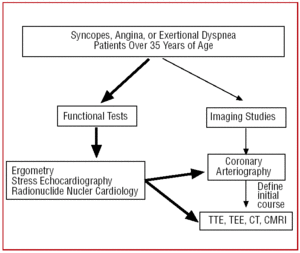
6. ábra. Javasolt diagnosztikai protokoll 35 év feletti, koszorúér-anomáliára gyanús betegeknél. A CRM a szív mágneses rezonanciás képalkotását jelöli; CT, komputertomográfia; TEE, transoesophagealis echokardiográfia; TTE, transthoracalis echokardiográfia.
HOGYAN ÉRTÉKELJÜK A KORONARIA ANOMALIA ELSŐ KORÁBBAN?
Ez a CAA vizsgálatának egyik legösszetettebb pontja, és alapvető szempontot jelent a kockázat azonosításában.
Kezdésként figyelembe kell vennünk, hogy a koszorúér nevét és jellegét az általa ellátott terület határozza meg, nem pedig az eredete. Így egy olyan koszorúér, amely a jobb sinus Valsalvából ered, és az elülső leszálló és a circumflex (Cx) artériák területének ellátására ágazik ki, nem jobb koszorúér, hanem bal fő koszorúér, amelynek eredete a rossz sinusban van. Ha egy koszorúér a rossz sinusból ered, a neve, a jellege, sőt a funkciója is ugyanaz marad, csak az eredete és a kezdeti lefolyása anomális.2
A rossz sinus Valsalvából való kilépést követően egy anomális koszorúér legalább öt különböző útvonalon2,52 keresztül érheti el a normális ellátási területét:
1. Retrocardialisan, a mitrális és a tricuspidalis billentyű mögött.
2. Retroaortás, általában a Cx követi, amelynek eredete a jobb Valsalva-szinuszban vagy a jobb koszorúérben van, a hátsó aortafal mellett, a pitvar és az aorta közötti barázdában (sinus transversus) (3. ábra).
3. Preaortás vagy interarteriális (az aorta és a tüdőartéria között), amelyben az anomális jobb koszorúér, bal elülső leszálló vagy bal fő koszorúér keresztezi a septumot vagy az aortopulmonális teret. Ez az a lefolyás, amely a leggyakrabban iszkémiás tünetekkel és/vagy hirtelen halállal jár (7. és 8. ábra).
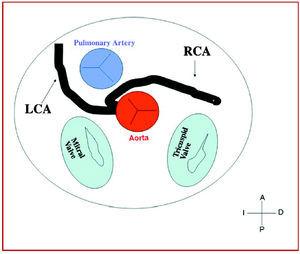
7. ábra. A jobb oldali koszorúér (RCA) kontrollaterális sinusból kiinduló interarteriális lefolyását bemutató ábra.
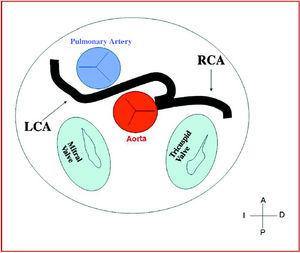
8. ábra. A kontrollaterális sinusból kiinduló bal koszorúér (LCA) interarteriális lefolyását bemutató ábra.
4. Intraseptális, az intraventrikuláris septum felső részén keresztül. Az esetek többségében intramyocardialis, és az angiográfián a myocardialis hídhoz hasonló szisztolés szűkületről ismerhető fel, valamint arról, hogy ebben a zónában általában 1 vagy 2 septalis perforátor ág található (9. ábra).

9. ábra. A jobb oldali sinus Valsalvából kiinduló bal oldali koszorúér (CI) intraseptális lefolyását bemutató ábra.
5. Prekardiális vagy prepulmonális, jellemző a szubepikardiális elhelyezkedése, a jobb kamra kiáramlási traktusának elülső falában vagy az infundibulumban. Ezt a járatot általában anomális jobb koszorúér, bal főtörzs vagy bal elülső leszálló koszorúér követi.
Egy adott betegnél más lehetséges járatokról vagy akár több járatról is beszámoltak.2
Hogyan azonosíthatók ezek a kezdeti járatok a koszorúér-angiográfiával? Kezdetben úgy gondolták, hogy az anomália és a nagy erek közötti kapcsolat meghatározásához elegendő egy vezetődrót bevezetése a tüdőartériába, majd ezt követően a koszorúér-arteriográfia oldalirányú vetítésben. Ez a technika azonban korlátozott értékű, mivel például oldalnézetben mind a szeptális, mind az interarteriális szakasz látszólag a tüdőartéria mögött és az aorta előtt helyezkedik el, miközben a valóságban a szeptális szakasz mindkét érhez képest caudalisan helyezkedik el.53
Az anomália és kezdeti szakaszának felismerésére szolgáló különböző koronária-angiográfiás jellemzőkről, még a vizualizáció előtt, szintén beszámoltak. Ezzel kapcsolatban Page és munkatársai54 két olyan jelet javasolnak, amelyek lehetővé teszik a Cx anomális eredésének és kezdeti lefolyásának felismerését:
1. A “nem perfundált myocardium” jel. A bal koszorúér szelektív átlátszatlansága során a bal kamra posterolaterális zónájában avaszkuláris területet figyelhetünk meg, amely a Cx anomális eredetére utal. Először kontrasztanyagot kell injektálni a bal koszorúér sinusba, hogy kizárjuk az elülső leszálló és a Cx artériáktól független ostiumok érintettségét. Ha azonban a Cx azonosítása nem egyértelmű, nem szabad elfelejtenünk, hogy gyakoribb a jobb koszorúér-szinuszból vagy a jobb koszorúérből eredő Cx megfigyelése, mint a bal koszorúér-szinuszban lévő különálló ostia jelenléte.55
2. Az “aorta gyökér” jel. Ventrikulográfiában a jobb elülső ferde vetületben látható az anomáliás Cx kontúrja, és követi annak lefolyását, amint a jobb koszorúér sinus mögött halad (10. ábra).
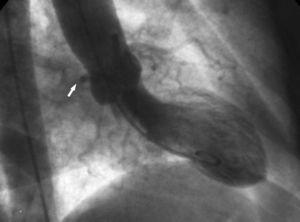
10. ábra. Ventrikulográfia jobb elülső ferde vetületben, amely a jobb oldali sinus coronaria mögött haladó anomális arteria circumflexa (nyíl) kontúrját mutatja; ezt a jelet aortagyökér-jelnek vagy Page-jelnek nevezik.
1985-ben Ishikawa és munkatársai,56 majd 1990-ben Serota és munkatársai,57 egy sor koronária-arteriográfiás kritériumot javasoltak, amelyek célja az anomális ér és az aorta, valamint a tüdőartéria közötti kapcsolat meghatározása volt a kezdeti szakasz mentén (11. ábra). Ezek a szerzők az anomális koszorúér és a koszorúérfa többi része által alkotott “hurok” orientációja56 alapján, illetve a “pont” fogalmának alkalmazásával (a CAA kontrasztanyag-oszlopának vizualizációja, amely az általa tett fordulat miatt egy pont morfológiáját veszi fel57) próbálták azonosítani a különböző lefolyásokat.
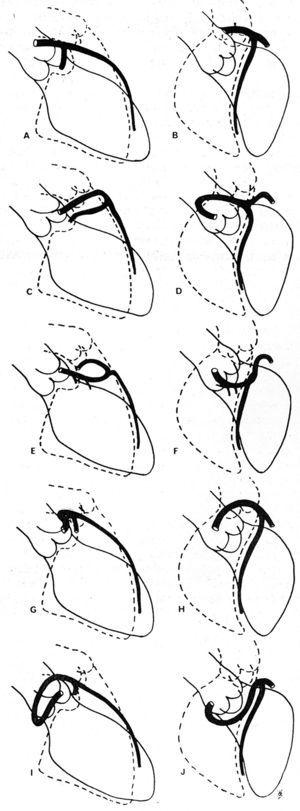
11. ábra. A bal elülső leszálló és a proximális circumflex koszorúerek coronaria-angiográfiásc felvételeinek illusztrációi jobb elülső ferde vetületben (A, C, E, G, I) és bal elülső ferde vetületben (B, D, F, H, J), amelyek a jobb sinus Valsalva-ból kiinduló bal koszorúér különböző lehetséges kezdeti lefutásait mutatják. A és B egy normális koszorúeret ábrázol; C és D: anterocranialis “hurok”, az elülső lefolyásban leírtak; E és F: anterocaudalis “hurok”, szeptális lefolyás; G és H: posterocranialis “hurok”, interarteriális lefolyás; I és J: posterocaudalis “hurok”, retroaorta lefolyás. Ishikawa és mtsi. 56
A CAA kezdeti lefolyásának azonosítása koronarográfiával sok esetben nehéz, mivel ez a technika kétdimenziós képet ad a koszorúérfáról, amely egy összetett háromdimenziós struktúra. A CAA diagnózisában jártas intervenciós kardiológusnak a koszorúér-angiográfia elegendő lehet a lefolyás helyes azonosításához. Tekintettel azonban alacsony előfordulási gyakoriságukra, a legtöbb intervenciós kardiológusnak korlátozott tapasztalata van a CAA vizsgálatában. Így az esetek túlnyomó többségében nem megfelelően írják le őket. Egy nemrégiben 13 spanyol kórházat érintő regiszterben a bejelentett CAA kezdeti lefolyását az esetek többségében nem azonosították.16
Ezért sok esetben a rossz sinusból kiinduló CAA kezdeti lefolyásának azonosításához további képalkotó technikára van szükség. Mint fentebb említettük, mind a TTE, mind a TEE alkalmazható erre a célra, de mivel kórházainkban egyre nagyobb számban állnak rendelkezésre olyan noninvazív technikák, amelyek a műtétre esetleg jelölt betegeknél a koszorúér anatómiájának és a szomszédos struktúrákkal való kapcsolatának pontosabb és pontosabb meghatározását teszik lehetővé, mi a CMRI vagy a multidetektoros CT mellett döntünk.35,37,47,49
Mi a legjobb terápiás megközelítés?
Ez az egyik legvitatottabb aspektusa ennek az állapotnak, mivel e tekintetben még nem alakultak ki hivatalos irányelvek.
Mihelyt a CAA-t diagnosztizálták és jellemezték, logikusnak tűnik, hogy megpróbálják meghatározni, hogy az okozza-e a myocardialis ischaemiát vagy sem. Ha a betegnek volt már szívinfarktusa (az ateroszklerózissal nem kimutatható összefüggésben), vagy az anomáliának tulajdonítható hirtelen halál miatt újraélesztésen esett át, és 35 év alatti, a legtöbb szerző revascularisatiót javasol.24,26,35
A döntési folyamatot segíti a talliumstresszvizsgálat vagy a gyógyszeres vagy terheléses stressz alatti echokardiográfia, amely reverzibilis ischaemiát mutat az anomália területén.36
Mit kell tenni azon fiatal, tünetmentes egyének esetében, akiknél a CAA-t véletlenül fedezik fel, ha a kockázati kritériumok teljesülnek, de a stresszteszt nem mutat ischaemiát? Először is, a betegnek mozgásszegény életmódot kell folytatnia.26,35
Corrado és munkatársai fiatal sportolók és nem sportolók hirtelen halálát hasonlították össze, és csak a CAA-nak vagy aritmogén jobb kamrai diszpláziának tulajdonított esetek voltak összefüggésben a terheléssel.58 A kezelés tekintetében a revaszkularizáció vitatott, de vannak szerzők, akik ezt a megközelítést választják, mivel ezeknél a betegeknél a hirtelen halál kiszámíthatatlan és a CAA első jele lehet.24,26,34,35 Egyes szerzők ezekben az esetekben támogatják az évenkénti kontrollvizsgálatokat echokardiogrammal vagy thallium stresszvizsgálattal, és az eredményekre alapozzák döntésüket.7,36 A műtéti kezelést követően a betegek normális életmódot folytatnak, beleértve a sportolásban való részvételt is.25,34,49
A 35 év feletti betegeknél a döntéseket egyénre szabottan kell meghozni. A hirtelen halál kockázata kisebb, de mivel a CAA tüneti myocardialis ischaemiát okozhat, egyes esetekben revaszkularizációra kerül sor (12. ábra).24,26
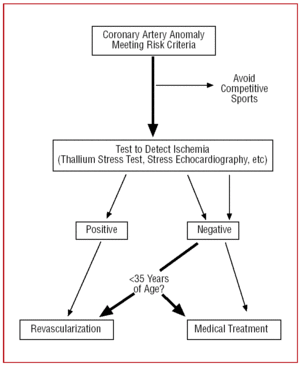
12. ábra. A kontralaterális sinus Valsalvából kiinduló koszorúér-anomáliákra javasolt terápiás protokoll rizikófaktorok jelenlétében.
Egyes csoportok vizsgálják bizonyos diagnosztikai protokollok alkalmazását (intrakoronáriás echokardiográfia az anomális koszorúér-ostium nyugalomban és dobutamin-infúzió vagy folyadék-túlterhelés után történő felmérésére)59 vagy intrakoronáriás nyomásdrótok felhasználását az iszkémia kimutatására.60
Mint megfigyelhető, amíg hivatalos irányelvek nem születnek ebben a kérdésben, a legésszerűbb megközelítésnek az tűnik, hogy először is meg kell erősíteni, hogy a beteg életkora és a CAA anatómiája összefügg-e a kockázattal, másodszor pedig ellenőrizni kell, hogy a (beteg által bemutatott vagy kimutatott) koszorúér-iszkémiát egyértelműen az anomália idézte-e elő.
HOGYAN KELL A REVASZKULÁRISZTÁCIÓT VÉGREHAJTANI?
Logikailag minden esetet egyénileg kell kezelni a koszorúér anatómiájának megfelelően; így a revaszkularizáció lehet sebészi vagy perkután.
A sebészi revaszkularizáció magában foglalja az aortokoronáriás bypass, az ostialis reimplantáció vagy az unroofing technika alkalmazását, amely a CAA intramurális szegmensét a CAA és az aorta közös falán végzett metszéssel szabadítja fel, így a megfelelő sinusban új, nagyobb nyílás jön létre.61,62 A műtéti revaszkularizációval kapcsolatban ezeknél a betegeknél, különösen a fiataloknál, sok az ellentmondás. Az aortokoronáriás bypass-graftot erősen kritizálták7,63 a “korlátozott” átjárhatóság és a bypass és a CAA közötti elkerülhetetlen versengő áramlás miatt. Ezért egyre gyakrabban alkalmazzák az unroofing technikát, amely fiziológiásabbnak tűnik62.
A perkután beavatkozást, stentek beültetésével a nagy erek közötti kompresszió és az anomális ostium régiójában, több esetben végeztek már, felnőtteknél, rövid távú sikerrel64. A mai napig a sebészeti revaszkularizációt fiatal betegeknél részesítik előnyben, a perkután beavatkozást pedig csak felnőtteknél végzik.26,62-64 Nyilvánvaló, hogy mindkét esetben hosszú távú követés szükséges.
A MEDIKÁLIS KEZELÉS LEHETŐSÉG?
A sorozat és a kontrollált vizsgálatok hiánya miatt nehéz erre a kérdésre válaszolni. Vannak olyan beszámolók, amelyek a 2 és 5 éves utánkövetést érintik azoknál a betegeknél, akik vagy a műtétet elutasító betegeknél, akiknél a megközelítés vagy várakozó kezelés, vagy béta-blokkolókkal való kezelés volt, és akik között nem fordult elő hirtelen halál.65-68 Egyes szerzők azonban ellene érvelnek annak a döntésnek, hogy gyermekeknél és serdülőknél “élethosszig tartó” kezelés kezdődjön.7
FŐBB MEGOLDATLAN PROBLÉMA
A hirtelen halál valódi kockázata az egyes anomáliákhoz kapcsolódóan ismeretlen.5 Ennek oka, hogy a kockázatot boncolási vizsgálatok alapján számítják ki, amelyek nem mutatják meg annak valós kockázatát, hogy egy személy CAA következtében hal meg, hanem azt a lehetőséget sugallják, hogy a hirtelen halált megélt személynek CAA-ja van.7 Ráadásul a kiszámított kockázatokat az általános népességhez képest túlbecsülhetik, mivel azokat versenysportolók sorozataiból nyerték, akiknél – amint arról már beszámoltak – kétszer nagyobb a hirtelen halál kockázata, mint egy mozgásszegény személynél.69 Tudjuk, hogy a CAA okozta hirtelen halál kockázata nagyobb a fiataloknál; valójában egyik vagy másik terápiás megközelítést ajánlják attól függően, hogy a beteg 30 vagy 35 évnél fiatalabb. Ezek a határértékek a témával foglalkozó kevés tanulmányon23,25 alapulnak, és ezért csupán tájékoztató jellegűnek tekintendők. Emiatt a terápiás megközelítésről mindig egyénileg kell dönteni.
Ha a fent leírt műtéti megoldást választjuk, figyelembe kell venni, hogy nincs olyan sorozat, amelyben a betegek lefolyását két évnél hosszabb ideig tanulmányozták volna. A bypass átjárhatóságával kapcsolatos bizonytalansághoz hozzáadódik az aortabillentyű esetleges károsodása, amelyet a tetőbontó eljárás okozhat. E tekintetben vannak beszámolók az eljárást követő aortaelégtelenségről vagy akár billentyűcseréről.7,70 Nem szabad elfelejtenünk, hogy a szívműtétek mindig magukban hordozzák a neurológiai szövődmények kockázatát, amelyek előfordulását fiatalok esetében 2,3% körülire becsülik.71
Végezetül, a kardiovaszkuláris anomáliákkal rendelkező versenysportolók kiválasztására vonatkozó irányelvek a CAA-s betegek kizárását javasolják minden versenysportból.51 Ismét egy sportolói populációból származó adatokat extrapoláltak az általános populációra. Egy serdülő esetében a “versenysport” fogalmát nehéz lehet meghatározni. Ráadásul egy serdülő vagy fiatal felnőtt eltiltása a tornaórákon vagy az általa esetleg kedvelt sportágban való részvételtől több kárt okozhat, mint hasznot. Talán a megerőltető sportokat kerülni kell, de egy kevésbé megerőltető sportot nem.7
Összefoglalás
A rossz Valsalva-szinuszból kiinduló koszorúerek alkotják a CAA-nak azt a csoportját, amely a leggyakrabban társul a szívizom iszkémiához és különösen a hirtelen halálhoz.
Az ezen anomália gyanúindexének magasnak kell lennie az angina, dyspnoe vagy terheléses syncope klinikai jeleit mutató fiatal betegeknél. Ezekben az esetekben TTE-t kell végezni, hogy megpróbáljuk azonosítani az ostiumokat és mindkét koszorúér kezdeti lefolyását.
Kórházunk jellemzőinek megfelelően egyértelműen meg kell határoznunk minden anomáliás koszorúér kezdeti lefolyását, olyan képalkotó eljárásokkal, mint a TTE, a TEE vagy lehetőleg a multidetektoros CT vagy a CMRI.
Kiemelten kell kezelnünk olyan nemzeti és nemzetközi regiszterek létrehozását, amelyek lehetővé teszik számunkra, hogy meghatározzuk ezen anomáliák előfordulását, valamint a kapcsolódó morbiditási és mortalitási arányokat, a prognózist, a kezelést, az esetleges genetikai vagy környezeti hatásokat, egyszóval, hogy minél többet megtudjunk erről.
A CAA miatt műtött betegek, különösen a fiatalok hosszú távú követését kell elvégezni. Mindenesetre a revaszkularizáció (sebészeti vagy perkután) érvényes lehet az ilyen típusú betegségben szenvedő betegek számára.
MEGJEGYZÉSEK
Köszönjük Dr. Joaquín Alonso és Dr. Gabriel C. Fernández segítségét a multidetektoros komputertomográfiás felvételek megszerzésében.
Köszönjük Dr. Joaquín Alonso és Dr. Gabriel C. Fernández segítségét a multidetektoros komputertomográfiás felvételek megszerzésében.