- Háttér és bevezetés
- Az eset bemutatása
- Diszkusszió
- Az ADI patofiziológiája
- Irodalomkutatás
- Az ADI okai
- Az ADI klinikai megjelenése
- Az ADI társuló szövődményei
- Az ADI kezelési megközelítései
- Következtetés
- Adatok elérhetősége
- Etikai nyilatkozat
- Beegyezés a részvételhez
- A szerzők hozzájárulása
- Finanszírozás
- Conflict of Interest Statement
- Acknowledgments
Háttér és bevezetés
A hipotalamikus adipsziás diabetes insipidus (ADI), egy ritka, heterogén klinikai megjelenésű szindróma, amelyet a vízháztartás homeosztatikus mechanizmusainak hibái jellemeznek. Ezek közé tartozik az ozmoregulációs szomjúságszabályozó mechanizmus, az arginin vazopresszin szekréció és a vizelet koncentrálására való vese képesség. Az elmúlt négy évtizedben világszerte kevesebb mint száz súlyos esetről számoltak be (1).
Az ilyen betegek kezelése rendkívül nagy kihívást jelent, mivel ezeknél a betegeknél a plazmanátrium nagymértékű ingadozására hajlamos még akkor is, ha a DI jól kontrollált (2).
Egy súlyos ADI esetről számolunk be, amely agyi arteriovenosus malformáció (AVM) műtét után, posztoperatívan következett be. Leírjuk a lehetséges patogenezist ebben az esetben, és áttekintjük az irodalmat az összes hasonlóan jelentett esetről, valamint ismertetjük a lehetséges mechanizmusokat, a klinikai megjelenést, az akut és a krónikus kezelést és a prognózist.
Az eset bemutatása
Egy 27 éves hölgy bal frontális intracerebrális vérzéssel jelentkezett intraventrikuláris kiterjedéssel, amely egy bazális ganglion nagy komplex (AVM) következménye, amely a bal középső agyi artériákból (MCA) és az elülső agyi artériákból (ACA) származó komplex artériás tápcsatornákkal rendelkezik, Spetzler Martin-féle 3-as osztályozási skálán (3).
A dekompresszív kraniotómia és a vérrögeltávolító műtét utáni kezdeti felépülés után ~2 héttel később elektív AVM kimetszési műtétet végeztek rajta. Az AVM műtét során a sebészek élénk vérzésről számoltak be a feeder-erekből (MCA, ACA és a choroidális erek), súlyos intracerebrális vérzéssel és intraventrikuláris vérzéssel, amely masszív, akár 32 egységnyi vérátömlesztést igényelt intraoperatívan. Barbiturát-indukált kómát és indukált hipotenziót kapott az agyi ödéma minimalizálása érdekében (4).
Nem sokkal a bőséges intraoperatív vérzés epizódja után intraoperatívan nagy mennyiségű vizeletet tartalmazó poliuria kezdődött. Bár preoperatívan nátriumkoncentrációja normális volt, a nátriumkoncentráció azonnal (az 1. órán belül) posztoperatívan 151-160 mmol/l tartományban magasabb volt, alacsony vizelet ozmolalitással <130 mosm/l mellett. Tranziens DI-nek tekintették, és intravénásan 1 mcg desmopressint (IV desmopressin) kezdtek adni neki, amelyet 3 egymást követő napon keresztül naponta 3,5-4 l félliteres sóoldatinfúzióval együtt adtak.
Azóta azonban tüdőödéma alakult ki nála (valószínűleg az intraoperatív masszív vérátömlesztés, az intravénás hipotóniás folyadék és az egyidejűleg adott IV desmopresszin következménye) a 4. posztoperatív napon, az IV desmopresszint abbahagyták, és friss fagyasztott plazmát és vízhajtókat (intravénás furoszemid 40 mg) adtak az extravaszkuláris ödéma csökkentése érdekében. A következő órában ismét poliuria kezdett kialakulni, egy óra alatt 800 ml vizeletürítéssel, és nátriumkoncentrációja 172 mmol/l-re emelkedett. Tekintettel az egyidejűleg fennálló posztoperatív agyi ödémára, úgy döntöttek, hogy a nátriumkoncentrációt célzottan úgy csökkentik, hogy a nátriumcsökkenés mértéke 5-10 mmol/l/napon belül maradjon, a célszint 155 mmol/l volt. Alacsony dózisú, 0,25 mcg dezmopresszint adtak intravénásan, és titrálási rendszert javasoltak a 100 ml/h alatti óránkénti vizeletmennyiség fenntartása érdekében. Az 5. posztoperatív napon 0,75 mcg desmopresszin intravénás adására volt szüksége, majd a 6. napon, amikor elérte a 155 mmol/l-es célszintet, naponta kétszer 0,25 mcg intravénás adásra volt szüksége. Ezt a nátriumkoncentrációt a desmopresszin adagolással további 2 napig fenn lehetett tartani.
A 9. napon posztoperatívan abbahagyták a desmopresszin adagolását, mivel a kis vizeletmennyiséget desmopresszin nélkül is fenn tudta tartani, és a nátriumkoncentráció stabil volt. Ebben a szakaszban úgy ítélték meg, hogy nála kialakult a nem megfelelő antidiuretikus hormonszekréció szindróma (SIADH), és a folyadékbevitelt 1 l/napra korlátozták. Nátriumkoncentrációja ezen a héten stabilan 134-138 mmol/l maradt.
A 14. posztoperatív napon ismét poliuria alakult ki nátriumkoncentráció és szérum ozmolalitás emelkedésével. Ekkor az intravénás desmopresszin adagolást újra felvették, napi kétszer 0,25 mcg mennyiségben. A nátriumkoncentrációt 138-150 mmol/l szinten lehetett tartani intravénás desmopresszinnel (naponta kétszer 0,25 mcg) és folyadékkal. A nő trifázisos fázison ment keresztül, átmeneti DI-vel, majd SIADH-val, és ezt követően állandó DI-vel (lásd az 1. ábrát). A szérum kortizol-, növekedési hormon-, inzulinszerű növekedési faktor-1-, pajzsmirigyfunkció- és prolaktinszintek mind a normális tartományban voltak.

1. ábra. A betegünknél a kórházi kezelés alatt végzett összes soros mérést bemutató grafikon.
Az AVM kimetszése után 6 héttel történt ventrikuloperitoneális sönt beültetése után (az intrakraniális nyomás fenntartása érdekében) rehabilitációs osztályra szállították, és az intravénás desmopressin kezelést szubkután (SC) kezelésre alakították át (lásd az 1. ábrát). Amikor a nasogastrikus szondatáplálást abbahagytuk, megpróbáltuk szomjúsággal szabályozni a folyadékbevitelt. A vérvizsgálatok 165 mmol/l-ig emelkedő nátriumszintet mutattak, és a szérum 350 mosm/kg-os szérumozmolalitása ellenére a hypernatraemia ezen időszakában nem érzett szomjúságot. Az afázia helyreállása ellenére adipsziás maradt. Szomjúságskálát nem alkalmaztunk, mivel kérdésre a nő úgy nyilatkozott, hogy egyáltalán nem érez szomjúságot, és a szomjúságskálát nem lehetett alkalmazni. Ezért a folyadékbevitelt szabályozni kellett a nátriumegyensúly fenntartása érdekében. A vizeletürítést rögzítették, és a nátriumegyensúlyt jól szabályozták a reggeli 0,5 mcg és az esti 0,375 mcg desmopressint tartalmazó SC-kezeléssel, napi 1,5-2 liter szabályozott folyadékbevitellel. Nem volt jele hőszabályozási zavarnak. Polyetheretheretherketone (PEEK) cranioplasztikát végeztek ~4 hónappal a kezdeti műtét után.
Az 5 hónapos intenzív multidiszciplináris rehabilitáció után még mindig nem működött a domináns jobb keze és jelentős kognitív deficitje maradt, és a szubkután desmopresszin biztonságos adagolása és önadagolása hosszú távon nem volt lehetséges.
A nazális desmopresszinnel és az orális desmopresszinnel végzett vizsgálat jelentős változó felszívódást mutatott, ami a nátriumkoncentrációk nagyobb ingadozásához vezetett. A továbbiakban a desmopressin Melt néven kapható szublingvális desmopresszin alkalmazása mellett döntöttünk. A különböző adagolási sémák többszöri kipróbálása után a reggeli 120 mcg (2 tabletta) és az esti 60 mcg (1 tabletta) dezmopressin Melt orális liofilizátummal a vizeletürítést körülbelül 2 L/napra tudtuk rögzíteni. Ennél az adagnál azonban a nap bizonyos időszakaiban hiponatrémia lépett fel. További dózistitrálást végeztünk úgy, hogy a dezmopresszin tablettákat csipesz/csipesz segítségével kivettük a buborékcsomagolásból, és a tablettákat tablettavágó segítségével pontos negyedrészekre (egyenként 15 mcg) vágtuk. A reggeli 90 mcg (1,5 tabletta) és az esti 75 mcg (1,25 tabletta) adagolással hasonló eredményeket értünk el, mint a szubkután adagolással. Ezzel a rendszerrel és napi 2 liter szabályozott folyadékbevitellel a nátriumkoncentrációját a 135-150 mmol/l-es tartományban tartottuk, nagyobb ingadozások és kognitív tünetek nélkül. Ez az adagolás azt is lehetővé tette, hogy napközben fokozottan aktív legyen a rehabilitáció érdekében, és éjjel a poliuria miatt zavartalanul tudott aludni.
Az 1. ábrán láthatók a nátrium sorozatos mérései ennél a betegnél a kórházi kezelés teljes időtartama alatt a fent leírt eseményekkel.
A klinikai anamnézisre és arra való tekintettel, hogy a hypophysis és a hypothalamus nagyrészt ép, nem valószínű, hogy a baroregulációban jelentős hibák voltak.
Diszkusszió
Az ADI patofiziológiája
Fiziológiás körülmények között a plazma nátrium, ozmolalitás és vízháztartás szűk tartományokon belül tartható másodlagosan a szomjúság és vízbevitel, a neurohypophysealis vazopresszin-szekréció és a vese distalis gyűjtőcsöveiben zajló antidiurézis gondos kölcsönhatásának köszönhetően.
A perifériás jelek (oropharyngeális, bél osmoszenzorok, vér ozmolalitás) valós időben kódolják az aktuális hidratációs állapotra vonatkozó információkat, és ezeket központilag integrálják (5). A dehidratáltság állapota stimuláló jeleket eredményez a subfornikus szerv (SFO) felé, amely hierarchikusan jeleket küld a lamina terminalis organum-vasculosum (OVLT) és a medián preoptikus mag (MnPO) felé (6). Az MnPO, amely “központi detektorként” szolgálhat, stimuláló jeleket küld a hipotalamikus magoknak, hogy növeljék a vazopresszin felszabadulását, és fokozott szomjúságjelzést is küld az SFO-n és az OVLT-n keresztül (7, 8). A szomjúsággal kapcsolatos neurális pályák, amelyek az SFO-t és az OVLT-t a cinguláris és az insuláris kéreggel kötik össze, a szomjúság tudatos érzékelését eredményezik (7, 8). Ezzel szemben a megfelelő hidratáltság állapotában a perifériás szenzorokból érkező jelek e területek gátlásához és az MnPO negatív visszacsatolásához vezetnek, ami a szomjúság elnyomását és a vazopresszin-szekréció és -felszabadulás csökkenését eredményezi (piros áramkör). Valójában az MnPO, az OVLT és az SFO neuronjai kiterjedten és kölcsönösen összekapcsolódnak, mivel e területek bármelyikének neuronjainak optogenetikai és kemogenetikai aktiválása stimulálhatja a szomjúságot (9). Ennélfogva a sejtkárosodást eredményező vérellátás megszakadása adipsziához vezet. Az SFO és az OVLT neuronális sejtjeinek autoimmunitásából eredő ADI eseteit is publikálták, ami jelzi ezen neuronális szenzorok funkcionális jelentőségét a szomjúságszabályozásban (10).
Az AVP neuronok “fázisos” akciós potenciálok aktivitását mutatják olyan intervallumokkal, amelyekben az AVP az axonvégződésekben felszabadul. A vazopresszin felszabadulását az MnPO-ból származó ozmózisérzékelő bemenetek szabályozzák a baroreceptorokon keresztül, és van egy anticipációs szabályozás is, amelyben a vazopresszin felszabadulása étkezés előtt (prandialis), hipertermián és cirkadián mintázatban stimulálódik (11). A keringésben a vazopresszin szekréciójának cirkadián napi mintázata van, a szintek 24:00 és 02:00 óra között emelkednek, és a nap folyamán fokozatosan csökkennek, a mélypont 16:00 és 20:00 óra között van (12). Ez a cirkadián éjféli emelkedés, amelyet a vazopresszin felszabadulás növekedése okoz, részben a magnocelluláris neuroszekréciós neuronok fokozott szinaptikus gerjesztésének eredménye a suprachiasmatikus mag által, amelyről ismert, hogy szabályozza a cirkadián ritmust (11). ADI-ben a vazopresszin-szekréció ozmózisszenzoros szabályozása a leginkább érintett, és az egyéb hatások a sérülés helyétől és kiterjedésétől függően változhatnak, míg a baroreceptor-válaszról ismert, hogy számos korlátozott sérüléssel rendelkező betegnél megmarad, amint azt egy tanulmány kimutatta (13).
Az AVP a vazopresszin-2 (V2) receptorokon keresztül hat a vese gyűjtőcsatornáira, hogy növelje a vízpermeabilitást, ami csökkent vizeletképződéshez vezet. A víz reabszorpcióját a vízcsatorna, az aquaporin-2 (AQP2) szabályozásán keresztül szabályozzák. Az AVP rövid távon az AQP2-t hordozó vezikulák intracelluláris transzlokációját indukálja az apikális plazmamembránba, így szabályozva az AQP2-kereskedelmet. Hosszú távon megfelelő AVP-koncentráció esetén szabályozza az AQP2 gén transzkripcióját, hogy növelje az AQP2 fehérje mennyiségét a gyűjtőcsatornában (14). Az ADI esetében azt a feltevést fogalmazzuk meg, hogy valószínűleg az akut ozmózisérzékelési választ jobban befolyásolja, mint a krónikus választ. Ennélfogva az aquaporin relatív abundanciája megmarad, de az apikális membránba irányuló akut trafikálást befolyásolja.
A mechanizmusok részletes bemutatását lásd a 2. ábrán.
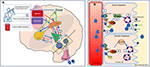
2. ábra. A folyadékegyensúly szabályozásának sematikus ábrázolása az emberben. (A) A vazopresszin-szekréció irányítása és szabályozása az agyban. (A) A perifériás jelek (oropharyngeális, bél ozmózisérzékelők, vér ozmolalitás) valós időben (1) és központilag integráltan (2) kódolják az aktuális hidratációs állapotra vonatkozó információkat. A dehidratáltság állapota stimuláló jeleket eredményez az SFO felé, amely hierarchikusan jeleket küld az OVLT-nek és az MnPO-nak (3). Az MnPO, amely “központi detektorként” szolgálhat, stimuláló jeleket küld a hipotalamikus magoknak, hogy növelje a vazopresszin felszabadulását (4), valamint fokozott szomjúságjelzést küld az SFO-n és az OVLT-n keresztül (5, kék áramkör az ábrán). Ezzel szemben a megfelelő hidratáltság állapotában a perifériás szenzorokból érkező jelek gátolják ezeket a területeket, és az MnPO negatív visszacsatolása a szomjúság elfojtásához és a vazopresszin-szekréció és -felszabadulás csökkenéséhez vezet (6. piros áramkör). A szomjúsággal kapcsolatos neurális pályák, amelyek az SFO-t és az OVLT-t a cinguláris és az insuláris kéreggel kötik össze, a szomjúság tudatos érzékelését eredményezik (7). Adipsziás DI-ben az ozmoszenzoros ingerek hiányában a sejtkárosodás miatt kapcsolódó neurális áramkörök, a vazopresszin stimuláló felszabadulása vagy gátlása és a szomjúság tudatos észlelése egyaránt zavart szenved. (B) A vazopresszin hatásmechanizmusa a vese gyűjtőtubulusaira. (B) A vérkeringésben lévő vazopresszin a vese disztális gyűjtőtubulusának fő sejtjeinek luminális felszínén lévő vazopresszin-receptor 2-höz kötődik (1). Az akut fázisban az AC-n (adenilát-cikláz) keresztül ATP-ből cAMP szintézis útján proteinkináz A-t képez (2), amely serkenti az aquaporin transzlokációját a tároló vezikulából az apikális membránba és a vér luminális felszínére (3). Ennek eredményeképpen víz kerül a sejtbe (4), majd felszívódik a keringésbe (5). A krónikus fázisban az aquaporin gén cAMP által közvetített transzkripciós kontrollja révén (6) az aquaporin vízcsatorna megnövekedett szintje található a fő sejtekben (7). Az adipsziás DI-ben az akut válasz valószínűleg jobban érintett, mint a krónikus válasz, mivel az ozmoszenzorral kapcsolatos vazopresszin-szekréciót érinti.
Irodalomkutatás
Szisztematikus irodalomkutatást végeztünk, beleértve a Pubmed, Scopus és Embase adatbázisokat az 1980 és 2018 közötti évek ADI esettanulmányaként vagy esetsorozataként közölt esetekre vonatkozóan. A keresési kifejezést használtuk: Adipszia, Adipsziás rendellenesség és Adipsziás DI, és a keresést az angol nyelvre és az Emberekre korlátoztuk. Az egyes esetjelentések/esetsorozatok olvasása során azonosított egyéb hivatkozásokra is rákerestünk. Az irodalomban 25 hivatkozást találtunk (10, 13, 15-39), összesen 45 esetről számoltak be. Az összes esetismertetést az 1. táblázatban foglaltuk össze.
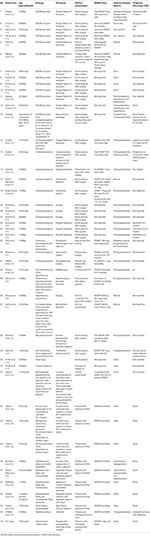
Táblázat 1. táblázat. Az irodalomban közölt adipsziás diabetes insipidusban szenvedő betegek demográfiája, etiológiája, klinikai megjelenése, kezelése és prognózisa.
Az ADI okai
A szakirodalomban leírt ADI esetek negyven százaléka (17/46) az anterior kommunikáló artéria (ACOM) aneurizma ruptura és a műtétet követő, frontális craniectomiás megközelítéssel végzett clipping következtében következett be. Egy esetben a craniopharyngioma és az ACOM aneurizma kettős patológiáját írták le (15). Az OVLT artériás ellátása négy forrásból származik (40): (1) egy felső medián forrás, amely az elülső kommunikáló artériából ágazik el, (2) és (3) két oldalsó forrás, amelyek az elülső kommunikáló artéria alatt az egyes elülső agyi artériákból elágazó artériákból származnak, és (4) egy alsó medián forrás, amely a chiasma opticus alatt emelkedik fel. Jellemző, hogy az e szervet bélelő kapillárisok a vér-agy gáton kívül helyezkednek el, ezért az ozmolalitás változása könnyen érzékelhető e szervek által (41). Meg kell jegyezni, hogy a műtéti technikák fejlődése és a coiling alkalmazása a clipping helyett csökkentheti ezeket a szövődményeket. A jó klinikai állapotban lévő, az elülső keringés rupturált aneurizmájával rendelkező, coilingre alkalmas betegek esetében egy metaanalízis adatai azt mutatják, hogy a coiling jobb kimenetellel jár (42). Összehasonlítva a clippeléssel, amely során az ACA mindkét végét lecsippentik a hypothalamus vérellátásának megszakításával, a tekercsnek az aneurizmába való behelyezésével végzett eljárás a legtöbb esetben képes megőrizni a hypothalamus táplálását.
Az ADI második okaként a suprasellaris craniopharyngiomát írták le (17/46). Ezek az esetek gyakran transzfrontális kimetszéssel járnak, és néhány esetben leírták a műtét utáni gyógyulást. Leírtak egy esetet kavernózus haemangiomáról is, amely hasonló manifesztációval járt vérzéses epizód után (26).
A hipotalamikus tumorok, beleértve a hamartomát, a tobozmirigy tumort és a csírasejtes tumort, ADI-vel járhatnak (26, 29, 30). Beszámoltak egy esetről, amikor a hepatocelluláris karcinóma metasztázist adott a hypothalamusba és ADI-t eredményezett (31).
Érdekes módon csak két esetben írtak le agyalapi mirigy daganatot ADI-val (18, 32). Mindkét esetben agresszív daganatról volt szó, többszörös transzfrontális reszekcióval és intraoperatívan intrakraniális vérzéssel. Egy-egy esetet fejsérüléssel és toluol expozícióval kapcsolatban is leírtak (13).
Négy esetet írtak le hirtelen akut poliuria és hipernátrémia megjelenésével. Ezeknél a betegeknél nem volt strukturális eltérés a hypothalamusban, és a részletes vizsgálatok az OVLT szervei elleni antitestek kimutatását igazolták. Ezekben az esetekben autoimmun patológiát tételeztek fel a háttérben (10, 33).
A corpus callosum fejlődési problémáival küzdő betegeknél veleszületett vagy kora gyermekkori eseteket is leírtak ADI manifesztációval (34-38). Az elülső agyalapi mirigyet, a hátsó agyalapi mirigyet és a hypothalamust kiterjedten érintő neurosarcoidosis esetét is leírták ADI-val (39).
Az ADI klinikai megjelenése
A legtöbb leírt esetben a klinikai megjelenés az AVM miatt végzett műtéti clippinget vagy a craniotomiát követő közvetlen héten poliuria. A biokémiai megjelenés hipernátrémia, megnövekedett szérum ozmolalitással a nem megfelelően híg, nagy mennyiségű vizelet jelenlétében. Ha a szomjúságérzetet szomjúságskálával mérik, ezek az ADI-betegek a hipernátrémia ellenére alacsony vagy minimális szomjúságról számolnak be. Érdekes módon ezek a betegek normálisan reagálnak a hipotenzióra, és baroreceptoros mechanizmusuk ép (13).
Páciensünk a kezdeti DI, majd a SIADH, majd a tartós DI trifázisán ment keresztül. Ezt a trifázisos válaszként leírt mintázatot hipofízis és craniopharyngioma műtétek után is leírták már. A trifázisos válasz patofiziológiája a jelek szerint a korai hipotalamusz diszfunkcióval (amelyet poliuria és hipernátrémia jellemez), ezt követően az előformált vazopresszin felszabadulásával a hátsó agyalapi mirigy tároló vezikuláiból (amely nem kapcsolódik semmilyen ingerhez) (amelyet a SIADH jellemez), végül pedig a vazopresszinraktárak kimerülésével (állandó DI) magyarázható (43). Betegünk esetében valószínű, hogy a harmadik fázisban a SIADH megszűnése után a vazopresszin felszabadulásában az ozmolalitásra adott válasz hiányossága lepleződik le, nem pedig a vazopresszin abszolút kimerülése.
Az ADI társuló szövődményei
A hőszabályozási zavarokat kevés esetismertetés írta le. Panhypopituitarizmusról csak craniopharyngioma és hypophysis tumoros esetekben számoltak be, a mi betegünknél nem volt jelen.
A hypernatremia egyéb fontos szövődményei közé tartozik a mélyvénás trombózis, bár nem következetesen jelentették, ezért akut betegség és immobilizáció idején alacsony molekulasúlyú heparin adható (18).
A hypothalamikus elhízásról és alvási apnoéról is gyakran beszámoltak (18). Egy esetsorozatban (13), amelyben a hipotenzióra adott AVP-választ értékelték, azt találták, hogy a craniopharyngiomás betegeknél a baro-szabályozott AVP-válasz is elmaradt. Ezeknél a betegeknél pánhypopituitarizmusra utaló jelek voltak, ami arra utal, hogy a daganataik műtéte az agyalapi mirigy szélesebb körű károsodását hagyta maga után, beleértve a hátsó agyalapi mirigyet is, amely az AVP-szekréció végső közös útvonala.
Az ADI kezelési megközelítései
Az ilyen esetek kezelését már leírták (15, 18). A beteg és a család felvilágosítása a vízháztartás és a kezelés elveiről döntő fontosságú. A vízbevitel napi 1,5-2 literben rögzíthető, majd a desmopresszin titrálása elvégezhető. A napi testsúlykövetés hasznos a dehidratáció vagy a folyadéktúlterhelés felismeréséhez. A plazma nátriumkoncentrációjának heti mérése ajánlott az ingadozások nyomon követése érdekében. A szigorú ellenőrzés ellenére nehéz reprodukálni a plazma nátriumkoncentrációjának éjjel-nappal történő, a fiziológiás ozmoregulációt utánzó szabályozását. Tekintettel a nátriumkoncentráció gyors ingadozásának kockázatára és az alacsony referenciatartományban észlelt hyponatremia tüneteire, célszerű a nátriumkoncentrációt a magasabb referenciatartományban tartani.
A desmopressint, az AVP szintetikus analógját először 1972-ben vezették be a DI kezelésére (44). A legtöbb beteg jól reagál a naponta kétszer adott alacsony dózisú desmopresszinre. Finom az egyensúly, és a nátriumszint nagyon alacsony szintre ingadozhat a legkisebb dózis-skálázással.
A mi betegünk nagyon jól bírta a nagyon alacsony dózisú parenterális adagolást, amelyről köztudott, hogy a biohasznosulása a legkisebb változékonyságú (45). Az intranazális készítmények felszívódása nagyon változó, különösen kognitív problémákkal küzdő gyermekek vagy felnőttek esetében, mivel előfordulhat, hogy nem következetesen lélegezik be az oldatot (46, 47). Az orális készítmények jó választásnak bizonyulnak, mivel a dózis növelése hosszabb hatástartamot eredményez, de nincs csúcshatás (48-50). Ezt a formát 50-100 mcg közötti különböző dózisokban próbáltuk ki, de jelentős napi eltéréseket tapasztaltunk a hatásban ennél a készítménynél. A szublingvális desmopresszin (Minirin Melt) 2005 óta kapható. Farmakológiai vizsgálatok kimutatták, hogy a szublingvális út ~60%-kal nagyobb biológiai hasznosulást eredményez az orális útvonalhoz képest (49, 50). A szublingvális desmopresszin finomított dózisát az egyes 60 mcg-os tabletták feldarabolásával lehetett elérni, ami 65-90 mcg-os szublingvális dózist tesz lehetővé. Az ilyen osztott tabletták hasonló farmakokinetikai profilját már leírták (51). Ismert, hogy az egyidejű táplálékbevitel 40%-kal csökkenti a felszívódás sebességét és mértékét, ezért a legjobb, ha a szublingvális desmopresszin tabletta beadása előtt és után egy órával kerüljük az ételfogyasztást. A közelmúltban részletes folyadékbeviteli protokollt írtak le napi nátriummonitorozással, fix dózisú szubkután desmopresszinnel (28), amely a napi szintű monitorozás nehézségeit mutatja be. Egy másik közelmúltbeli esetismertetés (27) szintén beszámolt a szublingvális desmopresszin forma alkalmazásáról ADI esetén napi 60 és 120 mcg dózisban. A szublingvális desmopresszin alkalmazása hasznos alternatíva lehet azokban az esetekben, amikor más készítményekkel nem lehet optimális hatást elérni. ezek a betegek a napi testsúly, a vizeletmennyiség és a folyadékbevitel szigorú, éjjel-nappal történő ellenőrzését igénylik. Tekintettel a kognitív és memóriazavarokra, amelyekkel ezek a betegek általában küzdenek, általában gondozóra van szükségük, aki figyelemmel kíséri a folyadékbevitelt, hogy biztosítsa, hogy a szükséges mennyiséget fogyasztják.
Az általunk áttekintett esetek közül 6 betegnél javult az ADI, ebből 2 ACOM aneurizmához (15, 16), 4 pedig craniopharyngiomához (15, 26) kapcsolódott. Egy neurosarcoidosisban szenvedő betegnél az Infliximab-terápia hatására remisszió következett be (39). Ezek a megfigyelések arra utalhatnak, hogy mind a szomjúságot szabályozó osmoreceptorok, mind azok efferens pályái nagyobb neuroplaszticitást mutatnak, mint az AVP-termelődést szabályozó pályák (26).
Következtetés
Az ADI a hypothalamusbetegségek rendkívül ritka szövődménye, amely a szomjúságközpont funkcióvesztését eredményezi. A szomjúságközpontból kiinduló hierarchikus kontroll miatt a szomjúság hiánya a vazopresszin szabályozás elvesztésével és polyuriával is jár. Az ADI-ban szenvedő alanyokat óvatosan kell kezelni alacsony dózisú desmopresszinnel és folyadékegyensúlyozással. A jelenlegi megfigyelési és személyre szabott gondozási megközelítésekkel még mindig nem lehetséges az éjjel-nappal történő kvázi fiziológiás ozmoreguláció utánzása.
Adatok elérhetősége
Az e tanulmányhoz létrehozott összes adatkészletet a kézirat/kiegészítő fájlok tartalmazzák.
Etikai nyilatkozat
A cikkben szereplő, potenciálisan azonosítható képek vagy adatok közzétételéhez a személy(ek)től írásbeli beleegyezést kaptak.
Beegyezés a részvételhez
A beteg legközelebbi hozzátartozójától írásbeli engedélyt kaptunk a kézirat megírásához és közzétételéhez.
A szerzők hozzájárulása
RD volt az elsődleges endokrinológus, aki a beteg folyadékegyensúlyát kezelte, ő fogalmazta meg az ötletet, írta a kéziratot, végezte az irodalmi áttekintést, szerezte az adatokat, írta és ellenőrizte a végleges kéziratot. HC, AC és JH rezidensek voltak, akik részt vettek a beteg kezelésében, és átnézték a végleges kéziratot. HT volt a betegért felelős aneszteziológus az intenzív ellátási fázisban, ő fogalmazta meg az ötletet, és kritikusan értékelte a végleges kéziratot. KC volt a betegért felelős fő rehabilitációs szakember, ő fogalmazta meg az ötletet, és kritikusan értékelte a végső kéziratot. BB fogalmazta meg az ötletet, és kritikusan értékelte a végső kéziratot.
Finanszírozás
RD részben az Országos Orvosi Kutatási Tanács Center Grant (NMRC/CG/017/2013) és az Országos Orvosi Kutatási Tanács Clinician Scientist Award (MOH-CSAINV17nov-0006) támogatásával készült.
Conflict of Interest Statement
A szerzők kijelentik, hogy a kutatást olyan kereskedelmi vagy pénzügyi kapcsolatok hiányában végezték, amelyek potenciális összeférhetetlenségként értelmezhetők.
Acknowledgments
Köszönjük a betegnek és szüleinek, hogy engedélyezték a kézirat megírását és közzétételét.
1. Eisenberg Y, Frohman LA. Adipsziás diabetes insipidus: áttekintés. Endocr Pract. (2016) 22:76-83. doi: 10.4158/EP15940.RA
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Az orvosok és az orvostudományi szakemberek által készített tanulmányok a következő cikkekből állnak:
2. Robertson GL. A szomjúságszabályozás rendellenességei. Kidney Int. (1984) 25:460-9. doi: 10.1038/ki.1984.39
PubMed Abstract | CrossRef Full Text | Google Scholar
3. Spetzler RF, Martin NA. Az arteriovenosus malformációk javasolt osztályozási rendszere. J Neurosurg. (1986) 65:476-83. doi: 10.3171/jns.1986.65.4.0476
PubMed Abstract | CrossRef Full Text | Google Scholar
4. 4. Hagyományosan a neurológiai és neurológiai kórképek, mint például az ún. Ellens NR, Figueroa BE, Clark JC. A barbiturát-indukált kóma alkalmazása cerebrovaszkuláris idegsebészeti beavatkozások során: az irodalom áttekintése. Brain Circ. (2015) 1:140-6. doi: 10.4103/2394-8108.172887
CrossRef Full Text | Google Scholar
5. Google Scholar
. Zimmerman CA, Huey EL, Ahn JS, Beutler LR, Tan CL, Kosar S, et al. A folyadék ozmolaritásának bélből az agyba irányuló jele szabályozza a szomjúság telítettségét. Nature. (2019) 568:98-102. doi: 10.1038/s41586-019-1066-x
PubMed Abstract | CrossRef Full Text | Google Scholar
6. Augustine V, Gokce SK, Lee S, Wang B, Davidson TJ, Reimann F, et al. Hierarchical neural architecture underlying thirst regulation. Nature. (2018) 555:204-9. doi: 10.1038/nature25488
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Bichet DG. A szomjúság és a vazopresszin felszabadulás szabályozása. Annu Rev Physiol. (2019) 81:359-73. doi: 10.1146/annurev-physiol-020518-114556
PubMed Abstract | CrossRef Full Text | Google Scholar
8. 8. A víztúltengés és a szomjúság iránti vágy kielégítése. McKinley MJ, Denton DA, Ryan PJ, Yao ST, Stefanidis A, Oldfield BJ. Az érzékszervi körkörös szervektől az agykéregig: a szomjúságot és az éhséget irányító idegi pályák. J Neuroendocrinol. (2019) 31:e12689. doi: 10.1111/jne.12689
PubMed Abstract | CrossRef Full Text | Google Scholar
9. Keresés English (2019) 31:212689. McKinley MJ, Yao ST, Uschakov A, McAllen RM, Rundgren M, Martelli D. A medián preoptikus mag: a testfolyadék, a nátrium, a hőmérséklet, az alvás és a kardiovaszkuláris homeosztázis szabályozásának frontja és központja. Acta Physiol. (2015) 214:8-32. doi: 10.1111/apha.12487
PubMed Abstract | CrossRef Full Text | Google Scholar
10. Google Scholar
. Hiyama TY, Matsuda S, Fujikawa A, Matsumoto M, Watanabe E, Kajiwara H, et al. Autoimmunitás az agyban lévő nátriumszint-szenzorral szemben esszenciális hipernátrémia okozója. Neuron. (2010) 66:508-22. doi: 10.1016/j.neuron.2010.04.017
PubMed Abstract | CrossRef Full Text | Google Scholar
11. Beszélgetés az Amerikai Tudományos Akadémia és a Magyar Tudományos Akadémia között. Baylis PH, Thompson CJ. A vazopresszin szekréció és a szomjúság ozmoregulációja egészségben és betegségben. Clin Endocrinol. (1998) 29:549-76. doi: 10.1111/j.1365-2265.1988.tb03704.x
PubMed Abstract | CrossRef Full Text | Google Scholar
12. XII. Gizowski C, Bourque CW. A homeosztatikus és az anticipatív szomjúság neurális alapjai. Nat Rev Nephrol. (2018) 14:11-25. doi: 10.1038/nrneph.2017.149
PubMed Abstract | CrossRef Full Text | Google Scholar
13. 13. A szomjúság és a szomjúságtudat kutatása és fejlesztése. Smith D, McKenna K, Moore K, Tormey W, Finucane J, Phillips J, et al. A vazopresszin felszabadulás baroregulációja adipsziás diabetes insipidusban. J Clin Endocrinol Metab. (2002) 87:4564-8. doi: 10.1210/jc.2002-020090
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Google Scholar
14. PubMed Abstract | CrossRef Full Text | Google Scholar. Jung HJ, Kwon TH. Az aquaporin-2 szabályozásának molekuláris mechanizmusai a vese gyűjtőcsatornájában. Am J Physiol Renal Physiol. (2016) 311:F1318-28. doi: 10.1152/ajprenal.00485.2016
PubMed Abstract | CrossRef Full Text | Google Scholar
15. Cuesta M, Gupta S, Salehmohamed R, Dineen R, Hannon MJ, Tormey W, et al. Heterogén mintázatok a szomjúság helyreállításában adipsziás diabetes insipidusban szenvedő felnőtt betegeknél. QJM. (2016) 109:303-8. doi: 10.1093/qjmed/hcv175
PubMed Abstract | CrossRef Full Text | Google Scholar
16. Google Scholar
. Imai E, Kaneko S, Tsukamoto Y. A vese kompenzációs alkalmazkodása a vízkezeléshez egy adipsziás diabetes insipidusban szenvedő betegnél az elülső kommunikáló artéria rupturált aneurizmájának clippingje után. Clin Nephrol. (2017) 88:112-6. doi: 10.5414/CN108963
PubMed Abstract | CrossRef Full Text | Google Scholar
17. PhD. McIver B, Connacher A, Whittle I, Baylis P, Thompson C. Adipsziás hypothalamus diabetes insipidus az anterior kommunikáló artéria aneurizma klipszelése után. BMJ. (1991) 303:1465-7. doi: 10.1136/bmj.303.6815.1465
PubMed Abstract | CrossRef Full Text | Google Scholar
18. MTA doktora. Ball SG, Vaidya B, Bayliss PH. Hypothalamus adipsziás szindróma: diagnózis és kezelés. Clin Endocrinol. (1997) 47:405-9. doi: 10.1046/j.1365-2265.1997.2591079.x
PubMed Abstract | CrossRef Full Text | Google Scholar
19. Hormonális hormonháztartás. Nguyen BN, Yablon SA, Chen CY. Hypodipsziás hypernatremia és diabetes insipidus az elülső kommunikáló artéria aneurizma clippingjét követően: diagnosztikai és terápiás kihívások az amnesztikus rehabilitációs betegnél. Brain Injury. (2001) 15:975-80. doi: 10.1080/02699050110063459
PubMed Abstract | CrossRef Full Text | Google Scholar
20. Agyvérzés és agykárosodás. Nussey SS, Ang VT, Jenkins JS. Krónikus hipernátrémia és hipotermia subarachnoidalis vérzést követően. Postgrad Med J. (1986) 62:467-741. doi: 10.1136/pgmj.62.728.467
CrossRef Full Text | Google Scholar
21. 21. Postgrad Med J. (1986) 62:467-741. Spiro SG, Jenkins JS. Adipszia és hipotermia subarachnoidalis vérzést követően. BMJ. (1971) 3:411-2. doi: 10.1136/bmj.3.5771.411
CrossRef Full Text | Google Scholar
22. Google Scholar
22. Crowley RK, Sherlock M, Agha D, Smith D, Thompson CJ. Klinikai betekintés az adipsziás diabetes insipidusba: egy nagy esetsorozat. Clin Endocrinol. (2007) 66:475-82. doi: 10.1111/j.1365-2265.2007.02754.x
PubMed Abstract | CrossRef Full Text | Google Scholar
23. Hosszú időn át tartó tanulmányok és tanulmányok a következő témakörökben készültek:
. Colleran K, Sanchez-Goettler L, Sloan A. Craniopharyngioma sebészi reszekcióját követő adipsziás centrális diabetes insipidusszal szövődményes hypothalamus obesitas. J Clin Hypertens. (2009) 11:608-10. doi: 10.1111/j.1751-7176.2009.00057.x
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Hiperhypertonia és hipertónia. Zantut-Wittmann D, Garmes HM, Panzan AD, Lima Mde O, Baptista MT. Súlyos rabdomiolízis adipsziás hipernátrémia miatt craniopharyngioma műtét után. Arq Bras Endocrinol Metabol. (2007) 51:7. doi: 10.1590/S0004-27302007000700023
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Raghunathan V, Dhaliwal MS, Gupta A, Jevalikar G. Az agyi sóveszteségtől az adipsziás diabetes insipidusig: egy craniopharyngiomás gyermek esetleírása. J Pediatr Endocrinol Metab. (2015) 28:323-6. doi: 10.1515/jpem-2014-0224
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Google Scholar
46. Sinha A, Ball S, Jenkins A, Hale J, Cheetham T. A szomjúság helyreállításának objektív értékelése adipsziás diabetes insipidusban szenvedő betegeknél. Pituitary. (2011) 14:307-11. doi: 10.1007/s11102-011-0294-3
PubMed Abstract | CrossRef Full Text | Google Scholar
27. 27. A szomjúság és a szomjúság hiánya, a szomjúság és a szomjúság hiánya. Pérez MA, Millán HA, Naranjo JA, Flórez Romero A. Adipsziás diabetes insipidus másodlagos craniopharyngioma reszekció után. BMJ Case Rep. (2019) 12:e225903. doi: 10.1136/bcr-2018-225903
PubMed Abstract | CrossRef Full Text | Google Scholar
28. BMJ Case Rep (2019) 12:e225903. Pabich S, Flynn M, Pelley E. Napi nátriummonitorozás és folyadékbeviteli protokoll: az ismétlődő kórházi kezelés megelőzése adipsziás diabetes insipidusban. J Endoc Soc. (2019) 3:882-6. doi: 10.1210/js.2018-00406
PubMed Abstract | CrossRef Full Text | Google Scholar
29. Az Endoc Soc. Pereira MC, Vieira MM, Pereira JS, Salgado D. Adipszia egy diabetes insipidusos betegnél. Case Rep Oncol. (2015) 8:385-8. doi: 10.1159/000440611
PubMed Abstract | CrossRef Full Text | Google Scholar
30. Google Scholar
. Zhang Y, Wang D, Feng Y, Zhang W, Zeng X. Juvenilis kezdetű köszvény és adipsziás diabetes insipidus: esetismertetés és irodalmi áttekintés. J Int Med Res. (2018) 46:4829-36. doi: 10.1177/0300060518800114
PubMed Abstract | CrossRef Full Text | Google Scholar
31. J. Int Med Res. Latcha S, Lubetzky M, Weinstein AM. Súlyos hyperosmolaritás és hypernatraemia egy adipsziás fiatal nőnél. Clin Nephrol. (2011) 76:407-11. doi: 10.5414/CN106617
PubMed Abstract | CrossRef Full Text | Google Scholar
32. Nephrológia. Sherlock M, Agha A, Crowley R, Smith D, Thompson CJ. Adipsziás diabetes insipidus makroprolaktinóma miatt végzett hipofízisműtétet követően. Pituitary. (2006) 9:59-64. doi: 10.1007/s11102-006-8280-x
PubMed Abstract | CrossRef Full Text | Google Scholar
33. A hipofízis és a hipofízis közötti összefüggésekről és a hipofízisről szóló tanulmányok. Hiyama TY, Utsunomiya AN, Matsumoto M, Fujikawa A, Lin CH, Hara K, et al. Adipsziás hipernátrémia hipotalamuszlézió nélkül, a subfornikus szervvel szembeni autoantitestekkel kísérve. Brain Pathol. (2017) 27:323-31. doi: 10.1111/bpa.12409
PubMed Abstract | CrossRef Full Text | Google Scholar
34. Google Scholar
. Komatsu H, Miyake H, Kakita S, Ikuta H. A corpus callosum hypoplasiája adipsziás hypernatremia és hypothalamus hypogonadotropinizmus mellett: esetismertetés és az irodalom áttekintése. Pediatr Int. (2001) 43:683-7. doi: 10.1046/j.1442-200X.2001.01453.x
PubMed Abstract | CrossRef Full Text | Google Scholar
35. Hosszú időn át tartó kutatások a gyermekkorban. Schaff-Blass E, Robertson GL, Rosenfield RL. A szomjúság és a vazopresszin ozmoregulációjának veleszületett hibájából eredő krónikus hypernatriémia. J Pediatr. (1983) 102:703-8. doi: 10.1016/S0022-3476(83)80237-6
PubMed Abstract | CrossRef Full Text | Google Scholar
36. PubMed Abstract | CrossRef Full Text | Google Scholar
. AvRuskin TW, Tang SC, Juan C. Esszenciális hipernátrémia, antidiuretikus hormon és neurohypophysin szekréció: válasz klórpropamidra. Acta Endocrinol. (1981) 96:145-53. doi: 10.1530/acta.0.0960145
CrossRef Full Text | Google Scholar
37. Google Scholar
37. Radetti G, Rizza F, Mengarda G, Pittschieler K. Adipsziás hipernátrémia két nővérnél. Am J Dis Child. (1991) 145:321-5. doi: 10.1001/archpedi.1991.02160030091028
PubMed Abstract | CrossRef Full Text | Google Scholar
38. 38. PubMed Abstract | CrossRef Full Text | Google Scholar
. Takeya T, Hamano K, Iwasaki N, Kitazawa R, Tsuji C, Jougamoto M. Krónikus hypernatremia esete corpus callosum agenezissel. Nippon Shounikagakkai Zasshi. (1996) 100:1392-5.
Google Scholar
39. O’Reilly MW, Sexton DJ, Dennedy MC, Counihan TJ, Finucane FM, O’Brien T, et al. Radiológiai remisszió és a szomjúságérzet helyreállítása infliximab-terápia után neurosarkoidózishoz másodlagos adipsziás diabetes insipidusban. QJM. (2015) 108:657-9. doi: 10.1093/qjmed/hct023
PubMed Abstract | CrossRef Full Text | Google Scholar
40. Duvernoy H, Koritké JG, Monnier G. . Zeitschrift für Zellforschung und mikroskopische Anatomie. (1969) 102:49-77. doi: 10.1007/BF00336416
PubMed Abstract | CrossRef Full Text | Google Scholar
41. Hírlevél a Magyar Tudományos Akadémiáról (1969). Duvernoy HM, Risold PY. A circumventricularis szervek: összehasonlító anatómiai és érrendszeri atlasz. Brain Res Rev. (2007) 56:119-47. doi: 10.1016/j.brainresrev.2007.06.002
PubMed Abstract | CrossRef Full Text | Google Scholar
42. 42. Brain Res Rev. (2007) 56:119-47. Lindgren A, Vergouwen MD, van der Schaaf I, Algra A, Wermer M, Clarke MJ, et al. Endovascular coiling versus neurosurgical clipping for people with aneurysmal subarachnoid haemorrhage. Cochrane Database Syst Rev. (2018) 8:CD003085. doi: 10.1002/14651858.CD003085.pub3
PubMed Abstract | CrossRef Full Text | Google Scholar
43. Ewout JH, Robert Z. Vízháztartási zavarok idegsebészeti beavatkozások után: a trifázisos válasz újragondolva. NDT Plus. (2010) 3:42-4. doi: 10.1093/ndtplus/sfp117
CrossRef Full Text | Google Scholar
44. A vízháztartás és a vízháztartás problémái. Andersson KE, Arner B. A DDAVP, a vazopresszin szintetikus analógjának hatásai koponyaűri diabetes insipidusban szenvedő betegeknél. Acta Med Scand. (1972) 192:21-7. doi: 10.1111/j.0954-6820.1972.tb04772.x
PubMed Abstract | CrossRef Full Text | Google Scholar
45. 45. Vizsgálati eredmények és adatok a gyógyszeres kezelésről. Rembratt A, Graugaard-Jensen C, Senderovitz T, Norgaard JP, Djurhuus JC. A dezmopresszin szájon át versus intravénásan, nappal versus éjszaka beadott desmopresszin farmakokinetikája és farmakodinamikája 55-70 éves egészséges férfiaknál. Eur J Clin Pharmacol. (2004) 60:397-402. doi: 10.1007/s00228-004-0781-9
PubMed Abstract | CrossRef Full Text | Google Scholar
46. Hosszú időn át tartó kutatás, amely során az orvosok és az orvostudományi szakemberek is részt vettek a vizsgálatban. Vande Walle J, Stockner M, Raes A, Nørgaard JP. A dezmopresszin 30 éves klinikai alkalmazása: biztonsági áttekintés. Curr Drug Saf. (2007) 2:232-8. doi: 10.2174/15748488607781668891
PubMed Abstract | CrossRef Full Text | Google Scholar
47. Yutaka O, Robertson GL, Nørgaard JP, Juul KV. A neurohypophysealis diabetes insipidus kezelése. J Clin Endocrinol Metabol. (2013) 98:3958-67. doi: 10.1210/jc.2013-2326
CrossRef Full Text | Google Scholar
48. Gyógyszerészi szakfolyóirat. Fjellestad-Paulsen A, Höglund P, Lundin S, Paulsen O. Az 1-deamino-8-D-arginin-vazopresszin farmakokinetikája különböző beadási módok után egészséges önkénteseken. Clin Endocrinol. (1993) 38:177-82. doi: 10.1111/j.1365-2265.1993.tb00990.x
CrossRef Full Text | Google Scholar
49. Hosszú időn át tartó kutatások és vizsgálatok. Lam KS, Wat MS, Choi KL, Ip TP, Pang RW, Kumana CR. Az orális 1-deamino-8-D-arginin-vazopresszin farmakokinetikája, farmakodinamikája, hosszú távú hatékonysága és biztonságossága centrális diabetes insipidusban szenvedő felnőtt betegeknél. Br J Clin Pharmacol. (1996) 42:379-85. doi: 10.1046/j.1365-2125.1996.39914.x
PubMed Abstract | CrossRef Full Text | Google Scholar
50. Hosszú időn át tartó vizsgálat, amely során az orvosok és az orvostudományi szakemberek is részt vettek a vizsgálatban. Steiner IM, Kaehler ST, Sauermann R, Rinosl H, Muller M, Joukhadar C. A desmopresszin plazma farmakokinetikája szublingvális beadást követően: feltáró dózis-skálázási vizsgálat egészséges férfi önkénteseken. Int J Clin Pharmacol Ther. (2006) 44:172-9. doi: 10.5414/CPP44172
PubMed Abstract | CrossRef Full Text | Google Scholar
51. Google Scholar
. De Waele K, Cools M, De Guchtenaere A, Van de Walle J, Raes A, Van Aken S, et al. Desmopressin lyophilisate for the treatment of central diabetes insipidus: első tapasztalatok nagyon fiatal csecsemőknél. Int J Endocrinol Metab. (2014) 12:e16120. doi: 10.5812/ijem.16120
PubMed Abstract | CrossRef Full Text | Google Scholar
.