Az immunrendszer
Az immunrendszer szövetekből, sejtekből és molekulákból áll, amelyek elsődleges funkciója a kórokozók és az átalakult sejtek felismerése, az azokra való reagálás és azok eliminálása.
A veleszületett és az adaptív immunválasz
Az immunrendszernek két fő összetevője van: 1) a veleszületett immunrendszer és 2) az adaptív immunrendszer. A veleszületett immunrendszer a védelem első vonalaként működik, és a kórokozókat a csíravonalban kódolt mintafelismerő receptorokon keresztül észleli, nem alakít ki memóriát, és gyorsan (perceken és órákon belül) reagál. Az adaptív immunrendszer lassan (napok alatt) reagál, antigénspecifikus receptorokat használ, amelyek a fejlődés során több génátrendeződésen mennek keresztül, és immunológiai memóriát alakít ki – “tanul” a kezdeti inzultusból, és felkészíti a szervezetet a hasonló káros anyaggal való jövőbeli érintkezés elleni küzdelemre. Az immunválasz mindkét típusát vagy az extracelluláris folyadékban lévő makromolekulák, vagy a specifikus immunsejtek aktiválása vezérli. Ezeket a válaszokat humorális immunitásnak, illetve sejtközvetített immunitásnak nevezzük.
A sejtközvetített immunválasz alatt az immunsejtek többnyire aszerint rétegződnek, hogy a válasz veleszületett vagy adaptív. A veleszületett immunrendszer főként fagocita sejtekből áll, például neutrofilekből, makrofágokból, természetes ölősejtekből, bazofilokból és másokból, amelyek a veszélyes behatoló szervezeteket veszik célba. Az adaptív immunrendszer sejtjei a T-sejtek és a B-sejtek. A természetes ölő (NK) T-sejtek mind a veleszületett, mind az adaptív immunsejtek jellemzőivel rendelkeznek. Ezenkívül a legtöbb más, nem specifikusan az immunrendszerre jellemző sejttípus is hordozhat veleszületett veleszületett immunfunkciókat citoplazmatikus receptorok, valamint jelátviteli és effektor molekulák, például a RIG-I, STING és NLR családok tagjai formájában. Amint azt a továbbiakban áttekintjük, mindkét rendszer sejtjei a vérképző őssejtek különböző myeloid és lymphoid vonalaiból származnak.
Az immunrendszer összetevői
Az érett immunsejtek az úgynevezett vérképző őssejtekből differenciálódnak. Ezek a csontvelőben, a perifériás vérben és a méhlepényben található pluripotens, differenciálatlan progenitor sejtek. Ezek a vérképző őssejtek differenciálódhatnak a közös myeloid progenitorsejtekké vagy a közös lymphoid progenitorsejtekké.
Lymphoid sejtek
A közös lymphoid progenitor sejtek a limfociták négy fő populációjává differenciálódhatnak, amelyeket a sejtfelszíni receptorok expressziója alapján lehet megkülönböztetni: T-sejtek, B-sejtek, természetes ölősejtek (NK-sejtek) és NK-T-sejtek.
T sejtek
A T sejtek kritikus szerepet játszanak a sejtközvetített immunitásban. Ezeket a sejteket a CD3 T-sejt jelátviteli láncok expressziója alapján azonosítják.
A T-sejtek limfoid progenitor sejtekből keletkeznek, amelyek eredetileg a csontvelőben lévő vérképző őssejtekből fejlődnek ki. Amint a limfoid progenitor elkötelezi magát a T-sejtté válás mellett, a csontvelőből a tímuszba vándorol (innen a T-sejt elnevezés). A tímusz biztosítja a megfelelő mikrokörnyezetet, ahol a T-sejtek különböző altípusokká fejlődhetnek, amelyeket a sejtfelszínen kifejeződő specifikus receptorok határoznak meg. A korai stádiumban érő T-sejtekből, vagyis a timocitákból hiányoznak mind a CD4, mind a CD8 receptorai, ezért ezeket kettős negatív (DN) sejteknek nevezik. A DN sejtek ezután genetikai átrendeződéseken és mutációkon mennek keresztül az alfa és béta T-sejt receptorokat (TCR) kódoló génekben, ami elindítja őket a vonalas elköteleződés útján, amelynek végeredménye egy egyedi antigénhez specifikus affinitással rendelkező T-sejt receptor lesz.
A timociták ezután szelektálódnak, pozitív és negatív módon egyaránt, hogy biztosítsák, hogy felismerjék az “idegen” antigéneket, de ne a gazdaszervezet antigénjeit, amelyek a sejtfelszínen lévő MHC-n keresztül peptidek formájában kerülnek bemutatásra. Ezután csak a mindkét vizsgálaton megfelelt sejteket indítják el a CD4 és a CD8 kifejezésére, így kettős pozitív sejtekké válnak. Az érés végén a T-sejtek vagy a CD4-et vagy a CD8-at fogják kifejezni (és elveszítik a másik kifejeződését), és így egypozitív sejtekké válnak. Ezek az érett CD4- vagy CD8-pozitív T-sejtek ezután a véráramba kerülnek, és kezdetben naiv állapotban vannak, ami azt jelenti, hogy még nem kötelezték el magukat egy adott T-sejt altípushoz.
Ha az érő tímocita az érés során köztes mértékű affinitást mutat a saját MHC peptidek iránt, akkor a káros “saját” antigének felismerésére való képessége miatt szelektálódhat szabályozó T-sejtté (Treg). A vérben vagy a perifériás szövetekben lévő T-sejtek lokálisan is indukálhatók, hogy Tregekké váljanak. A Tregek fő feladata a szelf-antigénekkel szembeni tolerancia fenntartása, valamint a T-effektor sejtek működésének és proliferációjának korlátozása.
A vérbe vagy a perifériás szövetekbe érkezve a naiv T-sejtek indukálhatók T-helper sejtekké. Az antigénprezentáló sejtek (APC-k), mint például a makrofágok, dendritikus sejtek és B-sejtek, megmutatják az antigént a T-sejtnek, és ha receptoruk rendelkezik affinitással, a T-sejt felismeri az antigént. Jellemzően a CD4+ T-sejtek alkalmasak a II. osztályú MHC-fehérjékhez kötött peptidantigének felismerésére. Miután a peptid-MHC-komplex felismerésre került, a T-sejt egy sor belső útvonalat aktivál, amelyek lehetővé teszik az antigénfelismerés igazolását. Csak ezután fog a T-segítő sejt szaporodni, bővítve a rendelkezésre álló, a káros antigénre, például különböző baktériumokra és parazitákra specifikus sejtek körét.
Miután a T-helper sejtek felismerték az antigént és aktiválódtak, különböző citokineket bocsátanak ki, amelyek olyan molekulák, amelyek jelzik a többi immunsejtnek, hogyan kell megfelelően reagálniuk a káros molekulára. A segítő T-sejteknek számos alcsoportja létezik, köztük a Th1, Th2 és Th17. Ezek az alcsoportok különböző citokineket termelnek és választanak ki, amelyek segítenek az immunválasz testre szabásában a kórokozó típusától függően. A Th1 sejtek például az IFN-γ effektor citokinre támaszkodnak, hogy jelezzék a makrofágoknak a káros anyag megemésztését és elpusztítását, míg a Th2 sejtek az IL-4, IL-5, IL-9, IL-10 és IL-13 kombinációját választják ki, hogy a bazofilokat, eozinofileket és más sejteket a fertőzés megtámadására indítsák. A citokinek konkrét mennyisége és fajtái határozzák meg a fertőzésre vagy a káros sejtre adott megfelelő választ. A T-sejtek az önmaga sejtjeire is reagálhatnak úgy, hogy citotoxikus T-sejtekké (vagy természetes ölő T-sejtekké) válnak. Ezek jellemzően CD8+ sejtek, amelyek felismerik a vírusfertőzött sejteket vagy a tumorsejteket. A természetes ölő T-sejteket (NKT) egy későbbi szakaszban részletesebben tárgyaljuk. Ezek és más típusú T-sejtek különböző feladataikat vagy effektor funkcióikat eltérő módon látják el, hogy felismerjék a káros anyagot és más immunsejteket toborozzanak annak elpusztítására, valamint hogy tartós immunválaszt építsenek ki az azonos típusú inzultusra.
A T-sejt receptorok jelátviteli interaktív útvonalát itt tekintjük át részletesen.
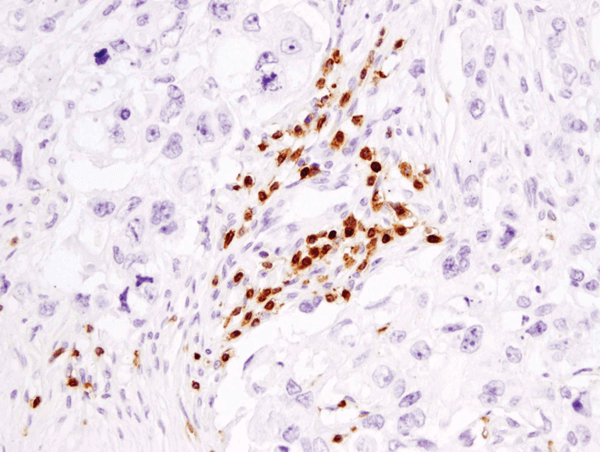
CD3ε (D7A6E™) XP® Rabbit mAb #85061: Paraffinba ágyazott humán emlőrák IHC analízise a #85061 használatával.
CD3ε (D7A6E™) XP® Rabbit mAb #85061: paraffinba ágyazott emberi emlőrák IHC-analízise a #85061 használatával.
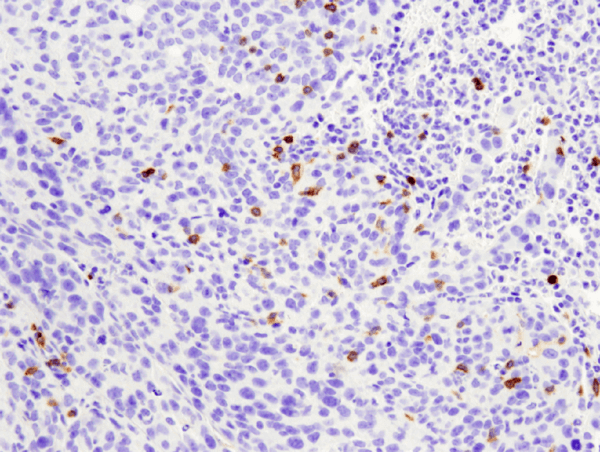
CD4 (D7D2Z) Rabbit mAb #25229: paraffinba ágyazott 4T1 metasztatikus daganat IHC-analízise egér tüdőben a #25229 használatával.
CD4 (D7D2Z) Rabbit mAb #25229: paraffinba ágyazott 4T1 metasztatikus daganat IHC elemzése egér tüdőben a #25229 használatával.
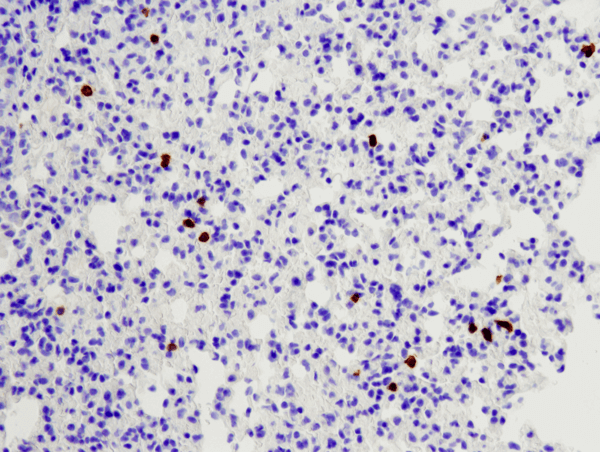
CD8α (D4W2Z) XP® nyúl mAb (egér specifikus) #98941: Paraffinba ágyazott egér tüdő IHC-elemzése a #98941 használatával.
CD8α (D4W2Z) XP® nyúl mAb (egér specifikus) #98941: Paraffinba ágyazott egér tüdő IHC-elemzése a #98941 használatával.
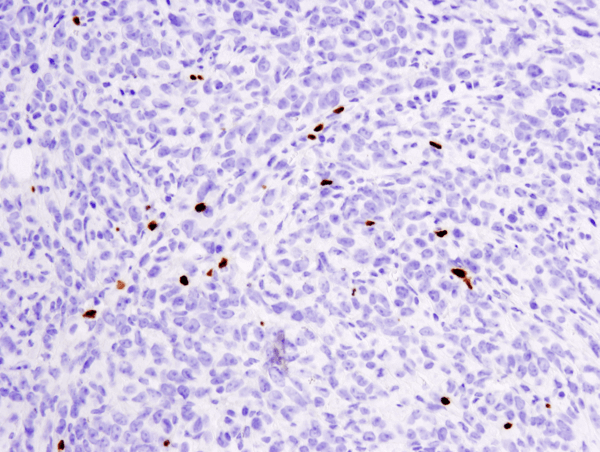
FoxP3 (D6O8R) nyúl mAb #12653: paraffinba ágyazott 4T1 metasztatikus daganat IHC-analízise egér tüdőben a #12653 használatával.
FoxP3 (D6O8R) Rabbit mAb #12653: IHC analízis paraffinba ágyazott 4T1 metasztatikus tumor paraffinjával egér tüdejében a #12653 használatával.
B sejtek
A B sejtek a vérben található kritikus sejtek, amelyek az antitestek termelését közvetítik. Amikor káros anyag kerül a véráramba, azt a B-sejtek specifikus receptorai antigénként ismerik fel. Ezután az antigén feldolgozása után és a T-sejtek segítségével a B-sejt plazmasejtekké érik, amelyek antitesteket választanak ki. A B-sejtek szerepet játszhatnak az antigének prezentálásában és a citokinszekrécióban is. A B-sejtek fejlődését és különböző funkcióit egyaránt tárgyaljuk.
A perifériás vérben található leukociták 15%-a B-sejt. A B-sejtek immunglobulinokat (Ig) termelnek, amelyek antigénkötő fehérjék (más néven antitestek), amelyek két azonos nehézláncból és két azonos könnyű láncból állnak. Ezek az immunglobulinok specifikus antigénkötő helyeket tartalmaznak, amelyek aminosav-sorrendje az egyes antitestmolekulák között eltérő. Ezek a helyek biztosítják az egyes antitestek specifitását egy adott antigén felismerésére.
Mint már említettük, a B-sejtek a csontvelőben található vérképző sejtekből differenciálódnak. A csontvelőben a felszíni Ig-receptorok (antitestek) a gének átrendeződésének folyamatán keresztül épülnek fel. A B-sejtek a kromoszómák sokaságán található különböző gének szomatikus összekapcsolódását használják, amelyek az Ig-t alkotó nehéz és könnyű láncok különböző részeit kódolják. A B-sejteket a csontvelői strómaszövetek IL-7 termelése révén a differenciálódás felé terelik. Ezek a fejlődő B-sejtek a sejtfelszíni receptorok eltérő expressziója által közvetített, egymást követő nehéz- és könnyűlánc-átrendeződések programját követik. Például egy specifikus pre-B sejtreceptor kifejeződése megakadályoz bizonyos génátrendeződéseket a nem rokon kromoszómákon annak érdekében, hogy az érett B sejt egy bizonyos Ig felszíni receptort tudjon kifejezni, amely képes specifikusan felismerni egyetlen antigént. Ezt a folyamatot allélkizárásnak nevezik. Az Ig nehézláncok és könnyűláncok helytelen összeszerelése másodlagos átrendeződést indukálhat a receptor szerkesztése érdekében.
Az Ig-receptor sejtfelszíni kifejeződése mellett a B-sejtek transzmembránfehérjéket is tartalmaznak, amelyek intracelluláris jeleket indukálhatnak, miután egy antigén az Ig-receptor extracelluláris részéhez kötődik. A B-sejtek a T-sejtekhez hasonló intracelluláris jelátviteli kaszkádokat használnak, amelyek a proliferációhoz és éréshez vezető transzkripciós változásokat indukálnak. Konkrétan, az Ig-receptor intracelluláris doménjei foszforilálódhatnak az src-kináz-család által, ami egy kaszkádot indít el, amelyet a Syk tirozinkináz és egy BLINK nevű linkerfehérje továbbít a foszfolipáz C-hez és a guanincsere-faktorokhoz, végül aktiválva a protein kináz C-t, mobilizálva a kalciumot és aktiválva a MAP-kinázt Ras/Rac-függő módon.
A B-sejtek egyedülálló jellemzője az izotípusváltás képessége. Ez konkrétan egy olyan DNS-átrendeződési folyamatra utal, amely kissé eltérő nehézláncokat hozhat létre. Ezenkívül a nehézlánc-exonok alternatív splicingje lehetővé teheti, hogy az Ig a sejtfelszínhez kötött maradjon, vagy szekretálódjon, ha a transzmembrán exon ki van splicingelve. Az alternatív splicinget és az izotípusváltást a T-sejtekből származó citokinek indukálják. Ezenkívül a T-sejtek szomatikus mutációkat indukálhatnak, amelyek a B-sejtek Ig-jének antigénkötő helyein belüli változásokhoz vezetnek. Egy önkorrigáló B-sejt funkció képes felismerni, hogy ezek a látszólag véletlenszerű mutációk az antigén iránti affinitás elvesztéséhez vezetnek-e, és elindítanak-e egy sejtpusztulási programot. Így a T-sejteket és a B-sejteket egyaránt aktiváló antigének izotípusváltáson és szomatikus mutációkon keresztül T-sejt által közvetített B-sejt érést váltanak ki, amelyek mindkettő nagymértékben összefügg a B-sejtmemóriával.
A memória válaszokat az ilyen antigénekre adott gyors és kiterjedt, nagy affinitású Ig-termelés jellemzi. Ezeknek a memóriaválaszoknak a kialakulása kritikus fontosságú a vakcinázás sikere szempontjából. Ugyanakkor fokozhatják az autoimmunitást és az allergiás reakciókat is.
T-sejt független B-sejt aktiváció is bekövetkezhet egy antigén hatására; ez a fajta aktiváció azonban gyenge immunmemóriával jár. Ráadásul ezeknek az antigéneknek polimereknek kell lenniük ahhoz, hogy a B-sejteket aktiválják.
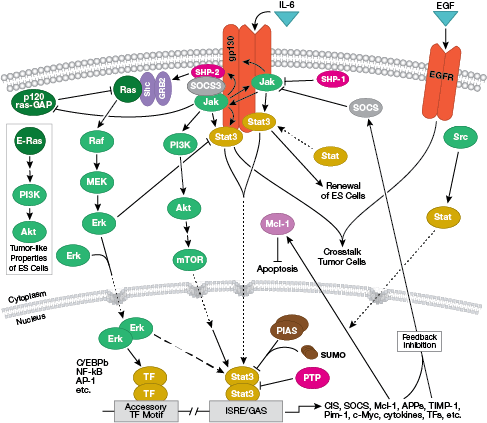
NB: A citokinek vagy interleukinok (IL-ek) olyan szekretált molekulák, amelyek transzmembrán sejtfelszíni receptorokra hatnak. Kötődéskor ezek a citokinek intracelluláris jelátviteli útvonalakat aktiválnak, amelyek jellemzően a Jak-STAT jelátviteltől függenek.
A B-sejt receptorok interaktív jelátviteli útvonalát itt tekintjük át részletesen.
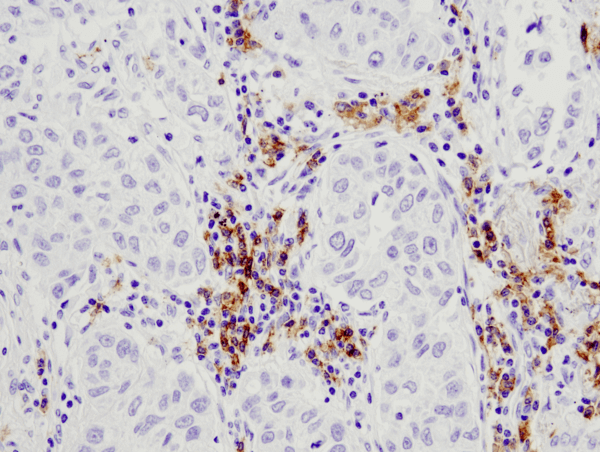
CD19 (D4V4B) XP® Rabbit mAb #90176: Paraffinba ágyazott humán tüdőrák IHC analízise a #90176 használatával.
CD19 (D4V4B) XP® Rabbit mAb #90176: Paraffinba ágyazott emberi tüdőrák IHC-analízise a #90176 használatával.
NK sejtek
A természetes ölő- vagy NK-sejtek egy másik sejttípus, amely a limfoid vonalból származik. A B-sejtekhez hasonlóan a csontvelőben fejlődnek citokin- és csontvelő-stromasejt-függő módon. A perifériás vér kis hányadát teszik ki, és nem rendelkeznek antigénspecifikus receptorokkal. Ehelyett az NK-sejtek transzmembrán receptorok komplex készletére támaszkodnak. Különösen olyan gátló sejtfelszíni receptorokat tartalmaznak, amelyek felismerik az I. osztályú HLA molekulákat, és így a saját MHC molekulák gátolják őket, és csak olyan sejteket ölnek meg, amelyek I. osztályú HLA expressziója lecsökkent. Ezért fontos célpontjaik a vírusfertőzött sejtek és a tumorsejtek, amelyek I. osztályú HLA-kifejeződése le van szabályozva, hogy elkerüljék a CD8+ természetes ölő T-sejtek (NK-T) általi pusztulást. Az NK-sejtek antitest-, interferon- vagy citokinfüggő módon is aktiválhatók, ezért nagy szerepet játszhatnak a daganatok elleni küzdelemben. Az NK-sejtek hatásmechanizmusa a citoplazmájukból granzimeket és perforint tartalmazó kis granulumok felszabadulásán alapul. Felszabadulásukkor ezek a fehérjék pórusokat képesek létrehozni és lebontani az intracelluláris fehérjéket az apoptózis kiváltása érdekében. Ezért az NK-sejteket citotoxikusnak mondják.
Az NK-T sejtek a T-sejtek egy speciális altípusa, amelyek bizonyos, jellemzően az NK-sejtek által kifejezett receptorokat és markereket fejeznek ki a T-sejt receptorok korlátozott repertoárjával kombinálva. Ezért ez az egyedülálló altípus osztozik mind a T-sejtek, mind az NK-sejtek tulajdonságaiban. Az NK-sejtekkel ellentétben, amelyek a csontvelőben fejlődnek, az NK-T sejtek a tímuszban fejlődnek.
Mieloid sejtek
A közös mieloid progenitor sejtek, amelyek a vérképző őssejtek leszármazottai, a mieloid sejtek számos különböző típusát hozzák létre, beleértve a makrofágokat, a dendritikus sejteket és számos más veleszületett immunsejtet és vérsejtet.
Makrofágok
A makrofágok kiválthatják az antigének, például a sérült sejtek vagy idegen anyagok felismerését, hogy igény szerint elpusztítsák azokat. A makrofágok a legtöbb szövetben jelen vannak, és szükség esetén reagálnak a fertőzésekre és a haldokló sejtekre. A felismert anyagot a makrofágok fagocitózis útján pusztítják el, innen kapták a sejtek a nevüket (“nagyevő” görögül). A makrofágok különböző formákat öltenek, amikor különböző helyeken vannak jelen, és a fagocitózison kívül további funkciókat is elláthatnak.
Szövetsérülés vagy kórokozó fertőzés esetén a vérben lévő monociták az érintett szövetbe toborzódnak, és makrofágokká differenciálódnak. A szöveti lokalizációtól függően különböző típusú makrofágok léteznek, például Kupffer-sejtek a májban, alveoláris makrofágok a tüdőben, mikroglia az agyban stb. Ezek a különböző típusú makrofágok mind a monocitákból származnak, de funkciójukat a rezidens szövetre specializálják. Az általános fagocitózis funkció nagy részét a rezidens szöveti makrofágok végzik. Az elhalt sejtek és idegen anyagok fagocitálása mellett a makrofágok citokineken keresztül jelezni is képesek más immunsejteknek. Bizonyos mértékig a makrofágok végzik az antigénprezentáció kritikus funkcióját, ennek megfelelően a T-sejtekkel együttműködve támogatják az adaptív immunitást. Emellett a makrofágok olyan citokineket is szekretálhatnak, mint az IL-12, és szerepet játszanak a helyi immunválaszokban, míg mások nagy mennyiségű IL-10-et választanak ki, ami a szövetek helyreállításában betöltött szerepüket közvetíti. A “nagyevők” tehát a fagocitózis fő feladatán kívül számos szerepet játszanak az immunrendszerben.
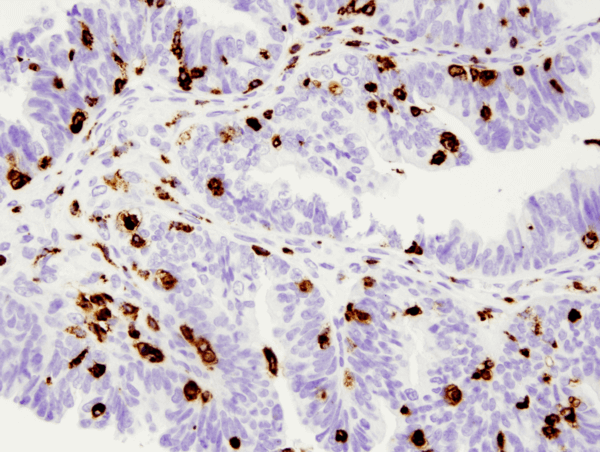
CD68 (D4B9C) XP® Rabbit mAb #76437: Paraffinba ágyazott humán szerózus papilláris petefészek karcinóma IHC elemzése a #76437 használatával.
CD68 (D4B9C) XP® Rabbit mAb #76437: IHC analízis a petefészek paraffinba ágyazott humán serosus papilláris karcinómáján a #76437 használatával.
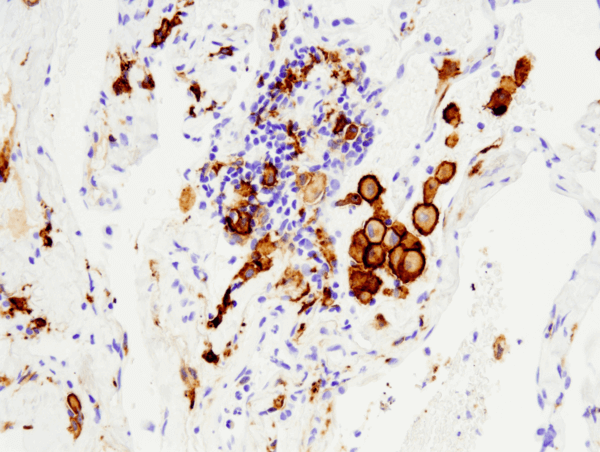
CD163 (D6U1J) Rabbit mAb #93498: Paraffinba ágyazott humán nem kissejtes tüdőrák IHC-analízise a #93498 használatával, Leica® Bond™ Rx készülékkel elvégezve.
CD163 (D6U1J) Rabbit mAb #93498: Paraffinba ágyazott humán nem kissejtes tüdőrák IHC-elemzése a #93498 felhasználásával a Leica® Bond™ Rx készülékkel elvégezve.
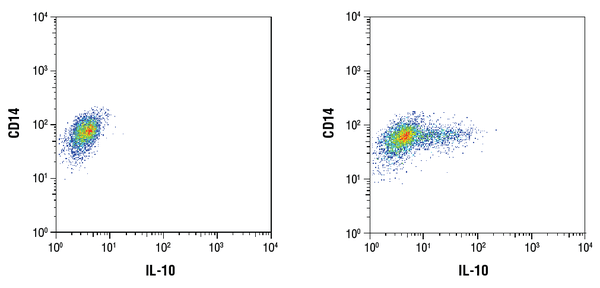
IL-10 (D13A11) XP® nyúl mAb #12163: Tisztított CD14+ humán perifériás vér mononukleáris sejtek áramlási citometriai elemzése kezeletlenül (balra) vagy LPS-szel (100ng/ml, 16 óra; jobbra) kezelve CD14 antitest és #12163 segítségével. Brefeldin A #9972-t (300ng/mL) adtunk a kezeletlen és kezelt sejtekhez 1 óra LPS-stimuláció után. Anti-nyúl IgG (H+L), F(ab’)2 fragmentum (Alexa Fluor® 647 konjugátum) #4414-et használtunk másodlagos ellenanyagként.
IL-10 (D13A11) XP® nyúl mAb #12163: Tisztított CD14+ humán perifériás vér mononukleáris sejtek áramlási citometriai elemzése kezeletlenül (balra) vagy LPS-szel (100ng/ml, 16 óra; jobbra) kezelve CD14 antitest és #12163 segítségével. Brefeldin A #9972-t (300ng/mL) adtunk a kezeletlen és kezelt sejtekhez 1 óra LPS-stimuláció után. Anti-nyúl IgG (H+L), F(ab’)2 fragmentum (Alexa Fluor® 647 konjugátum) #4414-et használtunk másodlagos ellenanyagként.
Dendritikus sejtek
A makrofágokhoz hasonlóan a dendritikus sejtek is képesek a sejtes és idegen anyagok elnyelésére, de ahelyett, hogy megemésztenék azokat eltávolítás céljából, a dendritikus sejtek feldolgozzák az anyagot és antigénként mutatják be a T-sejteknek. Mint ilyenek, a dendritikus sejtek antigénprezentáló sejtekként vagy járulékos sejtekként szolgálnak, és így közvetítik a kórokozókkal kapcsolatos információkat a veleszületett és az adaptív immunrendszer között. A dendritikus sejtek a nevüket különálló sejtnyúlványaikról kapták, amelyek kinyúlnak és megragadják az emésztendő káros anyagot.
A vérképző csontvelő progenitorokból kiindulva a kezdetben éretlen dendritikus sejtek egy “tanulási” fázison mennek keresztül, amikor a helyi területükön idegen anyagot vizsgálnak, és mintafelismerő receptorokon keresztül felismerő választ indítanak el (e receptorok egyik gyakori csoportja a toll-szerű receptorok). Ezek az éretlen dendritikus sejtek különböző helyeken tartózkodhatnak, amelyek hozzáférnek a külső környezethez, például az orr, a gyomor, a tüdő és még a bőr nyálkahártyáján is. Az antigén felismerését követően a dendritikus sejtek a nyirokcsomóba vándorolnak, ahol a T-sejteket az antigén felismerésére és a megfelelő válaszreakcióra tanítják. A dendritikus sejtek az egyetlen antigénprezentáló sejtek, amelyek mind a memória-, mind a naiv T-sejteket aktiválják. A Toll-szerű receptorok a makrofágokon és a dendritikus sejteken jelen lévő receptorok egy jól tanulmányozott osztálya, amelyek az idegen kórokozók felismerését és az azokra adott választ közvetítik. A T-sejtekkel való közvetlen kölcsönhatás mellett a dendritikus sejtek olyan citokineken keresztül is jelezhetnek, mint az IL-12, amely felkészíti az immunrendszert a káros anyag későbbi megtámadására. A dendritikus sejtek más típusai olyan citokineket szekretálhatnak, amelyek jelzik, hogy több makrofágot toborozzanak a túlterhelt hulladékanyag eltakarítására. Az antigénprezentáció fő sejtközvetítőiként a dendritikus sejtek tehát nélkülözhetetlen szerepet játszanak a veleszületett és az adaptív immunrendszer közötti keresztkapcsolatban.
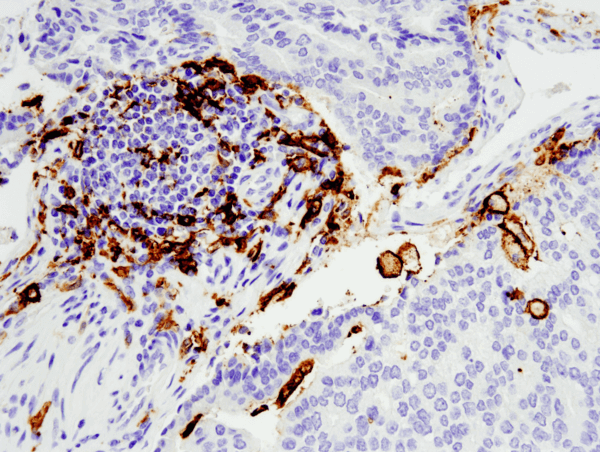
CD11c (D3V1E) XP® nyúl mAb #45581: Paraffinba ágyazott humán prosztata adenokarcinóma IHC-analízise a #455812 használatával, Leica® Bond™ Rx készülékkel elvégezve.
CD11c (D3V1E) XP® Rabbit mAb #45581: IHC-elemzés paraffinba ágyazott emberi prosztata adenokarcinóma paraffinba ágyazott, Leica® Bond™ Rx készülékkel végzett #455812 használatával.
Más veleszületett immunsejtek és jelátvitel
A veleszületett immunrendszer egyéb sejtjei közé tartoznak a hízósejtek, amelyek a sebgyógyulásban működnek és segítenek a kórokozók elleni védelmet biztosítani. Amikor egy kórokozó kiváltja őket, a hízósejtek citokineket, valamint hisztamint és heparint tartalmazó granulátumokat szekretálhatnak, amelyek további immunválaszt közvetítenek, például makrofágok toborzását és az erek tágulását. A neutrofileket, eozinofileket és bazofileket a citoplazmájukban található jellegzetes granulumok miatt együttesen granulocitáknak nevezik. A neutrofilekben a granulumok olyan toxikus vegyületeket szabadítanak fel, amelyek a kórokozókat, például gombákat és baktériumokat célozzák meg.
Immunológia az egészségben és a betegségben
Rákimmunológia
Az immunsejtek hasznosítása a rák elleni küzdelemben a klinikumban elért sikerek miatt igen forró kutatási témává vált. A jelenlegi immunterápia egyik legújabb fókusza a T-sejtek aktiválódását és válaszát normális esetben megakadályozó jelző ellenőrzőpont-fehérjék, például a PD-1 megcélzására irányul. Az adoptív sejtterápia egy másik izgalmas megközelítés, amely a pácienstől származó T-sejtek immunterápiáját foglalja magában. A T-sejteket úgy alakítják át, hogy a beteg rákos sejtjeire specifikus kiméra antigénreceptort fejezzenek ki. A T-sejteket ezután újra befecskendezik a betegbe, és most már úgy vannak programozva, hogy a normál T-sejtfunkciónak megfelelően felkutassák a rákos sejteket és elpusztítsák azokat. Ezek és más megközelítések, amelyekkel az immunrendszert úgy manipulálják, hogy az megtámadja a beteg káros rákos sejtjeit, a rák kezelésére szolgáló terápiák úttörő osztályát jelentik.