Az “ásvány” egy vagy több kémiai elemből álló szervetlen anyag. Definíció szerint az ásványnak:
Az ásvány kémiai összetételét elemi összetételnek nevezzük. A legtöbb ásvány vegyületként (több különböző elem kombinációjaként) fordul elő. Egyes ásványok azonban önmagukban is előfordulnak kémiai elemként. Ezeket natív ásványoknak nevezzük.
Mi a kristály?
A kristályok olyan szilárd anyagok, amelyek atomokból felépülő, szervezett kristályos szerkezettel rendelkeznek. Az atomok belső elrendeződése gyakran külső síkfelületeket eredményez, mint amilyeneket a kvarckristályon láthatunk, ez azonban nem feltétele annak, hogy kristálynak minősüljön. A kristályok az ásványoktól eltérő módon osztályozhatók, mivel egyes anyagok szerves kristályoknak tekinthetők. Mivel az ásványok tisztán szervetlenek, egy szerves kristály nem lehet ásvány. Például a fehérjék és a cukrok olyan szilárd anyagok, amelyek kristályokat képezhetnek, mivel azonban szerves anyagok, nem sorolhatók az ásványok közé.

A kristályokat képző oldatokban lévő szennyeződések színváltozást, valamint jelentős kristályszerkezeti változásokat eredményezhetnek. A kristályrácson belüli túl sok szennyeződés a kristályosodás során kisebb-nagyobb zárványokkal rendelkező kristályokat eredményezhet. Ezek a zárványok a kristály alakját is megváltoztathatják.
Ásványok, kristályok vagy kőzetek?
A legtöbb ásvány a természetben kristályként fordul elő, azonban nem minden kristály ásvány, mivel a szerves kristályok egyáltalán nem ásványok. Egy azonos kémiai képlettel rendelkező ásvány többféle kristálytípust is képezhet. Például a kalcium-karbonátnak három polimorfja (azonos kémiai képlet, különböző kristályszerkezet) létezik, amelyeket kalcit, aragonit és vaterit néven ismerünk. A kalcitkristályok a trigonális rendszerben fordulnak elő, az aragonitkristályok az orthorhombikus rendszerbe tartoznak, a vateritkristályok pedig a hexagonális rendszerben alakulnak ki. Ezek a kristályszerkezetek a képződés során több tényező hatására változhatnak, amelyek közé tartoznak a növekedési mintázatot gátló szennyeződések, a környezet hőmérséklete a képződés során, az ásványok telítettsége az oldatban, a kovalens kötések geometriája és az oldat mozgásának változásai.
Az ásványok természetesen kialakult, szervezett atomszerkezettel rendelkeznek, meghatározott kémiai összetétellel. A kristályok többnyire osztoznak ezekben a jellemzőkben, azonban az atomok ismétlődő mintázatban rendeződnek el, ami kristályrácsot eredményez, gyakran kristályfelületekkel mutatkozva.
Néhányszor hallani, hogy az emberek az ásványokat vagy a kristályokat kőzeteknek nevezik, azonban a “kőzet” meghatározása szerint az ásványok, mineraloidok vagy más kőzetek töredékeinek kötött halmaza. A “kötött” szó azt jelenti, hogy az ásványok halmazának bizonyos értelemben össze kell cementálódnia. Például a homokot nem tekintik kőzetnek, még akkor sem, ha a legtöbb esetben a homokszemcsék össze vannak kötve. A homokkő például azért vált kőzetté, mert a homokszemcséket finomabb szemcséjű ásványok és/vagy szerves anyagok cementálták össze, viszonylag szilárd masszát alkotva.
A kőzetek három fő osztályozása a vulkáni, a metamorf és az üledékes kőzetek.
Igneózus kőzet – Olyan kőzet, amely a litoszférán (földkéreg) belül vagy fölött lévő magma lehűlésével és kristályosodásával keletkezett. A magmán belül kristályok képződnek, amikor az elkezd megszilárdulni, amelyek közül a lehűlés sebessége szabhatja meg a képződő kristályok méretét.

A porfirites gránit, egy vulkáni kőzettípus közeli nézete. A porfirites gránit akkor keletkezik, amikor a magma lehűlésének hőmérséklete gyorsan változik. Ebben az esetben lassú lehűléssel nagy kristályok alakulhattak ki, majd egy hirtelen csökkenő hőmérsékletváltozás megszakította, ami felgyorsította a kristályosodási folyamatot, és kisebb kristályokat eredményezett.
Üledékes kőzet – Olyan kőzet, amely a korábban kialakult kőzetekből erodálódott anyagok lerakódásának eredményeként alakult ki az óceánok, folyók, tavak stb. feneke mentén, a vízből származó ásványok lerakódásával együtt. Az évek során ezek a lerakódások a természeti erők hatására tömörödnek, és később szilárd masszává (kőzetté) szilárdulnak.

Ez egy üledékes kőzetképződmény, amely a kaliforniai Death Valleyben található Zabriskie Point része. A nagyjából 5 millió évvel ezelőtt kiszáradt Furnace Creek-tó üledékeiből áll. Az évmilliókig tartó erózió következtében az üledékrétegek szabadon maradtak.
Metamorf kőzet – Olyan kőzet, amely akkor keletkezett, amikor a meglévő üledékes vagy vulkáni kőzeteket olyan nyomásnak és bizonyos esetekben hőmérsékletváltozásnak tették ki, amely megváltoztatta az eredeti ásványi összetételüket.

Metamorf kőzet, amelyet “gránit gneisz” néven ismerünk. Metamorfizált gránitból keletkezett.
Hogyan alakulnak ki a szervetlen kristályok?
A kristályok különböző folyamatok eredményeként alakulhatnak ki, többek között:
Evaporit lerakódások – Ezek olyan ásványi képződmények, amelyek a földfelszíni folyamatok eredményeként jönnek létre. A kristályok olyan ásványokat tartalmazó oldatokból alakulnak ki, amelyek egy vizes oldat kiszáradása/elpárolgása révén koncentrálódnak. Ahogy a folyadék a párolgás révén lassan távozik, a koncentrált ásványok összegyűlnek és a vízből strukturált mintázatban kicsapódnak, amely kristállyá alakul. A kicsapódási lerakódásokra példa a rózsaszín halitkristályok a kaliforniai Trona-ban található Seamless-tóból.
Szekunder ásványi lerakódások – Ezek az elsődleges ércek vízzel való érintkezése során, hidrotermális oldatokból történő lerakódás révén alakulnak ki, vagy magma kristályosodásával keletkeznek.
- Elsődleges ércekkel való érintkezés – A kőzeteken keresztül lefelé szivárgó víz által a feltárt ércekhez (jellemzően egy üregben) kerülő víz. Ez olyan kémiai folyamatokat indíthat el, amelyek lebontják az ércet, és az ásványokat a nyitott üregfalak mentén újraelosztják. Erre jó példa az azurit és a malachit, ahol a vizes oldatok áthatoltak az elsődleges rézérc területein, és azokat azurit- és malachitkristályokként újraelosztották, amelyek kialakulási követelményei között víz, karbonátok és réz is szerepel.
- Hidrotermális fluidumok lerakódása – a legtöbb esetben úgy történik, hogy a hidrotermális fluidumok felfelé haladnak a kőzetben, és közben ásványokat vesznek fel a környező kőzetben. Amikor egy nyitott üregbe kerülnek ezek a fluidumok, az ásványok kristályok és/vagy szilárd tömeg formájában kicsapódhatnak. Időnként a környező kőzetben lévő ásványok kicserélődhetnek, ezt az eseményt nevezzük csere-lelőhelynek.
- A magma kristályosodása – akkor következik be, amikor a magma lehűl, és a magmában lévő ásványok elkezdenek szétválni hasonló és kompatibilis ásványok csoportjaira. A lehűlés sebességétől, az összetételtől és a légkörtől függően a kristályok mérete jelentősen változhat. Néha a lehűlés túl gyorsan történhet, ami az elemi szerkezet hiányát eredményezi, erre példa az obszidián (vulkáni üveg). Az obszidián elsősorban SiO₂-ból (a legtöbb esetben kvarcból) áll, kémiai képlete alapján kristály/ásvány lehet, azonban a kristályos szerkezet hiánya és az összetétel változékonysága miatt inkább mineraloidnak minősül.

A mineraloid, obszidián.
Ásványi osztályok
Az ásvány kémiai összetétele határozza meg, hogyan fog előfordulni a természetben. Néhány gyakori ásványi osztály a kémiai összetételük alapján:
Natív ásványok – A természetben előforduló elemek, amelyek önálló ásványi szerkezettel és más elemmel való kombináció nélkül fordulnak elő. Néhány példa azokra az elemekre, amelyekről ismert, hogy natív ásványokként képződnek: arany (Au), ezüst (Ag), kén (S), réz (Cu), grafit ((C) – laza kötésű szén) és gyémánt ((C) – sűrű kötésű szén – jellemzően tartalmaz némi szennyeződést).

Kemény természetes gyémánt

Natív ezüst

Natív réz
Oxidok – Olyan kémiai vegyületosztály, amelyben egy oxigénion (O2-) párosodik egy elemmel, sok esetben egy pozitív töltésű fémmel. Néhány példa erre: SiO₂ – kvarc, Fe₂O₃ – hematit, Cu₂O – kuprit stb.
Karbonátok – Ásványok, amelyeket egy karbonátion (CO₃2-) jelenléte jellemez. Jellemzően fémkationokhoz kötődik, amelyek a legtöbb esetben oldhatatlan vegyületeket alkotnak (vízben nem oldódnak). Néhány példa erre: CaCO₃ – Kalcit/Aragonit, FeCO₃ – Sziderit, ZnCO₃ – Smithsonit stb.
Szilikátok – Az anionok családjába tartozó ásványok, amelyek szilíciumot (Si) és oxigént (O) is tartalmaznak. Ez a só az egész litoszférában (földkéreg) a kőzetek fő alkotóelemét képezi. Néhány példa a szilikátokra: SiO₂ – Kvarc, AlKO₆Si₂ – Kálium-alumínium-szilikát, (Fe,Mg)₂SiO₄ – Olivin stb.
Szulfid (szulfid) – A kén szervetlen anionja, amely az S^2- kémiai képlettel rendelkezik, és meglehetősen bonyolultnak tekinthető reakciókkal járhat. A szulfidok kicsapódása magában foglalhatja a nehézfémekkel való reakciókat, amelyekben oldhatatlan fémcsapadékok keletkeznek. Néhány példa ezekre a szulfidionokból képződő nehézfémekre: FeS₂ – pirit, CuFeS₂ – kalcopirit, PbS – galenit stb.
Szulfátok (szulfátok) – Sók, amelyek a kénsav (H₂SO₄) és egy másik vegyi anyag reakciójában keletkeznek. Néhány példa a szulfátokra: (Ba,Sr)SO₄ – Barit (Baryte), CaSO₄- 2H₂O – Gipsz, SrSO₄ – Celesztin (Celestite) stb.
Foszfátok – A komplex anion (PO₄)^3-. jelenlétével jellemezhető ásványok, amelyek többsége a természetben meglehetősen ritkának számít. Néhány példa a foszfátokra: Ca5(PO₄)(OH,F,CL) – Apatit, CuAl₆(PO₄)₄(OH)₈ – 4H₂O – Türkiz, Fe(II)3(PO4)₂- 8H2O – Vivianit, stb.
A kristályok és ásványok gazdaságossága
A modern korban ahhoz, hogy egy ásványt gazdaságilag érdemesnek tekintsünk a bányászatra, a hasznos ásványok olyan koncentrációjának kell léteznie, amelyet úgy lehet megmunkálni (bányászni), hogy közben még nyereséget is lehet elérni. A koncentrációnak is elég magasnak kell lennie ahhoz, hogy a kitermelés kifizetődő folyamat legyen. Néha a bányán belül a végéhez érő ásvány a bánya azonnali bezárását eredményezheti. Emiatt a bányászat gazdaságossági szempontból extra kockázatos üzlet lehet.
A fémek jelenleg a legfontosabb gazdasági ásványok, mivel a legkülönbözőbb modern alkalmazásokban használják őket. Ezeket a fémeket fémtartalmú lelőhelyekről nyerik ki, amelyek az ércből (a keresett ásványokból) és a legtöbb esetben a nemkívánatos, kevésbé gazdaságos környező ásványokból, az úgynevezett “üledékből” állnak.
Terminológia és illusztrációk
Kémiai elem – A kémiai elem olyan anyag, amelynek minden atomja azonos számú protont tartalmaz, amit atomszámnak nevezünk. A periódusos rendszer bizonyos értelemben egy kulcs, amelyet Dimitrij Mendelejev orosz kémikus állított össze, hogy ezeket az atomokat protonszámuk alapján elemkategóriákba sorolja. Például a hidrogén (H) atom egy protont tartalmaz, a hélium (He) atom két protont, a lítium (Li) atom három protont, és így tovább, és így tovább.
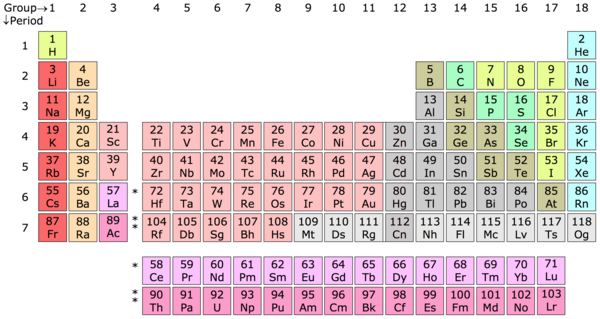
Szakaszos táblázat
Kémiai vegyület – Molekulákból áll. Ahhoz, hogy kémiai vegyületnek tekintsük, a molekulának legfeljebb kettőnél több különböző kémiai elemből kell állnia, amelyek egymáshoz kapcsolódnak.
Atom – Egy kémiai elem legkisebb egysége. Az atom proton(ok)ból, elektron(ok)ból és neutron(ok)ból áll, amelyek együttesen határozzák meg az atom töltését. Az atomok elektronokat veszíthetnek vagy nyerhetnek, ami pozitív és negatív töltéseket, úgynevezett ionokat eredményez.
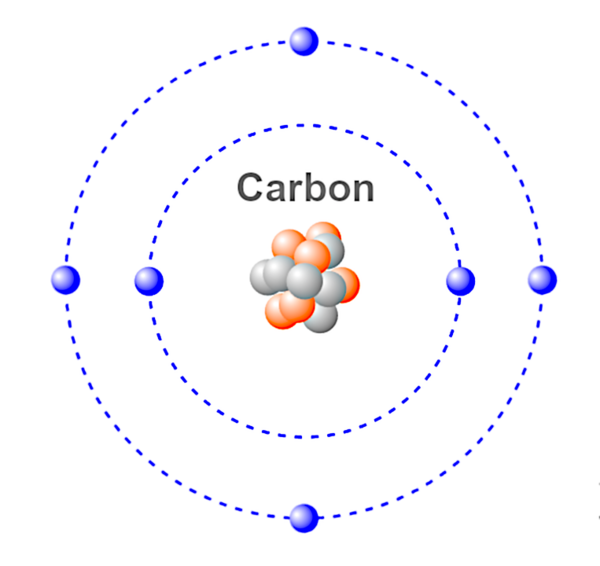
Ez egy szénatom illusztrációja.
Kék – elektronok.
Vörös & Szürke – Neutronok & Protonok.
Ion – Egy vagy több elektron elvesztéséből vagy nyereségéből származó elektromos töltéssel rendelkező atom vagy molekula.
Kation – Pozitív töltésű ion, amely vonzódik a negatív töltésű ionokhoz. Példa – Hidrogénion H+.
Anion – Negatív töltésű ion, amely pozitív töltésű ionokhoz vonzódik. Példa – Karbonátion CO₃2-.

Karbonátion kémiai képlete.
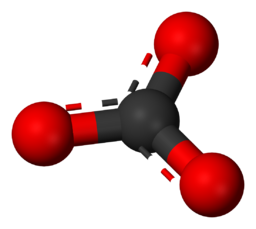
Ez a kép a karbonátion (CO₃2-) molekuláris szerkezetét szemlélteti atomi szinten.