1Introduction
L’ingestion de substances corrosives reste un problème de santé publique important principalement dans les pays en développement. Les enfants représentent 80% des cas dans le monde, principalement en raison d’une ingestion accidentelle.1 Les substances caustiques peuvent provoquer une sténose œsophagienne sévère. La gestion des sténoses œsophagiennes a évolué et le développement des techniques endoscopiques a conduit à une gestion plus conservatrice, plutôt qu’à une substitution chirurgicale plus agressive.
La dilatation endoscopique (par ballonnet ou bougienage) est utilisée dans le monde entier, bien qu’environ un tiers des patients développent des sténoses récurrentes après dilatation (définies comme une incapacité à maintenir un diamètre luminal satisfaisant pendant quatre semaines) et d’autres présentent des sténoses réfractaires nécessitant de multiples dilatations (définies comme une incapacité à atteindre un diamètre luminal satisfaisant sur cinq séances à deux semaines d’intervalle).2,3 D’autre part, les dilatations endoscopiques présentent un risque significatif de perforation (15-20%) et de développement de nouvelles sténoses en raison de la pression élevée sur la paroi œsophagienne.4-6
Au cours de la dernière décennie, la pose de stents œsophagiens est devenue populaire. Plusieurs auteurs ont décrit leur expérience avec différents types de stents, bien que les dispositifs pédiatriques adaptés soient encore rares et que la majorité d’entre eux provoquent une force centrifuge sur la paroi œsophagienne tout en permettant le passage des aliments à l’intérieur du stent. Ce type de stents peut provoquer un étirement et une hypertrophie de la muqueuse, avec un risque non négligeable de migration, de perforation et d’occlusion.7-13
Depuis 1988, l’équipe de l’unité de chirurgie digestive et d’endoscopie de l’hôpital Bambino Gesù – Rome a développé un dispositif appelé « stent dynamique » (DS), qui permet le passage des aliments entre le stent et la paroi de l’œsophage, améliorant ainsi la motilité de l’œsophage et, par conséquent, prévenant la récidive de la sténose.13,14 Le DS est un dispositif en silicone personnalisé construit coaxialement sur une sonde nasogastrique pour atteindre la longueur et le diamètre souhaités, afin de créer une zone plus large adaptée pour être placée le long de la sténose. L’expérience publiée de deux décennies d’utilisation du DS confirme la sécurité et l’efficacité du dispositif et peut même être considéré comme la première option dans le traitement de la sténose caustique de l’œsophage.14,15
Nous décrivons le cas d’un patient présentant une double sténose caustique réfractaire de l’œsophage qui a été traitée avec un DS dans l’unité de gastroentérologie pédiatrique, Centre hospitalier de São João, Porto. Habituellement, les lésions caustiques sont plus sévères au site du rétrécissement fonctionnel de l’œsophage (au niveau du croisement des vaisseaux principaux ou juste au-dessus du cardia) et ont tendance à être uniques avec une longueur variable, mais il arrive qu’il y ait plus d’un site, comme dans le cas présent, ce qui entraîne un défi thérapeutique supplémentaire.
2Cas clinique
Un garçon de deux ans, auparavant en bonne santé, a ingéré accidentellement un liquide alcalin fort qui a entraîné une double sténose (à 5 cm de distance, à 15 et 20 cm de la bouche) de l’œsophage. Chacun des segments sténotiques était court (moins de 2 cm), mais la visibilité était limitée et il était difficile de les aborder tous les deux pour les dilater. Il a d’abord été traité par des dilatations endoscopiques avec des bougies (Savary-Gilliard) avec une récurrence de la dysphagie deux mois plus tard et même après d’autres dilatations par bougies. À certaines occasions, lorsqu’il y avait suffisamment de visibilité de la lumière œsophagienne à travers les deux segments sténotiques, des ballons TTS de 10 mm ont été utilisés, mais une fois qu’il y avait une perforation de la paroi œsophagienne, gérée avec succès avec des mesures conservatrices.
Plusieurs mois après la perforation, la dysphagie est réapparue avec un grade 1 (la dysphagie a été classée en utilisant une échelle précédemment décrite comme suit : grade 0=capable de manger un régime normal/aucune dysphagie ; grade 1=capable d’avaler certains aliments solides ; grade 2=capable d’avaler uniquement des aliments semi-solides ; grade 3=capable d’avaler uniquement des liquides ; grade 4=dysphagie totale),16 qui a évolué vers le grade 3 douze mois plus tard. Les dilatations endoscopiques (initialement avec des bougies Savary-Gilliard et ensuite avec des ballons TTS) ont été reprises à intervalles de deux semaines. La mitomicine C topique a été appliquée pendant quatre séances consécutives, initialement à 0,1 mg/mL, puis portée à 1 mg/mL. Cependant, la sténose est restée réfractaire et de multiples séances de dilatation (plus de 30, largeur maximale 12mm) pendant 18 mois.
Trois ans après l’accident initial, une DS a été envisagée. Malgré une dysphagie significative (grade 3), le garçon a eu une croissance et une prise de poids adéquates, principalement grâce à l’ajustement de la consistance des aliments en fonction de sa tolérance. Une autorisation éthique a été obtenue et les parents ont donné leur consentement éclairé. L’emplacement exact et l’étendue de la sténose ont été préalablement évalués radiologiquement avec contraste (Fig. 1) et des marqueurs cutanés radio-opaques ont été appliqués. Les deux sténoses ont ensuite été dilatées jusqu’à l’obtention d’un calibre adéquat (avec des bougies Savary-Gilliard de 7 et 9 mm suivies d’un ballon de 12 mm) permettant la mise en place du stent (Fig. 2). Le DS a ensuite été inséré par la bouche et la position correcte a été confirmée radiologiquement avec le plus grand diamètre au niveau des sténoses en utilisant les marqueurs cutanés comme référence. La Fig. 3 montre le dispositif réel et le schéma de l’emplacement du dispositif après insertion. La sonde nasogastrique de l’endoprothèse a ensuite été passée avec un mouvement vers l’arrière à travers le nasopharynx et le nez, et fixée à l’extérieur avec du ruban adhésif pour éviter tout déplacement distal (Fig. 4). Le jour suivant, le patient a commencé à être alimenté par voie orale avec une alimentation molle qui a progressivement évolué vers une alimentation normale. Un traitement par inhibiteur de la pompe à protons (oméprazole 20mg id) et corticostéroïde (prednisone 1mg/kg/jour une fois par jour) a été maintenu pendant trois jours, selon le protocole publié.14,15
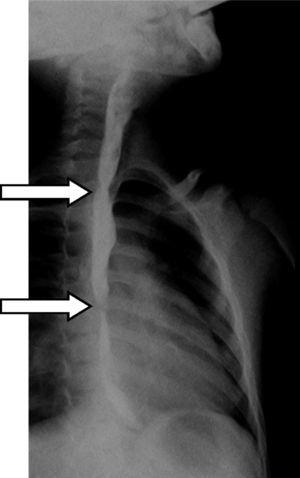
Esophagogramme montrant l’emplacement exact et l’étendue de la sténose (flèches).

Dilatation par ballonnet de la sténose avant la pose du stent.

Stent dynamique – aperçu de la version commerciale qui sera disponible sur le marché après l’approbation complète de l’agence réglementaire (à gauche) ; illustration schématique du placement intra-œsophagien du dispositif (à droite).
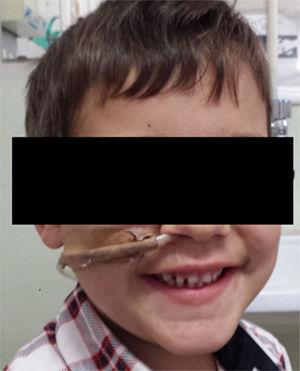
Patient avec le stent dynamique illustrant la fixation extérieure.
Le stent a été retiré après sept semaines sous anesthésie générale avec contrôle endoscopique de la paroi œsophagienne. À ce moment-là, le patient mangeait des solides sans dysphagie (grade 0). L’endoscopie supérieure réalisée après le retrait de l’endoprothèse a montré une lumière œsophagienne adéquate sans aucune ulcération (Fig. 5). L’ensemble du processus et le dispositif ont été bien tolérés sans événements indésirables.

Aspect endoscopique de la muqueuse œsophagienne après retrait de l’endoprothèse (A – sténose distale ; B – sténose proximale).
Plus d’un an après, le patient reste asymptomatique lors d’une alimentation orale normale (pas de dysphagie – grade 0).
3Discussion
L’utilisation de stents pour les sténoses œsophagiennes a évolué rapidement au cours des 10 dernières années et elle est largement pratiquée chez les adultes, notamment pour le traitement des sténoses malignes17. Plus récemment, la pose temporaire de stents a été de plus en plus utilisée pour les sténoses œsophagiennes bénignes réfractaires2.
Les stents métalliques auto-expansibles (SEMS) ont été les premiers dispositifs utilisés,18 mais ils ont été associés à un taux de complication élevé, principalement dû à l’incrustation de tissus hyperplasiques (jusqu’à 80 %) et à un taux de migration de 26,4 %.17,19 Pour surmonter ce problème, les SEMS entièrement couverts semblent préférables, mais actuellement les données sur leur utilisation dans les sténoses œsophagiennes bénignes réfractaires sont encore limitées20.-23
Les endoprothèses plastiques auto-expansibles (SEPS) ont été proposées comme alternative aux SEMS. Deux revues récentes, ont trouvé un taux de réussite clinique de seulement 45-52% avec l’utilisation des SEPS pour le traitement des sténoses œsophagiennes bénignes chez 172 et 130 patients, respectivement, avec un taux de migration significatif de l’endoprothèse de 24-31%.24,25 Bien qu’efficace, la conception des SEPS doit encore être améliorée pour réduire le risque de migration.
Une autre option de traitement qui a été plus récemment introduite est l’endoprothèse biodégradable. Seuls des rapports de cas et un petit nombre d’études de cohorte sur l’utilisation de stents biodégradables ont été publiés et la majorité d’entre eux ne concernaient que peu de patients.26-28 Les études les plus importantes portant sur 20-30 patients présentant des sténoses œsophagiennes bénignes réfractaires ont montré un taux de récurrence de la dysphagie de 50-75% après six mois de suivi avec la nécessité de répéter la procédure de pose de stent.29-31 Ce taux de récurrence pourrait s’expliquer par la force radiale relativement faible et la nature dégradable de ces stents. En 2011, une comparaison directe non randomisée entre les stents biodégradables et les SEPS a révélé un soulagement similaire à long terme de la dysphagie (33% et 31%, respectivement) chez les patients présentant des sténoses œsophagiennes bénignes réfractaires.32
La première étude la plus importante sur l’utilisation des stents dans la population pédiatrique a été publiée en 1996, elle comprenait 69 enfants présentant des sténoses œsophagiennes corrosives et a montré une différence significative entre l’utilisation des stents et le traitement traditionnel (68% contre 83% de taux de guérison). Les stents ont été laissés en place pendant un an sans complications sérieuses.33
Malgré ces résultats prometteurs, jusqu’à présent le nombre d’études publiées sur l’utilisation des stents dans la population pédiatrique est encore rare, la majorité inclut également des adultes et l’utilisation spécifique dans les sténoses corrosives est limitée à des séries de cohortes qui incluent des sténoses œsophagiennes bénignes d’autres étiologies. Manfredi et al. ont traité 24 enfants présentant une sténose œsophagienne anastomotique après réparation d’une atrésie œsophagienne et le succès clinique n’était que de 39 % à 30 jours et de 26 % à 90 jours, avec une récidive élevée de la sténose après le retrait du stent. Les résultats étaient indépendants du type de stent utilisé (ils comprenaient les stents Polyflex pour les voies aériennes, les stents trachéobronchiques entièrement couverts AERO et les stents œsophagiens entièrement couverts ALIMAXX-ES).34 Récemment (2015), Lange et al. ont publié leur expérience de l’utilisation de SEMS entièrement couverts chez des enfants présentant des sténoses œsophagiennes bénignes de différentes étiologies (mais aucun avec des sténoses corrosives). Entre 2006 et 2014, 11 enfants ont été traités avec un SEMS (stents commercialisés biliaires, bronchiques et coliques). Lors du suivi, 55 % ont été traités avec succès sans autre intervention, mais 36 % ont dû subir un resting au maximum quatre fois et 27 % ne se sont pas améliorés, nécessitant une intervention chirurgicale. Ils n’ont rapporté que deux migrations d’endoprothèse.35 Zhang et al. ont utilisé une nouvelle SEMS entièrement couverte avec des connecteurs intermittents afin de réduire la migration de l’endoprothèse et ils ont été fabriqués sur mesure pour chaque patient. Bien que les résultats aient été décevants : parmi les cinq patients présentant une resténose œsophagienne postopératoire, une sténose ulcéreuse a été observée chez deux patients et une migration de l’endoprothèse s’est produite chez trois d’entre eux.36 Le premier rapport sur l’utilisation d’une endoprothèse biodégradable chez un enfant a été fait par Vandenplas et al. en 2009, mais après quatre mois sans symptômes, le patient a développé une sténose œsophagienne distale sévère.37 Plus récemment (2013), une série de cas rétrospective de sept patients présentant des sténoses œsophagiennes caustiques comprenait deux enfants (5 et 14 ans) qui ont été traités avec une endoprothèse biodégradable. Tous deux ont dû subir de multiples dilatations après la pose de l’endoprothèse (10-12 procédures) en raison d’une dysphagie récurrente.28
Comme les résultats de la pose d’endoprothèses œsophagiennes ne sont pas optimaux et qu’il n’existe pas d’endoprothèses œsophagiennes spécialement conçues pour les enfants disponibles dans le commerce, d’autres types de dispositifs sur mesure ont été utilisés. Woynarowski et al. ont développé un tube spécifique à double lumière, de diamètre variable, perforé, de protection de la fermeture de l’œsophage, construit de manière coaxiale sur une fine sonde naso-gastrique. Ce dispositif a été utilisé chez deux patients présentant une sténose œsophagienne réfractaire après une blessure caustique. Malgré les bons résultats cliniques, l’utilisation à long terme d’une sonde nasogastrique (5-9 mois) a été nécessaire et les résultats après le retrait du dispositif dans un cas n’ont pas été rapportés.38,39
Dans l’ensemble, l’utilisation rapportée de l’endoprothèse par la force physique chez les patients pédiatriques n’est toujours pas optimale. Une approche différente consistant à insérer un dispositif sans pression à travers la sténose et une « dilatation » intermittente effectuée par la nourriture avalée semble être une idée attrayante qui réduit la pression pure et continue du dispositif et le risque de migration. À cet égard, le DS semble être le dispositif pédiatrique ayant inclus un plus grand nombre de patients. L’expérience publiée en 2011 incluait 80 enfants âgés de 3 mois à 10 ans, la majorité (55) présentant une sténose œsophagienne caustique. Les sténoses ont été traitées avec succès dans 88,6 % des cas et 50 % n’ont nécessité qu’une seule procédure de pose de stent.14 Les complications décrites étaient essentiellement liées à un déplacement partiel du stent dans 14,7 % des cas et à la migration du stent dans l’estomac dans seulement deux cas qui ont été facilement récupérés par endoscopie.14 Ces taux de complications sont largement inférieurs à ceux décrits pour les stents conventionnels avec un taux de migration de 24-31 % avec la nécessité d’une intervention chirurgicale pour la récupération du stent dans un nombre non négligeable de cas.19,24,25,34,40 Le temps médian de pose de la sonde nasogastrique était plus court (39 jours avec un maximum de 65 jours) par rapport aux autres dispositifs et, même si la sonde nasogastrique a un fort impact psychologique, elle était bien tolérée avec une bonne observance par les enfants et les parents14. En 2013, ce groupe a publié son expérience de l’utilisation de la DS dans la sténose postopératoire chez 26 enfants atteints d’atrésie de l’œsophage et le taux de réussite était de 80,7% avec un suivi moyen de 5,4 ans.15
En conclusion, à l’heure actuelle, l’accord pour le traitement de la sténose œsophagienne chez les patients pédiatriques est faible et les raisons sont variées. Il s’agit notamment des petites séries de cas qui ont été analysés et de la rareté des dispositifs pédiatriques dédiés.1,14,34-36 A l’avenir, des études prospectives et multicentriques seront nécessaires pour optimiser les indications et les protocoles de pose de stent œsophagien chez les patients pédiatriques après ingestion de substances corrosives.
Nous souhaitons signaler l’utilisation du DS comme une option valable dans le traitement de la sténose œsophagienne récurrente comme moyen d’éviter la chirurgie, sans doute beaucoup plus agressive. Ce dispositif représente un nouveau concept de dilatation fonctionnelle et mérite d’être considéré dans tous les cas de sténose œsophagienne récurrente après les procédures de dilatation initiales habituelles. Bien qu’il ait été décrit depuis quelques années, les publications d’utilisation de ce type de dispositif sont encore limitées à leurs développeurs, dérivées du fait qu’ils ont été fabriqués sur mesure en interne, mais une version commerciale sera bientôt disponible sur le marché.
Divulgations éthiquesProtection des sujets humains et animaux
Les auteurs déclarent qu’aucune expérience n’a été réalisée sur des humains ou des animaux pour cette étude.
Confidentialité des données
Les auteurs déclarent qu’aucune donnée sur les patients n’apparaît dans cet article.
Droit à la vie privée et au consentement éclairé
Les auteurs déclarent qu’aucune donnée sur les patients n’apparaît dans cet article.
Conflits d’intérêts
Les auteurs n’ont aucun conflit d’intérêts à déclarer.