Introduction
La péricardite constrictive (PC) est une maladie de plus en plus reconnue, aux causes diverses, caractérisée par un péricarde fibrotique, épaissi. Parfois, un péricarde calcifié est observé avec un encastrement du cœur empêchant le remplissage diastolique . Il est difficile d’établir un diagnostic correct sur la seule base de données cliniques ; le diagnostic provisoire doit être confirmé par une imagerie multimodale non invasive comprenant une échocardiographie bidimensionnelle (2D) et Doppler comme technique de premier choix, qui peut être complétée par une tomographie assistée par ordinateur (CT) et une imagerie par résonance magnétique (IRM) dans certains cas. Les mesures hémodynamiques invasives deviennent utiles lorsque l’imagerie ne fournit pas d’informations diagnostiques adéquates ou nécessite une caractérisation plus poussée. La cardiomyopathie restrictive (MRC) est une maladie aux causes diverses qui affecte la fonction myocardique soit par un dysfonctionnement primaire des myocytes et/ou par une infiltration extracellulaire ou une fibrose. Les deux maladies, la PC et la MRC, entraînent une insuffisance cardiaque diastolique avec un remplissage ventriculaire anormal et des caractéristiques cliniques similaires. La différenciation précise de la PC et de la MRC peut être un défi diagnostique même pour le clinicien expérimenté, mais elle est d’une importance capitale, car la PC est une maladie potentiellement curable, alors que dans la MRC le pronostic est mauvais en raison des options thérapeutiques limitées. Cependant, les progrès récents de l’échocardiographie et d’autres modalités d’imagerie ont rendu cette tâche auparavant difficile beaucoup plus facile.
Pathophysiologie
L’enveloppe fibrotique autour du cœur dans la PC affecte l’hémodynamique cardiaque de deux façons différentes. Premièrement, il y a une dissociation entre les pressions intrathoraciques et intracardiaques. Habituellement, le gradient de pression de remplissage du ventricule gauche (la différence entre la pression du coin capillaire pulmonaire et la pression diastolique du ventricule gauche) reste constant pendant le cycle respiratoire. Dans le cas de la PC, la réduction inspiratoire de la pression intrathoracique est transmise aux veines pulmonaires extracardiaques, mais pas entièrement à l’oreillette et au ventricule gauches encastrés, ce qui entraîne une réduction du remplissage diastolique du VG avec l’inspiration. Deuxièmement, comme le volume sanguin total des quatre cavités cardiaques reste relativement constant, l’interdépendance ventriculaire est exagérée dans la PC. Avec la diminution inspiratoire du remplissage du ventricule gauche et du volume diastolique, le remplissage du ventricule droit est augmenté de manière compensatoire. Comme la veine cave supérieure, mais pas la veine cave inférieure, est sujette à des variations de pression intrathoracique, la plupart du flux vers l’oreillette droite à haute pression pendant l’inspiration arrive de la veine cave inférieure qui est également aidée par une augmentation de la pression transabdominale inspiratoire. Ceci explique physiologiquement l’augmentation paradoxale de la pression veineuse jugulaire lors de l’inspiration (signe de Kussmaul). À l’expiration, des changements opposés se produisent dans le remplissage du cœur droit et du cœur gauche. En revanche, la compliance péricardique est normale dans la MRC et la variation respiratoire des pressions intrathoraciques est transmise normalement aux chambres cardiaques. Avec l’inspiration, la pression du coin capillaire pulmonaire et la pression diastolique du VG sont abaissées de manière égale, laissant ainsi le gradient de pression pour le remplissage du VG presque inchangé.
Interdépendance ventriculaire
Hatle et al ont fourni un aperçu des changements respiratoires dynamiques dans le remplissage et les pressions ventriculaires qui se produisent chez les patients atteints de PC. Le concept d’interdépendance ventriculaire et les changements réciproques de la pression respiratoire dans le VR et le VG lors du cathétérisme cardiaque constituent un paramètre diagnostique utile. Chez les patients atteints de paralysie cérébrale, on observe généralement une augmentation de la pression systolique du ventricule droit pendant le pic d’inspiration, moment où la pression systolique du ventricule gauche est la plus faible. En revanche, on observe une diminution concordante des pressions systoliques du VR et du VG pendant le pic d’inspiration chez les patients atteints de MRC. L’interdépendance ventriculaire dans la PC peut également être évaluée par échocardiographie Doppler avec la courbe de vitesse de régurgitation tricuspide . Pendant l’inspiration, la pression systolique du VR augmente, de même que la durée de la systole du VR, car il faut plus de temps pour éjecter un volume accru du VR.
Échocardiographie bidimensionnelle
L’épaisseur normale du péricarde est de 2 mm ou moins. Un péricarde rigide et/ou épaissi est le substrat anatomique responsable de la physiologie constrictive. Malgré des rapports isolés sur l’utilité de l’échocardiographie en mode M et en 2D pour détecter un péricarde épaissi, la fiabilité de l’échocardiographie transthoracique à cette fin est discutable en raison des limites techniques, telles que la position du transducteur, le gain, les réglages des niveaux de gris et les réverbérations. En outre, la PC peut être principalement localisée dans une région du cœur. La résolution supérieure obtenue avec l’échocardiographie transoesophagienne permet une meilleure définition du péricarde. L’IRM et le scanner permettent également de mesurer avec précision l’épaisseur du péricarde. Cependant, les informations anatomiques ne reflètent pas nécessairement les anomalies physiopathologiques. De plus, la PC et l’épaississement du péricarde ne sont pas uniformément associés, car des patients peuvent avoir une PC prouvée chirurgicalement malgré une épaisseur péricardique normale . A l’inverse, un péricarde épaissi peut être présent sans caractéristiques constrictives, notamment chez les patients ayant subi une radiothérapie thoracique ou une chirurgie à cœur ouvert.
La fonction systolique myocardique évaluée par la fraction d’éjection du VG est préservée dans la PC. Le mouvement du septum interventriculaire respirophasique observé sur l’échocardiographie en mode M et en 2D est induit par des changements brusques du volume ventriculaire et reflète une interdépendance ventriculaire accrue. Le remplissage du ventricule gauche étant moindre au début de l’inspiration, le septum interventriculaire se déplace brusquement vers la gauche. À l’expiration, le VG se remplit mieux et le septum revient à une position normale. En outre, on observe fréquemment un discret « frémissement » du septum à chaque battement, indépendamment de la respiration, en raison des taux de remplissage différentiels des deux ventricules en diastole. L’hypertrophie biatriale et la congestion veineuse systémique (pléthore de la veine cave inférieure) sont des constatations non spécifiques, car elles sont rencontrées à la fois dans la PC et la MRC.
Échocardiographie Doppler à ondes pulsées
Parce que la pression diastolique du VG est élevée et que la quasi-totalité du remplissage ventriculaire du VG se produit au début de la diastole, la vitesse de l’onde E mitrale est augmentée et le temps de décélération raccourci (généralement <160 ms) avec une onde A petite ou absente ressemblant à un modèle d’afflux restrictif qui est observé à la fois dans la PC ainsi que dans la MRC. Hatle et al ont été les premiers à décrire les caractéristiques du flux Doppler mitral et tricuspide qui sont utilisées pour différencier la constriction de la restriction. Lors de l’inspiration, la dissociation des pressions intrathoraciques et intracardiaques entraîne une diminution de la pression motrice initiale pour le remplissage du ventricule gauche. Par conséquent, on observe une diminution de la vitesse maximale de l’onde E mitrale de >25 % pendant le premier battement de l’inspiration, ainsi qu’une prolongation du temps de relaxation isovolumique (généralement >20 %). L’interdépendance ventriculaire est responsable de changements réciproques dans le schéma d’écoulement trans-tricuspide avec une augmentation inspiratoire de la vitesse maximale de l’onde E de >40%. Des changements inverses se produisent à l’expiration dans les deux ventricules. D’autres chercheurs ont rapporté des résultats caractéristiques des changements respiratoires dans les veines pulmonaires et les veines hépatiques. En termes simplifiés, le flux diastolique vers le cœur gauche diminue avec l’inspiration, tandis que des changements opposés sont observés pour le cœur droit. Cependant, des études ultérieures de plus grande envergure ont découvert l’absence de variation respiratoire de l’influx mitral chez un tiers des patients atteints de PC .
Les résultats du Doppler peuvent être trompeurs dans certains cas. Premièrement, chez les patients présentant un rythme irrégulier (par exemple, une fibrillation auriculaire), des changements respirophasiques peuvent encore être observés, mais ils sont facilement confondus par l’intervalle RR variable. Deuxièmement, une pression auriculaire gauche nettement élevée peut atténuer la variation respiratoire de la vitesse de l’E mitral en raison d’un gradient de pression élevé persistant et d’un retour veineux vers le cœur gauche. Les manœuvres qui diminuent la précharge peuvent démasquer la variation Doppler respiratoire caractéristique. Troisièmement, une fluctuation respiratoire considérable de la pression intrathoracique, telle que celle observée dans la bronchopneumopathie chronique obstructive (BPCO), peut imiter la variation respiratoire des vitesses d’entrée mitrale et tricuspide rencontrée dans la PC. Cependant, le rapport E/A est plus faible, le temps de décélération est plus prolongé et l’interrogation Doppler de la veine cave supérieure montre une augmentation marquée du flux systolique inspiratoire vers l’avant, ce qui n’est pas observé chez les patients atteints de PC .
Doppler tissulaire et imagerie de déformation myocardique
L’échocardiographie 2D de base montre souvent un anneau mitral hyperdynamique avec un mouvement exagéré chez les patients atteints de PC . Ce phénomène peut être reconnu à l’œil nu sur des images en niveaux de gris, mais il est mieux apprécié par l’imagerie Doppler tissulaire. En général, une vitesse e’ de l’anneau mitral ³8 cm/s représente un point de coupure d’amplitude discret pour distinguer la PC de la MRC, peut-être en raison d’une plus grande contribution du mouvement longitudinal du ventricule gauche pour le remplissage diastolique et la relaxation normale du VG. En outre, en raison de l’attache du péricarde adjacent fibrotique et cicatrisé, qui influence la translocation latérale de l’anneau mitral chez les patients atteints de PC, la vitesse e’ latérale est inférieure à la vitesse e’ médiale, un phénomène appelé annulus reversus , qui est présent dans jusqu’à 75 % des PC prouvées chirurgicalement .
Pour la même raison, le dysfonctionnement épicardique marqué dans la PC entraîne une altération du raccourcissement circonférentiel (également appelé strain), et de la mécanique de torsion, alors que la déformation myocardique sous-endocardique (strain longitudinal) est bien préservée dans la PC, mais significativement réduite dans la MRC, affectant principalement les fibres sous-endocardiques orientées dans une direction longitudinale . Ces deux modèles distincts dans la mécanique longitudinale et circonférentielle du VG sont facilement évaluables par le suivi de speckle 2D, une technique relativement indépendante de l’angle qui suit les caractéristiques intramyocardiques uniques dans les images en mode B en échelle de gris, appelées speckles.
Il existe une relation inverse entre le rapport des vitesses transmitrales précoces et annulaires (E/e’) et les pressions de remplissage du VG (l’annulus paradoxus et le rapport E/e’ ne doivent pas être utilisés pour estimer les pressions de remplissage du VG chez les patients atteints de PC). L’explication plausible de ce résultat est le mouvement longitudinal exagéré de l’anneau mitral, malgré des pressions de remplissage élevées. En tant que mesure secondaire, la propagation du flux en mode M couleur du remplissage du ventricule gauche peut aider au diagnostic différentiel entre la PC et la MRC. La vitesse d’écoulement du premier aliasing est habituellement normale ou nettement augmentée (habituellement >100 cm/s) dans la PC, mais significativement plus faible dans la MRC .
La fibrillation auriculaire est une complication de la PC et de la MRC et rend difficile l’évaluation des changements respiratoires dynamiques par échocardiographie Doppler. La variation de la vitesse du flux mitral est plus liée à la longueur du cycle cardiaque qu’à la phase respiratoire, mais dans les veines hépatiques, les inversions de flux diastoliques restent proéminentes pendant l’expiration . Les vitesses annulaires mitrales mesurées par Doppler tissulaire restent également un paramètre fiable .
Récemment, un algorithme à facettes multiples avec cinq résultats échocardiographiques clés, y compris le mouvement septal ventriculaire lié à la respiration, le modèle de flux entrant mitral, la vitesse e’ annulaire mitrale médiale (septale) et l’inversion du flux diastolique expiratoire de la veine hépatique a été proposé qui est également applicable aux patients en fibrillation auriculaire . Les principales caractéristiques échocardiographiques sont énumérées dans le tableau 1 et les résultats Doppler typiques sont affichés dans la figure 1.
Tableau 1. Principales caractéristiques échocardiographiques de la péricardite constrictive.
- Déplacement septal ventriculaire respiratoire (également appelé rebond septal)
- Vitesse accrue de l’onde E mitrale et rapport E/A >1.6 (en expiration)
- Variation respiratoire de la vitesse de pointe de l’onde E mitrale (au moins 1,5 mm).(au moins >15%)
- Inversion du flux diastolique expiratoire dans les veines hépatiques
- Vitesse diastolique précoce (e’) de l’anneau mitral médian conservée ou exagérée (³9 cm/s)
- Vitesse e’ médiale égale ou supérieure à la vitesse e’ de l’anneau mitral latéral (annulus reversus)
- Déformation myocardique circonférentielle contrainte et longitudinale préservée (strain)
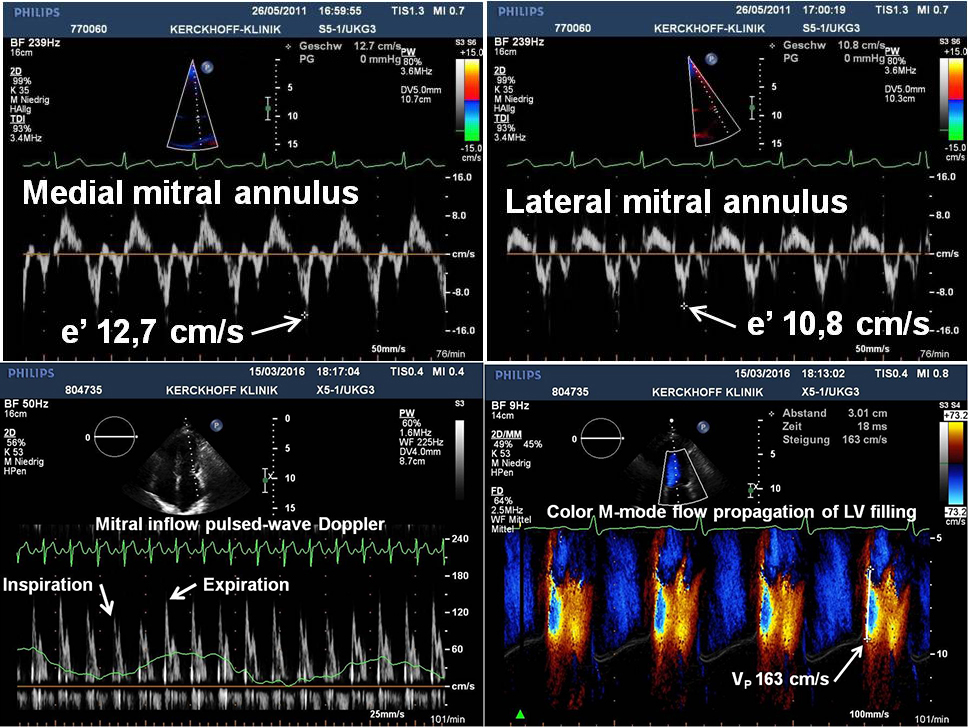
Figure 1. Résultats Doppler typiques d’un patient présentant une péricardite constrictive prouvée chirurgicalement. Les vitesses diastoliques précoces (e’) de l’anneau mitral médial (en haut à gauche) et latéral (en haut à droite) par Doppler tissulaire montrent une fonction longitudinale préservée et une inversion de la relation habituelle (dite annulus reversus). Le spectre Doppler à ondes pulsées des vitesses de l’influx mitral (en bas à gauche) montre une variation respiratoire marquée de la vitesse de pointe de l’onde E. La propagation du flux en mode M du Doppler couleur du remplissage du ventricule gauche (VG) (en bas à droite) illustre une pente abrupte (163 cm/s) du premier contour de vitesse d’aliasing (ligne blanche).
Incertitudes diagnostiques : constriction et restriction mixtes
Après une radiothérapie thoracique, une CP, une MRC, une maladie valvulaire, une coronaropathie prématurée ou une combinaison de ces éléments peuvent se développer. Ces caractéristiques qui se chevauchent représentent un autre défi dans le diagnostic différentiel entre la PC et la MRC et rendent nécessaire de déterminer si les anomalies sont causées par la contention péricardique, la restriction myocardique, ou les deux. Si une maladie péricardique et myocardique concomitante est présente, la décision de procéder à une péricardiectomie dépend du degré auquel le péricarde anormal contribue à l’augmentation des pressions intracardiaques.
Directives futures
Les techniques d’imagerie cardiaque actuellement disponibles ont la capacité de générer une vaste quantité de données structurelles et fonctionnelles cardiaques, dont seule une fraction est utilisée par le clinicien interprète pour établir un diagnostic et prendre une décision clinique. Une solution potentielle pour relever ce défi est d’appliquer une approche cognitive d’apprentissage automatique pour aider à la différenciation de la PC de la MRC .
Conclusions
La PC est caractérisée par l’encastrement du cœur par un péricarde rigide non souple, ce qui entraîne une altération du remplissage diastolique. Une compréhension des anomalies physiopathologiques caractérisées par une dissociation entre les pressions intrathoraciques et intracardiaques et une interdépendance ventriculaire exagérée est essentielle au diagnostic précis et à la différenciation de la MRC. L’échocardiographie serait considérée comme la modalité diagnostique de première ligne et le décalage septal ventriculaire lié à la respiration comme un point de départ très sensible. Un mouvement annulaire mitral préservé, voire accéléré, chez un patient présentant des symptômes d’insuffisance cardiaque, ainsi qu’une inversion de la relation entre les vitesses Doppler du tissu annulaire latéral et médial (également appelée annulus reversus) doivent alerter le clinicien interprète du diagnostic de PC. Le Doppler conventionnel à ondes pulsées de la vitesse du flux mitral de pointe diastolique précoce montre souvent une diminution marquée de l’inspiration. Bien que ces résultats Doppler soient généralement diagnostiques, il existe des résultats faussement positifs et faussement négatifs, et aucun paramètre échocardiographique unique ne doit être utilisé de manière exclusive, au profit d’une approche multidimensionnelle. En outre, l’imagerie multimodale par tomodensitométrie et CMR peut aider à délimiter l’épaisseur du péricarde, bien qu’elle ne prouve pas sa signification physiologique, et l’augmentation de l’épaisseur du péricarde n’est pas une caractéristique diagnostique essentielle de la PC. Lorsqu’une étude échocardiographique transthoracique complète permet de diagnostiquer une constriction, aucun autre test diagnostique ne devrait être nécessaire. Dans les cas équivoques, lorsque l’évaluation non invasive n’est pas concluante ou discordante avec les résultats cliniques, une évaluation hémodynamique par cathétérisme cardiaque doit être réalisée.