(CNN) Si vous avez la malchance qu’un serpent venimeux plante ses crocs en vous, votre meilleur espoir est un antivenin, qui est fabriqué de la même manière depuis l’époque victorienne.
Il s’agit de traire le venin de serpent à la main et de l’injecter à des chevaux ou à d’autres animaux à petites doses pour provoquer une réponse immunitaire. Le sang de l’animal est prélevé et purifié pour obtenir des anticorps qui agissent contre le venin.
Produire un antivenin de cette manière peut devenir désordonné, sans parler du danger. Le processus est sujet aux erreurs, laborieux et le sérum fini peut entraîner de graves effets secondaires.
Les experts réclament depuis longtemps de meilleurs moyens de traiter les morsures de serpent, qui tuent quelque 200 personnes par jour.
Maintenant — enfin — les scientifiques appliquent la recherche sur les cellules souches et la cartographie du génome à ce domaine de recherche longtemps ignoré. Ils espèrent que cela fera entrer la production d’antivenin dans le 21e siècle et sauvera finalement des milliers, voire des centaines de milliers, de vies chaque année.
Des chercheurs néerlandais ont créé en laboratoire, à l’aide de cellules souches, des glandes productrices de venin du serpent du Cap et de huit autres espèces de serpents. Les toxines produites par les répliques miniatures en 3D des glandes des serpents sont pratiquement identiques au venin du serpent, a annoncé l’équipe jeudi.
Dans une avancée parallèle, des scientifiques indiens ont séquencé le génome du cobra indien, l’un des « quatre grands » serpents du pays, responsable de la plupart des 50 000 décès par morsure de serpent que connaît l’Inde chaque année.
« Ils ont vraiment fait avancer les choses », a déclaré Nick Cammack, chef de l’équipe chargée des morsures de serpent à l’organisme britannique de recherche médicale Wellcome. « Ce sont des développements massifs parce que cela apporte la science 2020 dans un domaine qui a été négligé. »
Du cancer au venin de serpent
Hans Clevers, le chercheur principal de l’Institut Hubrecht pour la biologie du développement et la recherche sur les cellules souches à Utrecht, ne s’attendait pas à utiliser son laboratoire pour fabriquer du venin de serpent.
Il y a dix ans, il a inventé la technique permettant de fabriquer des organoïdes humains – des organes miniatures fabriqués à partir des cellules souches de patients individuels. Ils ont permis aux médecins de tester les effets spécifiques des médicaments en toute sécurité en dehors du corps, ce qui a révolutionné et personnalisé des domaines tels que le traitement du cancer.
 Les scientifiques ont reproduit la glande du venin du serpent corail du Cap, vu ici au zoo d’Olomouc, en République tchèque, le 11 mai 2018.
Les scientifiques ont reproduit la glande du venin du serpent corail du Cap, vu ici au zoo d’Olomouc, en République tchèque, le 11 mai 2018. Alors pourquoi avoir décidé de mettre en culture une glande à venin de serpent ?
Clevers a déclaré que c’était essentiellement un caprice de trois doctorants travaillant dans son laboratoire qui s’étaient lassés de reproduire des reins, des foies et des viscères de souris et d’humains. « Je pense qu’ils se sont assis et se sont demandé quel est l’animal le plus emblématique que nous pouvons cultiver ? Pas l’homme ou la souris. Ils ont dit que ça devait être le serpent. La glande à venin du serpent. »
« Ils ont supposé que les serpents auraient des cellules souches de la même manière que les souris et les humains, mais personne n’avait jamais étudié cela », a déclaré Clevers.
Après s’être procuré des œufs de serpent fécondés auprès d’un marchand, les chercheurs ont constaté qu’ils étaient capables de prendre un minuscule morceau de tissu de serpent, contenant des cellules souches, et de le nourrir dans un plat avec le même facteur de croissance qu’ils ont utilisé pour les organoïdes humains – bien qu’à une température inférieure – pour créer les glandes à venin. Et ils ont constaté que ces organoïdes de serpent — de minuscules boules d’à peine un millimètre de large — produisaient les mêmes toxines que le venin de serpent.
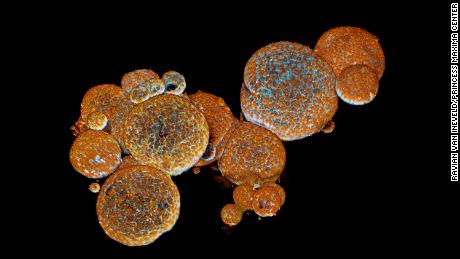 Les organoïdes de glandes à venin de serpent vus au microscope./
Les organoïdes de glandes à venin de serpent vus au microscope./ « Ouvrez-les et vous avez beaucoup de venin. D’après ce que nous savons, il est identique. Nous l’avons comparé directement au venin de la même espèce de serpent et nous trouvons exactement les mêmes composants », a déclaré Clevers, qui était l’un des auteurs de l’article publié dans la revue Cell la semaine dernière.
L’équipe a comparé son venin fabriqué en laboratoire avec le vrai venin au niveau génétique et en termes de fonction, et a constaté que les cellules musculaires cessaient de fonctionner lorsqu’elles étaient exposées à leur venin synthétique.
 Un cobra à lunettes venimeux, également connu sous le nom de cobra indien (Naja Naja) ou cobra blanc, est vu près d’une peinture à l’intérieur de son enclos au jardin zoologique Kamla Nehru à Ahmedabad, le 30 janvier 2019.
Un cobra à lunettes venimeux, également connu sous le nom de cobra indien (Naja Naja) ou cobra blanc, est vu près d’une peinture à l’intérieur de son enclos au jardin zoologique Kamla Nehru à Ahmedabad, le 30 janvier 2019. Cellules et ADN, pas chevaux
Les antivenins actuels dont nous disposons, produits chez les chevaux et non chez les humains, déclenchent des taux relativement élevés de réactions indésirables, qui peuvent être légères, comme des éruptions cutanées et des démangeaisons, ou plus graves, comme l’anaphylaxie. C’est aussi un produit coûteux. Wellcome estime qu’un flacon d’antivenin coûte 160 dollars, et un traitement complet nécessite généralement plusieurs flacons.
Même si les personnes qui en ont besoin peuvent se le permettre — la plupart des victimes de morsures de serpent vivent dans les zones rurales d’Asie et d’Afrique — le monde dispose de moins de la moitié du stock d’antivenin dont il a besoin, selon Wellcome. De plus, des antivenins n’ont été mis au point que pour environ 60% des serpents venimeux du monde.
Dans ce contexte, la nouvelle recherche pourrait avoir des conséquences d’une grande portée, permettant aux scientifiques de créer une biobanque d’organoïdes de glandes de serpent provenant des quelque 600 espèces de serpents venimeux, qui pourraient être utilisés pour produire des quantités illimitées de venin de serpent en laboratoire, a déclaré Clevers.
« La prochaine étape est de prendre toutes ces connaissances et de commencer à étudier de nouveaux antivenins qui adoptent une approche plus moléculaire », a déclaré Clevers.
Pour créer un antivenin, l’information génétique et la technologie des organoïdes pourraient être utilisées pour fabriquer les composants spécifiques du venin qui causent le plus de dommages — et à partir d’eux produire des anticorps monoclonaux, qui imitent le système immunitaire du corps, pour combattre le venin, une méthode déjà utilisée dans les traitements d’immunothérapie pour le cancer et d’autres maladies.
« C’est une nouvelle façon formidable de travailler avec le venin en termes de développement de nouveaux traitements et de mise au point d’antivenins. Les serpents sont très difficiles à soigner », a déclaré Cammack, qui n’a pas été impliqué dans la recherche.
Clevers a déclaré que son laboratoire prévoit maintenant de fabriquer des organoïdes de glandes à venin à partir des 50 animaux les plus venimeux du monde et ils partageront cette biobanque avec des chercheurs du monde entier. Pour le moment, Clevers a dit qu’ils sont capables de produire les organoïdes à un rythme d’un par semaine.
Mais la production d’antivenin n’est pas un domaine dans lequel les entreprises pharmaceutiques ont traditionnellement été désireuses d’investir, a dit Clevers
Les militants décrivent souvent les morsures de serpent comme une crise sanitaire cachée, les morsures de serpent tuant plus de personnes que le cancer de la prostate et le choléra dans le monde, a dit Cammack.
« Il n’y a pas d’argent dans les pays qui souffrent. Ne sous-estimez pas le nombre de personnes qui meurent. Les requins en tuent environ 20 par an. Les serpents en tuent 100 000 ou 150 000 », a déclaré Clevers.
« Je suis un chercheur sur le cancer essentiellement et je suis consterné par la différence d’investissement dans la recherche sur le cancer et cette recherche. »
Le venin est un cocktail complexe
L’un des défis de la fabrication d’un antivenin synthétique est la complexité même de la façon dont un serpent désactive sa proie. Son venin contient plusieurs composants différents qui ont des effets différents.
Des chercheurs en Inde ont séquencé le génome du cobra indien, pour tenter de décoder le venin.
Publié dans la revue Nature Genetics au début du mois, c’est le génome de serpent le plus complet assemblé et il contient la recette génétique du venin du serpent, établissant le lien entre les toxines du serpent et les gènes qui les codent. Ce n’est pas un cocktail simple – l’équipe a identifié 19 gènes sur 139 gènes de toxines comme étant ceux responsables des dommages causés aux humains.
« C’est la première fois qu’un serpent très important sur le plan médical a été cartographié de manière aussi détaillée », a déclaré Somasekar Seshagiri, président de la SciGenom Research Foundation, un centre de recherche à but non lucratif en Inde.
« Cela crée le plan du serpent et nous aide à obtenir les informations des glandes à venin. » Ensuite, son équipe va cartographier les génomes de la vipère à écailles, du krait commun et de la vipère de Russell — le reste des « quatre grands » de l’Inde. Cela pourrait aider à fabriquer de l’antivenin à partir des glandes, car il sera plus facile d’identifier les bonnes protéines.
En tandem, ces deux percées permettront également de découvrir plus facilement si certaines des puissantes molécules contenues dans le venin de serpent méritent elles-mêmes d’être prospectées en tant que médicaments — ce qui permettra aux serpents de laisser leur empreinte sur la santé humaine d’une manière différente de celle prévue par la nature — en sauvant des vies.
Le venin de serpent a été utilisé pour fabriquer des médicaments qui traitent l’hypertension (pression sanguine anormalement élevée) et les troubles cardiaques tels que l’angine.
« En plus d’être effrayant, le venin est étonnamment utile », a déclaré Seshagari.