TOIMINTA
Heterotsygoottinen familiaalinen hyperkolesterolemia (FH) on yleinen perinnöllinen sairaus, johon liittyy ennenaikainen ateroskleroottinen sydän- ja verisuonitauti (ASCVD). Lapsilla, joilla on hoitamaton FH, on suurentunut ennenaikaisen ASCVD:n riski 20 ikävuoden jälkeen.1 Matalatiheyksisen lipoproteiinikolesterolin (LDL-C) pitoisuuksien voimakas kohoaminen alkaa jo sikiössä ja johtaa valtimon seinämän jatkuvaan altistumiseen LDL-C:lle, mikä kiihdyttää kolesterolin kertymistä ja verisuonitulehdusta ja altistaa ateroskleroosin varhaiselle käynnistymiselle erityisesti sepelvaltimoissa ja aortassa.
Statiinit ja muut lipidejä alentavat hoidot (LLT) alentavat tehokkaasti LDL-C:tä, ovat turvallisia lapsilla ja nuorilla ja palauttavat endoteelin toiminnan jo varhaisessa iässä.2-4 Hiljattain on ehdotettu lasten yleistä seulontaa 2 vuoden iästä alkaen ja ennen 8 vuoden ikää5,6 hoitoa tarvitsevien henkilöiden havaitsemiseksi. Tämä lähestymistapa perustuu kuitenkin teoreettisiin pohdintoihin, eikä sitä ole todistettu tosielämässä.
Kuitenkin alle 18-vuotiaiden FH-potilaiden ominaisuuksista, näillä potilailla käytetystä LLT:stä ja tosielämässä saavutetuista lipiditavoitteista tiedetään vain vähän. Tietovaje on vielä suurempi seurantatietojen osalta. Kansallisista rekistereistä voidaan saada tätä ratkaisevan tärkeää tietoa, jota tarvitaan FH:n hoitomallien, hoitoprotokollien ja terveyspolitiikan parantamiseksi.7,8,8 SpAnish Familial HypErcHolEsterolaemiA CohoRt STudy (SAFEHEART) (NCT02693548) suunniteltiin parantamaan käsitystä ASCVD:n ja kuolleisuuden kehittymiseen vaikuttavista ennustetekijöistä ja mekanismeista FH-populaatiossa.
Tavoitteenamme oli analysoida potilaiden ominaisuuksia ja arvioida LLT- ja lipiditavoitteita sisäänottohetkellä ja seurannan aikana SAFEHEART-tutkimukseen osallistuneilla alle 18-vuotiailla FH-potilailla sekä määrittää tekijät, jotka ennustavat näiden tavoitteiden saavuttamisen todennäköisyyttä.
MENETELMÄTutkimuksen rakenne ja väestö
SAFEHEART-tutkimus on avoin, monikeskustutkimus, joka on maanlaajuinen, pitkäkestoinen, pitkäkestoinen, tulevaisuuteen suuntautuva kohorttitutkimus molekyylisesti määritellyssä FH-väestössä Espanjassa. Osallistujien rekrytointi FH-perheistä alkoi vuonna 2004 ja jatkuu edelleen. Tutkimukseen otettiin mukaan indeksitapauksia, joilla oli geneettinen FH-diagnoosi, ja heidän yli 15-vuotiaita sukulaisiaan, joilla oli geneettinen FH-diagnoosi, sekä heidän sukulaisiaan, joilla ei ollut geneettistä FH-diagnoosia (kontrolliryhmä). Kuitenkin myös alle 15-vuotiaat osallistujat otettiin mukaan, jos heidän vanhempansa sitä pyysivät. Paikalliset eettiset toimikunnat hyväksyivät tämän tutkimuksen. Kaikki vaatimukset täyttävät henkilöt ja/tai vähintään yksi heidän vanhemmistaan tai laillisista huoltajistaan antoivat kirjallisen tietoon perustuvan suostumuksen. Madridissa, Espanjassa sijaitseva koordinointikeskus vastasi osallistujien seurannasta. Potilaisiin ja/tai heidän vanhempiinsa otettiin vuosittain yhteyttä standardoidulla puhelinsoitolla, jossa kirjattiin elintavoissa ja lääkityksessä tapahtuneet muutokset sekä mahdolliset sydän- ja verisuonitapahtumat tai muut lääketieteelliset ongelmat. Osallistuvat lääkärit, jotka rekisteröivät potilaita ja perheitä tähän rekisteriin, saivat koulutusta, ja parhaita käytäntöjä koskevia ohjeita vahvistettiin vuotuisissa kokouksissa, joihin osallistui alan asiantuntijalääkäreitä; lisäksi käytettiin sähköistä ohjelmaa ja puhelinneuvontaa sekä verkkopohjaista koulutusohjelmaa, jolla tuettiin hallintaa tarvittaessa. Hoitopäätökset teki yksinomaan kunkin potilaan lääkäri.
Kliiniset ja laboratoriomittaukset
Demografiset ja kliiniset ominaisuudet kirjattiin muualla kuvatulla tavalla.9 Laskimoverinäytteet otettiin 12 tunnin paaston jälkeen. Seerumi-, plasma- ja DNA-näytteet otettiin ja säilytettiin -80 °C:ssa. Seerumin kokonaiskolesteroli-, triglyseridi- ja HDL-C-pitoisuudet mitattiin keskuslaboratoriossa entsymaattisin menetelmin. Seerumin LDL-C-pitoisuus laskettiin Friedewaldin kaavalla. DNA eristettiin kokoverestä standardimenetelmillä, ja FH diagnosoitiin geneettisesti DNA-mikrosirulla.10 LDL-C-tavoitteet määriteltiin viimeaikaisten suositusten ja tavoitteiden mukaisesti. Matalatiheyksinen lipoproteiinikolesteroli
mg/dl oli ensisijainen tavoite.11 Vaihtoehtoinen tavoite alle 14-vuotiaille potilaille koostui LDL-C mg/dl:stä, jos muita sydän- ja verisuonitautien riskitekijöitä (tupakointi, HDL-C mg/dl, lipoproteiini (a) > 50 mg/dl tai LDL-C > 250 mg/dl) tai ennenaikaista sydän- ja verisuonitautia kanta- tai isovanhemmilla ei ollut.6 Ennenaikainen tuttu ASCVD määriteltiin ensimmäisen tapahtuman esiintymiseksi miehillä ennen 55 vuoden ikää ja naisilla ennen 65 vuoden ikää.Lipidien alentavan hoidon luokittelu
Maksimaaliseksi statiiniannokseksi määriteltiin atorvastatiini 40-80mg/d tai rosuvastatiini 20-40mg/d, joita pidettiin suuritehoisina statiiniannoksina. Suurin yhdistelmähoito määriteltiin suurimmaksi statiiniannokseksi ja ezetimibiksi 10 mg/d. Maksimaaliseksi LLT:ksi määriteltiin mikä tahansa LLT, jonka odotettiin vähentävän LDL-C:n lähtötasoa vähintään 50 %: simvastatiini 20, 40 tai 80 mg/d plus ezetimibi 10 mg/d; pravastatiini 40 mg/d yhdessä ezetimibin 10 mg/d kanssa; fluvastatiini 80 mg/d plus ezetimibi 10 mg/d; atorvastatiini 40 tai 80 mg/d ezetimibin 10 mg/d kanssa tai ilman sitä; atorvastatiini 10 tai 20 mg/d plus ezetimibi 10 mg/d; rosuvastatiini 20 tai 40 mg/d yhdessä ezetimibin 10 mg/d kanssa tai ilman sitä; rosuvastatiini 10 mg/d plus ezetimibi 10 mg/d; ja pitavastatiini 4 mg/d yhdessä ezetimibin 10 mg/d kanssa.12,13
Geneettinen analyysi
Matalatiheyksikköisen lipoproteiinikolesterolireseptorin (LDLR) mutaatiot luokiteltiin sen mukaan, millainen vaikutus niillä tiedetään olevan LDL-reseptoriproteiinin toimintaan, nollamutaatioihin (reseptorinegatiiviset mutaatiot) ja viallisiin mutaatioihin (reseptorindefektiiviset mutaatiot), kuten aiemmin on kuvattu.14 Reseptorinegatiivisiksi mutaatioiksi luokiteltiin mutaatiot, jotka johtavat proteiinin täydelliseen poissaoloon tai typistymiseen (toiminnon häviämiseen), joka osoitettiin toiminnallisella in vitro -analyysillä tai tietokonesimulaatioanalyysillä. Näihin variantteihin kuuluivat seuraavat: a) pistemutaatiot, jotka aiheuttavat ennenaikaisen stop-kodonin; b) missense-mutaatiot, jotka vaikuttavat viidenteen kysteiinirikkaaseen toistoon LDL-C-reseptorigeenin ligandia sitovassa domeenissa (luokan 2A mutaatio); c) pienet deletiot tai insertiot, jotka aiheuttavat kehyssiirtymän ja ennenaikaisen stop-kodonin; ja d) suuret uudelleenjärjestelyt. Reseptorivirheellisiä mutaatioita olivat loput inframekaaniset pistemutaatiot ja pienet inframekaaniset deleetiot ja insertiot. Kaikki mutaatiot, joiden toiminnallisuutta ei tiedetty analysoida in vitro -tutkimusten tai tietokonesimulaatioanalyysin avulla, luokiteltiin ”tuntemattomaksi toiminnallisuudeksi”, koska emme voineet olla varmoja siitä, oliko vaikutus reseptoriin negatiivinen vai viallinen; niitä pidettiin kuitenkin patogeenisina, koska kaikilla henkilöillä, jotka kantoivat yhtä näistä mutaatioista, oli hyperkolesterolemia, kun taas sukulaisillaan, joilla ei ollut kyseistä mutaatiota, oli tavanomaiset kolesteroliarvot.14
Statistinen analyysi
Statistinen analyysi suoritettiin käyttäen apuvälineenä SPSS:n versiossa 18.0 olevaa versiota 6.0. (SPSS Inc., Chicago-Illinoisin yliopisto, Illinoisissa, Yhdysvalloissa). Muuttujien jakauman normaalisuus analysoitiin Kolmogorov-Smirnovin testillä. Kvantitatiiviset tiedot ilmaistaan mediaanina ja kvartiilien välisenä vaihteluvälinä (IQR) ja kvalitatiiviset tiedot absoluuttisena lukumääränä ja prosentteina. Määriteltiin kaksi populaatiota: aloitusväestö (n = 241) ja seurantaväestö (ns. kohortti), johon kuuluivat ne potilaat, joilla oli täydellinen plasman lipidiprofiili seurannassa (n = 217). Kaikki tulo- ja seurantatutkimuksen väliset vertailut tehtiin kohorttitutkimuksessa. Laadullisten muuttujien välisten frekvenssien vertailu tehtiin khiin neliö -testillä. Muutokset binäärisissä muuttujissa analysoitiin McNemarin testillä. Kvantitatiivisten muuttujien mediaaniarvoja verrattiin soveltuvin osin ei-parametrisella Mann-Whitneyn testillä tai parittaisella Wilcoxonin allekirjoitetulla rank-testillä. Kohorttitutkimuksessa tehtiin eteenpäin suuntautuva binäärinen logistinen regressioanalyysi statiinien käyttöön liittyvien muuttujien määrittämiseksi. Mukaan otettiin muuttujat, jotka olivat tilastollisesti merkitseviä yksimuuttuja-analyyseissä, sekä a priori-ennustajat ja sekoittajat: ikä, sukupuoli ja seuranta ensisijaisessa/erikoistuneessa ympäristössä. Kohorttitutkimuksessa tehtiin toinen eteenpäin suuntautuva binäärinen logistinen regressioanalyysi, jossa jätettiin pois ne potilaat, jotka saavuttivat tavoitteen aloitusvaiheessa, jotta voitiin määrittää muuttujat, jotka liittyivät LDL-C-arvon
mg/dl saavuttamiseen. Mukaan otettiin muuttujat, jotka olivat tilastollisesti merkitseviä yksimuuttuja-analyyseissä, sekä a priori-ennustajat ja sekoittajat: ikä, sukupuoli, mutaatiotyyppi (nolla tai viallinen), ezetimibin käyttö ja seuranta ensisijaisessa/erikoistuneessa ympäristössä. Erot katsottiin tilastollisesti merkitseviksi P TULOKSET
Tänä päivänä SAFEHEART-rekisteriin on rekisteröity 4141 osallistujaa; 392 on alle 18-vuotiaita. Heistä 241:llä on molekyylivahvistus FH:sta, ja 217:llä seurannassa on täydellinen lipidiprofiili (90,0 %) (kuva 1). Analyysistä jätettiin pois 24 potilasta, koska heillä ei ollut täydellistä lipidiprofiilia seurannan aikana. 40 potilasta (18,4 %) seurattiin perusterveydenhuollossa. Seuranta-ajan mediaani oli 4,69 vuotta (IQR, 2,48-6,38 vuotta).
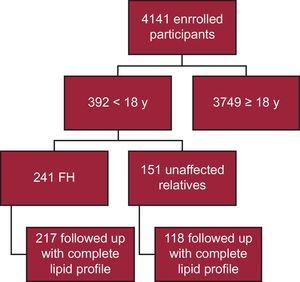
Tutkimuksen kaavamainen vuokaavio. FH, familiaalinen hyperkolesterolemia.
Sisäänottohetkellä (sisäänottopopulaatio) 129 FH-potilasta (53,5 %) oli miehiä. Mediaani-ikä oli 15,0 vuotta (IQR, 14,0-16,0 vuotta). Kaksi nuorinta potilasta oli 8-vuotiaita. Yhdelläkään potilaalla ei ollut aiempaa ASCVD:tä, ja 40:llä (16,6 %) oli ennenaikainen familiaalinen ASCVD. Perusominaisuudet on esitetty taulukossa 1. Taulukossa 1 on vertailu kohorttipotilaiden ja niiden potilaiden, joita ei seurattu, lähtötilanteen ominaisuuksista sisäänottohetkellä. Näiden kahden ryhmän välillä ei havaittu merkittäviä eroja. Yhdelläkään potilaalla ei ollut ASCVD:tä, korkeaa verenpainetta tai diabetes mellitusta. Seurantaan osallistumattomien ryhmästä suurempi osa oli hoidettu perusterveydenhuollossa, vaikka ero ei ollut tilastollisesti merkitsevä. Kohortissa kokonaiskolesterolin, LDL-C:n, triglyseridien ja muun kuin HDL-C:n pitoisuudet plasmassa pienenivät merkittävästi; myös HDL-C:n pitoisuus kasvoi merkittävästi seurannassa (taulukko 2).
Tulospopulaation lähtötason ominaisuudet
| FH-potilaat, joilla oli seurantaa Medianarvo (IQR)/kpl. (%) |
FH-potilaat ilman seurantaa Mediaani (IQR)/kpl. (%) |
P | |
|---|---|---|---|
| No. | 217 | 24 | |
| Sukupuoli (miespuolinen) | 117 (53,9 %) | 12 (50 %) | .72 |
| Ikä, v | 15.0 (14.0-16.0) | 15.0 (13.0-15.8) | .06 |
| Premissiokäyttäytyminen tutun ASCVD:n piirissä | 36 (16.6 %) | 4 (16.7 %) | 1.00 |
| Aktiivinen tupakoitsija | 13 (6.0 %) | 2 (8.3 %) | .65 |
| Xanthomas | 1 (0.5 %) | 0 (0.0 %) | .99 |
| Corneal arcus | 6 (2.8 %) | 1 (4.2 %) | .53 |
| BMI, kg/m2 | 21.09 (19.40-22.80) | 20.79 (17.80-22.70) | .64 |
| Vyötärönympärys, cm | 72.0 (66.0-78.0) | 72.0 (66.0-75.8) | .94 |
| Kokonaiskolesteroli, mg/dl | 223.5 (194.0-262.3) | 217.5 (194.5-277.5) | .76 |
| LDL-C, mg/dl | 162.6 (133.0-195.8) | 153.9 (13.1-209.3) | .71 |
| HDL-C, mg/dl | 49.0 (42.8-55.0) | 48.5 (41.5-56.0) | .96 |
| TG, mg/dl | 62.0 (49.0-80.3) | 66.0 (42.1-82.3) | .90 |
| Non-HDL-C, mg/dl | 174.0 (145.8-210.9) | 167.0 (146.5-225.3) | .74 |
| Lp(a), mg/dl | 18.80 (7.00-48.50) | 13.45 (9.10-28.10) | .46 |
| Hoidetaan perusterveydenhuollossa | 40 (22.9%) | 7 (46.7%) | .06 |
ASCVD, ateroskleroottinen sydän- ja verisuonitauti; BMI, painoindeksi; FH, familiaalinen hyperkolesterolemia; HDL-C, suuritiheyksinen lipoproteiinikolesteroli; LDL-C, pienitiheyksinen lipoproteiinikolesteroli; Lp(a), lipoproteiini (a); IQR, interkvarttiilivyöhyke; TG, triglyseridit.
Plasman lipidi- ja lipoproteiinipitoisuudet (kohortti)
| Kohortti tulohetkellä | Kohortti seurannassa-up | P | ||
|---|---|---|---|---|
| Kokonaiskolesteroli, mg/dl | 221.0 (194.0-260.2) | 203.0 (183.0-233.5) | .001 | |
| LDL-C, mg/dl | 157.7 (132.8-194.5) | 138.0 (116.5-165.4) | .001 | |
| HDL-C, mg/dl | 49.0 (43.0-55.0) | 50.0 (44.0-58.0) | .002 | |
| TG, mg/dl | 62.0 (49.0-80.2) | 70.0 (54.5-91.0) | .004 | |
| Non-HDL-C, mg/dl | 171.0 (145.8-209.2) | 154.0 (132.0-182.5) | .001 |
HDL-C, suuren tiheyden lipoproteiinikolesteroli; LDL-C, matalan tiheyden lipoproteiinikolesteroli; TG, triglyseridit.
Arvot ovat mediaaneja (interkvarttiiliväli).
Funktionaaliset mutaatiot
Havaitsimme 212 potilasta, joilla oli mutaatio LDL-C-reseptorigeeneissä (97,7 %) ja 5 potilasta, joilla oli mutaatio apolipoproteiini B:n geeneissä (2,3 %). LDL-C-reseptorigeenien mutaatioista 95 (43,8 %) luokiteltiin nollamutaatioiksi, 92 (42,4 %) viallisiksi mutaatioiksi ja 25 (11,5 %) tuntemattoman toiminnallisuuden mutaatioiksi.
Lipidiarvoja alentava hoito ja tavoitteiden saavuttaminen
Taulukosta 3 käy ilmi erilaisten LLT-hoitojen käyttö aloitusvaiheessa ja seurannassa. Tulokset osoittavat, että statiinien (44,2 % aloitusvaiheessa ja 68,2 % seurannassa), ezetimibin (8,7 % aloitusvaiheessa ja 15,2 % seurannassa), suurimman mahdollisen statiiniannoksen (3,3 % aloitusvaiheessa ja 13,9 % seurannassa) ja suurimman mahdollisen LLT:n (7,9 % aloitusvaiheessa ja 23,6 % seurannassa) käyttö lisääntyi merkittävästi. Yleisimmin määrätty statiini aloitusvaiheessa (25,3 %) ja seurannassa (30.5 %) oli atorvastatiini. Rosuvastatiinin määrääminen lisääntyi (6,0 %:sta 6,0 %:sta 20,3 %:iin seurannassa). Statiinihoidon mediaanikesto oli 7,0 vuotta (5,0-9,0 vuotta). Menarke-ikä oli 12,0 vuotta (12,0-13,0 vuotta) tytöillä, joita hoidettiin statiineilla, ja 12,0 vuotta (11,0-13,0 vuotta) tytöillä, joita ei hoidettu statiineilla (P = .77). Maksan transaminaasien tai kreatiinifosfokinaasin nousua ei havaittu. Fibraatteja ja sappihapposekvestrantteja käytettiin vain 15 potilaalla sisäänottohetkellä (7,0 %) ja 3 potilaalla seurannassa (1,5 %). Etsetimibimonoterapiaa ilman statiinia käytettiin 18 potilaalla (8,3 %) sisäänottohetkellä ja 24 potilaalla (11,1 %) seurannassa. Hoitoon sitoutumisen osalta 10 potilasta (4,6 %) ilmoitti, että he eivät ottaneet lääkkeitä vähintään yhtenä päivänä kuukaudessa seurannan aikana. Monimuuttuja-analyysissä mikään muuttuja ei ollut itsenäisesti yhteydessä statiinin käyttöön.
Lipidiarvoja alentavat hoidot ja LDL-C-tavoitteen saavuttaminen (kohortti)
| Sisäänpääsy- /seuranta-…up- | At entry-/follow-up+ | At entry+/follow-up- | At entry+/follow-up+ | P | |
|---|---|---|---|---|---|
| Potilaat, jotka saivat statiineja | 60 (27.6 %) | 61 (28.1 %) | 9 (4.1 %) | 87 (40.1 %) | .001 |
| Potilaat, jotka käyttivät suurinta statiiniannosta | 186 (85.7 %) | 24 (11,1 %) | 1 (0,5 %) | 6 (2,8 %) | .001 |
| Potilaat, jotka saivat ezetimibiä | 177 (81,6 %) | 21 (9.7 %) | 7 (3,2 %) | 12 (5,5 %) | .013 |
| Potilaat, jotka saivat maksimaalista yhdistelmähoitoa | 211 (97,2 %) | 6 (2,8 %) | 0 (0.0 %) | 0 (0.0 %) | N/A |
| Potilaat, jotka saivat maksimissaan LLT-hoitoa | 163 (75.1 %) | 37 (17.1 %) | 3 (1.4 %) | 14 (6.5 %) | .001 |
| LDL-C | 111 (51.2%) | 62 (28.6%) | 16 (7.4 %) | 28 (12,9 %) | .001 |
| LDL-C | 44 (20,3 %) | 64 (29.5 %) | 19 (8,8 %) | 90 (41,5 %) | .001 |
LDL-C, matalan tiheyden lipoproteiinikolesteroli; LLT, lipidejä alentava hoito.
Luvut ovat n (%). – = ei ole; + = on.
Katso teksti LLT-luokitus.
Plasman LDL-C-pitoisuus laski keskimäärin 12,5 % ja saavutti seurannassa mediaaniarvon 138,0 mg/dl. FH:ta koskevien tuoreiden kansainvälisten suositusten mukaiset matalan tiheyden lipoproteiinikolesterolin tavoitteet saavutettiin 20,3 %:lla aloitusvaiheessa ja 41,5 %:lla seurannassa (taulukko 3 ja kuva 2). Kun vaihtoehtoisena tavoitteena pidettiin LDL-C:tä
mg/dl alle 14-vuotiaille potilaille, tavoitteen saavutti 8 potilasta 48:sta (16,7 %) 48:sta (16,7 %) ja 1 potilas 6:sta (16,7 %) 6:sta (16,7 %) 8:sta 48:sta (16,7 %) ja 1 potilas 6:sta (16,7 %). Ainoa muuttuja, joka oli monimuuttuja-analyysissä itsenäisesti yhteydessä LDL-C-tavoitteen saavuttamiseen, oli statiinien käyttö (odds ratio 13,83; 95 prosentin luottamusväli 2,98-64,15). Terveydenhuollon tarjoajan tyyppi (erikoislääkäri tai perusterveydenhuollon lääkäri), ikä, sukupuoli, lipoproteiini(a)-pitoisuus ja mutaatiotyyppi eivät olleet yhteydessä LDL-C-tavoitteen saavuttamiseen.
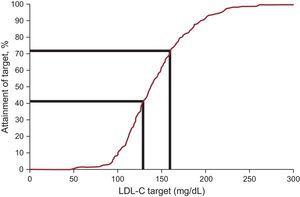
Hoitotavoitteet alle 18-vuotiailla familiaalista hyperkolesterolemiaa sairastavilla potilailla: LDL-C-tavoitteen saavuttaneiden potilaiden osuus. LDL-C, matalan tiheyden lipoproteiinikolesteroli.
KESKUSTELU
Tässä tutkimuksessa kerromme ominaispiirteistä, LLT:n käytöstä ja LDL-C-tavoitteen saavuttamisesta pitkittäiskohortissa, joka koostui molekyylitason mukaan määritellyistä, nuoremmista, alle 18-vuotiaista FH-potilaista, jotka olivat ilmoittautuneet SAFEHEART-rekisteriin. Tämä ainutlaatuinen FH-potilaiden rekisteri perustuu tietoihin, jotka on saatu todellisesta elämästä Espanjassa sekä erikoissairaanhoidon että perusterveydenhuollon piirissä. Tuloksemme osoittavat, että LDL-C:n hoitotavoite
mg/dl saavutettiin vain 20,3 %:lla potilaista sisäänottohetkellä ja 41,5 %:lla seurannassa, ja 68,2 %:lla potilaista oli LLT. Statiinien käyttö oli ainoa tekijä, joka oli itsenäisesti yhteydessä LDL-C-tavoitteen saavuttamiseen. Tietojemme mukaan missään muussa työssä ei ole osoitettu tavoitteen saavuttamista alle 18-vuotiailla FH-potilailla, ja tämä tutkimus on ensimmäinen, jossa se raportoidaan suuressa populaatiossa.
Juuri äskettäin Yhdistyneessä kuningaskunnassa tehdyssä rekisterissä15 analysoitiin 207 FH:ta sairastavaa lasta, ja siinä tunnistettiin mutaatioita 64 %:lla lapsista, ja todettiin, että 48 %:lla heistä oli LLT-hoito; LDL-C:n aleneminen 35 %:lla oli saavutettu. Kirjoittajat eivät kuitenkaan raportoineet tavoitteiden saavuttamisen tuloksia. Toisessa raportissa, jossa analysoitiin pientä otosta (n = 89), havaittiin 43 prosentin LDL-C:n väheneminen pitkäaikaisseurannassa.16 Tämä suurempi väheneminen johtuu todennäköisesti siitä, että yhdistelmähoitoa käytettiin useammin (56 %). Tavoitteiden saavuttamista koskevia tuloksia ei esitetty. Toisessa retrospektiivisessä artikkelissa, johon osallistui 207 potilasta Alankomaissa, vain 26 % potilaista käytti LLT-hoitoa, eikä jälleen kerran raportoitu tuloksia LDL-C-tavoitteen saavuttamisesta.17
Tämä pitkittäistutkimus osoitti, että alle 18-vuotiaiden FH-potilaiden LDL-C-pitoisuudet voivat muuttua ajan mittaan LLT:n muutoksen ja lääkärin antaman koulutuksen ansiosta. Statiinia käyttävien potilaiden osuus, suurin statiiniannos ja suurin LLT-arvo kasvoivat merkittävästi seurannan aikana. Mielenkiintoista on, että tietomme osoittavat, että kohorttimme ei ole vääristynyt, koska seurannan ulkopuolelle jääneiden potilaiden ja kohortin välillä ei ollut tilastollisesti merkitseviä eroja.
FH:n varhainen diagnosointi ja hoito on olennaista erityisesti lapsilla ja nuorilla, jotta voidaan ehkäistä ASCVD:n kehittyminen aikuisuudessa. FH:n seulonta lapsilla on kannattavaa, ja se on tehtävä ennen 8 vuoden ikää, koska hyperkolesterolemiaa sairastavilla lapsilla on suurentunut ennenaikaisen ASCVD:n riski. Lisäksi seulonnalla voidaan tunnistaa suurimmassa riskissä olevat lapset ja käynnistää LLT-menetelmä, jonka on osoitettu kääntävän ateroskleroottisen prosessin tehokkaasti ja vähentävän ASCVD-riskiä. FH:ta sairastavilla lapsilla ei yleensä ole kliinistä ASCVD:tä. Kuitenkin tulevan riskin olemassaolo tukee LLT:n käyttöä, ja statiinit ovat FH:n hoidon kulmakivi.18
LLT:n turvallisuus ja siedettävyys lasten FH:ssa ovat aina kiistanalaisia, vaikka niiden on raportoitu olevan samankaltaisia kuin aikuisilla.5,19,20 Hiljattain Ramaswami ym.15 raportoivat, että turvallisuusongelmia ei ole ilmennyt, ja ne ovat samankaltaisia kuin meidänkin tulokset. Tiukkaa valvontaa suositellaan kuitenkin erityisesti niille potilaille, jotka saavat suurempia statiiniannoksia. Nuoria tyttöjä olisi myös neuvottava keskeyttämään statiinihoito, kun he harkitsevat raskautta. Vaikka pitkäaikaisessa LLT-hoidossa olevien lasten turvallisuuskysymyksistä tarvitaan lisää tietoa, viimeaikaiset pitkäaikaiset seurantatutkimukset ovat kuitenkin osoittaneet, että turvallisuusprofiili on erinomainen.21 Tietomme tukevat epäsuorasti tätä havaintoa, koska suuri osa potilaista aloitti LLT-hoidon seurannan aikana ja keskeyttämisiä oli vähän. Tuloksistamme käy selvästi ilmi, että yhä useammat potilaat käyttivät statiinia, suurta statiiniannosta ja maksimaalista LLT-hoitoa, ja vain pieni osa potilaista luopui lääkityksestä. Nämä tiedot vahvistavat statiinien turvallisuuden, noudattamisen ja siedettävyyden, vaikka niitä käytettäisiinkin suurina annoksina, alle 18-vuotiailla FH-potilailla.22 Lisäksi tuloksemme ovat yhtäpitäviä aiempien raporttien kanssa, joiden mukaan niillä ei ole vaikutusta seksuaaliseen kypsymiseen.23 Kaikki nämä tulokset vahvistavat käsitteen ”mitä nuorempi, sitä parempi”, joka koskee ihanteellista ikää statiinien aloittamiselle näillä nuorilla FH-potilailla.23
Tuloksemme osoittavat, että alle 18-vuotiaiden FH-potilaiden määrä on suuri, ja aiempien tutkimusten15,16 mukaisesti ne viittaavat siihen, että aikuiset FH-potilaat ovat halukkaita ottamaan lähimmät perheenjäsenensä mukaan seulonta- ja rekisteritoimintaan. Tämä seikka kuvastaa sitä, miten vakavasti nämä potilaat suhtautuvat ongelmaansa ja miten lääkärin neuvot voivat vaikuttaa heidän elämäntapojensa muuttamiseen. Tällainen asenne aikuispotilailla muodostaa perustan heidän sukulaistensa terveellisille elämäntavoille.24
Vaikka alle 18-vuotiaiden FH-potilaiden yleisin tavoite on alle 130 mg/dl:n LDL-C-taso, vaihtoehtoista lähestymistapaa, joka muodostuu LDL-C mg/dl:stä, voidaan käyttää niillä alle 14-vuotiailla potilailla, jotka eivät ole tupakoitsijoita, joilla on HDL-C-arvo ≥ 40 mg/dl, lipoproteiini(a)-arvo mg/dl, LDL-C mg/dl ja joilla ei ole sydän- ja verisuonitautien ennenaikaisuutta esivanhemmilla tai isoisovanhemmilla.6 Muissa viimeaikaisissa ohjeissa suositellaan LDL-C:n vähentämistä 50 %:lla hoitoa edeltävästä tasosta, mutta ≥ 10-vuotiaille lapsille, erityisesti jos heillä on muita sydän- ja verisuonitautien riskitekijöitä, kuten kohonnut lipoproteiini (a), LDL-C:n tavoitetason tulisi olla mg/dl.11 Tuloksemme osoittavat myös, että näillä potilailla on vaikeuksia saavuttaa rasva-arvotavoitteet.25 Lisäksi LDL-C-tavoitteen saavuttaminen oli samanlaista riippumatta siitä, olivatko potilaat erikoisalojen vai perusterveydenhuollon erikoislääkärien hoidossa. Näin ollen on mahdollista saavuttaa perusterveydenhuollossa FH:ta sairastavien lapsipotilaiden hoidon taso, joka on verrattavissa erikoissairaanhoidossa saavutettuun tasoon. Tämän tavoitteen saavuttamiseksi on tärkeää korostaa tukea, jota lääkärit saavat rekistereiden ja erityisten koulutusohjelmien kautta. Rekisterit voivat optimoida alle 18-vuotiaiden FH-potilaiden hoidon mahdollistamalla perusterveydenhuollon ja erikoissairaanhoidon yhdistämisen, ja ne voivat myös tukea terveysviranomaisia päätöksenteossa.8,26
Rajoitukset ja vahvuudet
Tässä laajassa, alle 18-vuotiaiden FH-potilaiden seurantatutkimuksessa interventio ei muuttunut potilaslääkärin antamasta hoidosta. Luotettava lähtötason lipidiprofiili puuttuu tästä rekisteristä, koska osa potilaista sai jo hoitoa, kun heidät otettiin mukaan. Lisäksi tuloksia ovat saattaneet muuttaa useat olosuhteet, kuten erilaiset elintavat, ja yhteys erilaisiin sydän- ja verisuonitautien riskitekijöihin, jotka olisivat voineet muuttaa tuloksia.
YHTEENVETO
SAFEHEART-rekisterin tiedot osoittavat, että suurella osalla FH-potilaista, jotka ovat alle 18-vuotiaita, on korkeat LDL-C-pitoisuudet ja että he eivät saavuta suositeltuja LDL-C-tavoitteita. Havaitsimme LLT-intensiteetin lisääntyneen ja LDL-C-tasojen laskeneen merkittävästi seurannan aikana. Statiinien käyttö oli ainoa riippumaton LDL-C-tavoitteen saavuttamista ennustava tekijä. Seurannan aikana ei myöskään havaittu turvallisuusongelmia. Nämä tulokset osoittavat, että monet FH-potilaat eivät ole riittävän hyvin hallinnassa ja että hoitoa on vielä mahdollista parantaa. Lisäksi tämän FH-populaation seuranta voi edistää tietämystä elinikäisen LLT:n turvallisuudesta ja optimaalisesta iästä hoidon aloittamiselle ASCVD:n kehittymisen ehkäisemiseksi aikuisiässä.
RAHOITUS
Tätä työtä on tuettu Fundación Hipercolesterolemia Familiar -järjestön apurahalla G03/181, Instituto de Salud Carlos III:n apurahalla FIS PI12/01289 ja Centro Nacional de Investigación Cardiovascularin apurahalla 08-2008.
HYÖDYKKEELLISYYTEEN LIITTYVÄT RIIPPUVUUDET
Eivät ole ilmoittaneet mitään.
- –
Lapsilla, joilla on hoitamaton heterotsygoottinen familiaalinen hyperkolesterolemia, on suurentunut ennenaikaisen ASCVD:n riski 20 ikävuoden jälkeen.
- –
Statiineilla ja muilla lipidejä alentavilla hoitomuodoilla voidaan tehokkaasti alentaa LDL-C:tä, ja ne ovat turvallisia lapsille ja nuorille.
- –
Vähän tiedetään alle 18-vuotiaiden FH-potilaiden ominaispiirteistä, näillä potilailla käytetyistä lipidejä alentavista hoidoista ja todellisuudessa saavutetuista lipiditavoitteista.
- –
Tämä tietovaje on vieläkin suurempi seurantatiedoissa.
MITÄ TÄMÄ TARKOITTAA?
- –
Suuri osa alle 18-vuotiaista FH-potilaista ei saavuta suositeltuja LDL-C-tavoitteita.
- –
Havaitsimme LLT-intensiteetin lisääntyvän ja LDL-C-tasojen laskevan merkittävästi seurannan aikana.
- –
Statiinin käyttö oli ainoa itsenäinen ennustaja LDL-C-tavoitteen saavuttamiselle, eikä seurannan aikana havaittu turvallisuusongelmia.
- –
Tulokset vahvistavat ajatusta ”mitä nuorempi, sitä parempi”.