Generischer Name: Aciclovir
Dosierung Form: Creme
Medically reviewed by Drugs.com. Last updated on Dec 1, 2020.
- Übersicht
- Nebenwirkungen
- Dosierung
- Fachkundige
- Interaktionen
- Mehr
- Indikationen und Anwendung für Zovirax Creme
- Zovirax Creme Dosierung und Anwendung
- Dosierungsformen und Stärken
- 4KONTRAINDIKATIONEN
- Warnungen und Vorsichtsmaßnahmen
- Allgemein
- Kontaktsensibilisierung
- Nebenwirkungen
- Erfahrungen aus klinischen Studien
- Erfahrungen nach der Markteinführung
- Arzneimittelwechselwirkungen
- VERWENDUNG IN BESONDEREN POPULATIONEN
- Risiko-Zusammenfassung
- Schwangerschaft
- Stillen
- Anwendung bei Kindern
- Geriatrische Anwendung
- Überdosierung
- Zovirax Creme Beschreibung
- Zovirax Creme – Klinische Pharmakologie
- Wirkungsmechanismus
- Pharmakokinetik
- Mikrobiologie
- Nichtklinische Toxikologie
- Kanzerogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
- Klinische Studien
- Erwachsene Probanden
- Kinder
- Lagerung und Handhabung
- Patientenberatung
- PATIENTENINFORMATIONENZOVIRAX (zho-vahy-rex)(acyclovir)Creme
- Hauptanzeigefeld – 5g Tube Karton
- Mehr über Zovirax Creme (Acyclovir topisch)
- Ressourcen für Verbraucher
- Ressourcen für Fachleute
- Andere Formulierungen
- Verwandte Behandlungsleitfäden
Indikationen und Anwendung für Zovirax Creme
Zovirax Creme ist ein Herpes-simplex-Virus (HSV)-Desoxynukleosid-analoger DNA-Polymerase-Inhibitor, der zur Behandlung von wiederkehrendem Herpes labialis (Fieberbläschen) bei immunkompetenten Erwachsenen und Jugendlichen ab 12 Jahren angezeigt ist.
Zovirax Creme Dosierung und Anwendung
Zovirax Creme sollte 5 mal täglich für 4 Tage aufgetragen werden. Die Therapie sollte so früh wie möglich nach dem Auftreten von Anzeichen oder Symptomen von Herpes labialis eingeleitet werden, d.h. während des Prodromums oder beim Auftreten von Läsionen.
Für Jugendliche ab 12 Jahren ist die Dosierung die gleiche wie bei Erwachsenen.
Dosierungsformen und Stärken
Jedes Gramm Zovirax Creme enthält 50 mg (entsprechend 5 Gew.-%) Aciclovir.
4KONTRAINDIKATIONEN
Zovirax Creme ist kontraindiziert bei Patienten mit bekannter Überempfindlichkeit gegen Acyclovir, Valacyclovir oder einen Bestandteil der Formulierung.
Warnungen und Vorsichtsmaßnahmen
Allgemein
Zovirax Creme sollte bei Patienten mit Herpes labialis nur auf die betroffenen äußeren Bereiche der Lippen und des Gesichts aufgetragen werden. Da keine Daten vorliegen, wird die Anwendung auf menschlichen Schleimhäuten nicht empfohlen. Zovirax Creme ist nur für die Anwendung auf der Haut bestimmt und sollte nicht im Auge oder im Mund oder in der Nase verwendet werden.
Kontaktsensibilisierung
Zovirax Creme kann zu Reizungen und Kontaktsensibilisierung führen.
Die Wirkung von Zovirax Creme wurde bei immungeschwächten Patienten nicht nachgewiesen.
Nebenwirkungen
Erfahrungen aus klinischen Studien
Da klinische Studien unter sehr unterschiedlichen Bedingungen durchgeführt werden, können die in den klinischen Studien eines Arzneimittels beobachteten Nebenwirkungsraten nicht direkt mit den Raten in den klinischen Studien eines anderen Arzneimittels verglichen werden und spiegeln möglicherweise nicht die in der klinischen Praxis beobachteten Raten wider.
In fünf doppelblinden, placebokontrollierten Studien wurden 1124 Patienten mit Zovirax Creme und 1161 mit Placebo (Vehikel) Creme behandelt. Lokale Reaktionen an der Applikationsstelle wurden von 5 % der Patienten, die Zovirax-Creme erhielten, und 4 % der Patienten, die Placebo erhielten, gemeldet. Die häufigsten unerwünschten Wirkungen an der Applikationsstelle waren trockene Lippen, Abschuppung, trockene Haut, rissige Lippen, Hautbrennen, Juckreiz, schuppige Haut und Stechen auf der Haut; jede unerwünschte Wirkung trat bei weniger als 1 % der Patienten auf, die Zovirax Creme oder Placebo erhielten. Drei Patienten, die Zovirax Creme erhielten, und ein Patient, der Placebo erhielt, brachen die Behandlung aufgrund eines unerwünschten Ereignisses ab.
Eine zusätzliche Studie, an der 22 gesunde Erwachsene teilnahmen, wurde durchgeführt, um die Hautverträglichkeit von Zovirax Creme im Vergleich zum Vehikel zu bewerten, wobei die Methodik eines einzelnen verschlossenen und halbverschlossenen Pflastertests verwendet wurde. Sowohl Zovirax Creme als auch Placebo zeigten ein hohes und kumulatives Reizungspotenzial. Eine weitere Studie, an der 251 gesunde Erwachsene teilnahmen, wurde durchgeführt, um das Kontaktsensibilisierungspotenzial von Zovirax-Creme mit Hilfe von Patch-Test-Methoden mit wiederholtem Insult zu bewerten. Von 202 auswertbaren Probanden wurden mögliche Sensibilisierungsreaktionen der Haut bei denselben 4 (2 %) Probanden sowohl mit Zovirax-Creme als auch mit Placebo beobachtet, und diese Reaktionen auf Zovirax-Creme und Placebo wurden bei 3 Probanden nach erneuter Provokation bestätigt. Der/die sensibilisierende(n) Bestandteil(e) wurde(n) nicht identifiziert.
Das Sicherheitsprofil bei Patienten im Alter von 12 bis 17 Jahren war ähnlich wie das bei Erwachsenen beobachtete.
Erfahrungen nach der Markteinführung
Zusätzlich zu den unerwünschten Ereignissen, die aus klinischen Studien berichtet wurden, wurden die folgenden Ereignisse während der Anwendung von Acyclovir-Creme nach der Zulassung festgestellt. Da sie freiwillig aus einer Population unbekannter Größe gemeldet wurden, können keine Schätzungen der Häufigkeit vorgenommen werden. Diese Ereignisse wurden aufgrund einer Kombination aus ihrer Schwere, der Häufigkeit der Meldungen oder eines möglichen kausalen Zusammenhangs mit Aciclovir-Creme für die Aufnahme ausgewählt.
Allgemein: Angioödem, Anaphylaxie.
Haut: Kontaktdermatitis, Ekzem.
Arzneimittelwechselwirkungen
Klinische Erfahrungen haben keine Wechselwirkungen bei gleichzeitiger topischer oder systemischer Verabreichung von anderen Arzneimitteln mit Zovirax Creme ergeben. Aufgrund der minimalen systemischen Absorption von Zovirax Creme sind systemische Arzneimittelwechselwirkungen unwahrscheinlich.
VERWENDUNG IN BESONDEREN POPULATIONEN
Risiko-Zusammenfassung
Acyclovir wird nach topischer Verabreichung nur minimal systemisch absorbiert, und es ist nicht zu erwarten, dass die mütterliche Anwendung zu einer fetalen Exposition gegenüber Zovirax Creme führt. Die Erfahrung mit der topischen Anwendung von Acyclovir bei schwangeren Frauen über mehrere Jahrzehnte hinweg, basierend auf der veröffentlichten Literatur, einschließlich Beobachtungsstudien, hat kein arzneimittelassoziiertes Risiko für schwerwiegende Geburtsfehler, Fehlgeburten oder nachteilige mütterliche oder fötale Ergebnisse ergeben. Tierische Reproduktionsstudien mit systemischer Exposition von Acyclovir wurden durchgeführt. Das geschätzte Hintergrundrisiko für schwere Geburtsfehler und Fehlgeburten für die angegebene Population ist nicht bekannt. Alle Schwangerschaften haben ein Hintergrundrisiko für Geburtsfehler, Fehlgeburten oder andere unerwünschte Ergebnisse. In der Allgemeinbevölkerung der USA beträgt das geschätzte Hintergrundrisiko für schwere Geburtsfehler und Fehlgeburten bei klinisch anerkannten Schwangerschaften 2 % bis 4 % bzw. 15 % bis 20 %.
Schwangerschaft
Zusammenfassung der Risiken
Acyclovir wird nach topischer Verabreichung nur geringfügig systemisch resorbiert, und es ist nicht zu erwarten, dass die mütterliche Anwendung zu einer fetalen Exposition gegenüber Zovirax Creme führt. Die Erfahrung mit der topischen Anwendung von Acyclovir bei schwangeren Frauen über mehrere Jahrzehnte hinweg, basierend auf der veröffentlichten Literatur, einschließlich Beobachtungsstudien, hat kein arzneimittelassoziiertes Risiko für schwerwiegende Geburtsfehler, Fehlgeburten oder nachteilige mütterliche oder fötale Ergebnisse ergeben. Tierische Reproduktionsstudien mit systemischer Exposition von Acyclovir wurden durchgeführt. Das geschätzte Hintergrundrisiko für schwere Geburtsfehler und Fehlgeburten für die angegebene Population ist nicht bekannt. Alle Schwangerschaften haben ein Hintergrundrisiko für Geburtsfehler, Fehlgeburten oder andere unerwünschte Ergebnisse. In der amerikanischen Allgemeinbevölkerung beträgt das geschätzte Hintergrundrisiko für schwere Geburtsfehler und Fehlgeburten bei klinisch anerkannten Schwangerschaften 2 % bis 4 % bzw. 15 % bis 20 %.
Stillen
Risikozusammenfassung
Acyclovir wird nach topischer Verabreichung nur minimal systemisch resorbiert, und es ist nicht zu erwarten, dass das Stillen zu einer Exposition des Kindes gegenüber Zovirax Creme führt. Es gibt keine Daten über die Auswirkungen von ZOVIRAX auf den gestillten Säugling oder auf die Milchproduktion. Die entwicklungs- und gesundheitsfördernden Wirkungen des Stillens sollten zusammen mit dem klinischen Bedarf der Mutter an Zovirax-Creme und möglichen unerwünschten Wirkungen von Zovirax-Creme oder der mütterlichen Grunderkrankung auf das gestillte Kind berücksichtigt werden.
Anwendung bei Kindern
Eine offene, unkontrollierte Studie mit Zovirax-Creme wurde an 113 Patienten im Alter von 12 bis 17 Jahren mit rezidivierendem Herpes labialis durchgeführt. In dieser Studie wurde die Therapie nach demselben Dosierungsschema wie bei Erwachsenen durchgeführt, und die Probanden wurden hinsichtlich unerwünschter Ereignisse beobachtet. Das Sicherheitsprofil war mit dem bei Erwachsenen beobachteten vergleichbar. Sicherheit und Wirksamkeit bei pädiatrischen Patienten unter 12 Jahren wurden nicht nachgewiesen.
Geriatrische Anwendung
Klinische Studien mit Aciclovir-Creme umfassten keine ausreichende Anzahl von Probanden im Alter von 65 Jahren und darüber, um festzustellen, ob sie anders reagieren als jüngere Probanden. In anderen Berichten über klinische Erfahrungen wurden keine Unterschiede im Ansprechen zwischen älteren und jüngeren Patienten festgestellt. Die systemische Absorption von Acyclovir nach topischer Anwendung ist minimal.
Überdosierung
Eine Überdosierung durch topische Anwendung von Zovirax Creme ist aufgrund der minimalen systemischen Exposition unwahrscheinlich. Es liegen keine Informationen über eine Überdosierung vor.
Zovirax Creme Beschreibung
ZOVIRAX ist der Markenname für Acyclovir, ein synthetisches Desoxynukleosid-Analogon, das gegen Herpesviren wirkt. Zovirax Creme 5% ist eine Formulierung zur topischen Anwendung.
Der chemische Name von Acyclovir ist 2-Amino-1,9-dihydro-9–6H-purin-6-on; es hat die folgende Strukturformel:
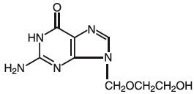
Acyclovir ist ein weißes, kristallines Pulver mit der Summenformel C8H11N5O3 und einem Molekulargewicht von 225. Die maximale Löslichkeit in Wasser bei 37°C beträgt 2,5 mg/ml. Die pKa-Werte von Aciclovir liegen bei 2,27 und 9,25.
Jedes Gramm Zovirax Creme enthält 50 mg (entspricht 5 % w/w) Aciclovir und die folgenden inaktiven Bestandteile: Cetostearylalkohol, Mineralöl, Poloxamer 407, Propylenglycol, Natriumlaurylsulfat, Wasser und weiße Vaseline.
Zovirax Creme – Klinische Pharmakologie
Wirkungsmechanismus
Acyclovir ist ein antivirales Arzneimittel, das gegen α-Herpesviren wirkt.
Pharmakokinetik
Eine klinische Pharmakologiestudie wurde mit Zovirax Creme an erwachsenen Freiwilligen durchgeführt, um die perkutane Absorption von Acyclovir zu bewerten. In dieser Studie, an der 6 männliche Probanden teilnahmen, wurde die Creme auf eine Fläche von 710 cm2 auf dem Rücken der Probanden aufgetragen, und zwar fünfmal täglich im Abstand von 2 Stunden über einen Zeitraum von insgesamt 4 Tagen. Das Gewicht der aufgetragenen Creme und die Urinausscheidung von Acyclovir wurden täglich gemessen. Die Plasmakonzentration von Acyclovir wurde 1 Stunde nach der letzten Anwendung bestimmt. Die durchschnittliche tägliche Ausscheidung von Acyclovir im Urin betrug etwa 0,04 % der täglich aufgetragenen Dosis. Die Plasma-Acyclovir-Konzentrationen lagen bei 5 Probanden unter der Nachweisgrenze (0,01 μM) und waren bei 1 Probanden kaum nachweisbar (0,014 μM). Die systemische Absorption von Acyclovir aus Zovirax Creme ist bei Erwachsenen minimal.
Die systemische Absorption von Acyclovir nach topischer Anwendung der Creme wurde bei Patienten <18 Jahren nicht untersucht.
Mikrobiologie
Wirkmechanismus: Acyclovir ist ein synthetisches Purindesoxynukleosid-Analogon mit zellkultur- und in vivo-inhibitorischer Aktivität gegen HSV-Typen 1 (HSV-1) und 2 (HSV-2) DNA-Polymerasen. Es hemmt die Replikation von HSV-1 und HSV-2 in Zellkultur und in vivo.
Die hemmende Wirkung von Aciclovir ist selektiv aufgrund seiner Affinität zu dem Enzym Thymidinkinase (TK), das von HSV kodiert wird. Dieses virale Enzym wandelt Acyclovir in Acyclovir-Monophosphat, ein Desoxynukleotid-Analogon, um. Das Monophosphat wird von der zellulären Guanylatkinase weiter in Diphosphat und von einer Reihe von zellulären Enzymen in Triphosphat umgewandelt. In biochemischen Tests hemmt Aciclovir-Triphosphat die Replikation der DNA des α-Herpesvirus. Diese Hemmung wird auf 3 Arten erreicht: 1) kompetitive Hemmung der viralen DNA-Polymerase, 2) Einbau in die wachsende virale DNA-Kette und deren Abbruch und 3) Inaktivierung der viralen DNA-Polymerase.
Antivirale Aktivität
Die quantitative Beziehung zwischen der Empfindlichkeit von Herpesviren gegenüber Virostatika in der Zellkultur und dem klinischen Ansprechen auf die Therapie ist beim Menschen nicht bekannt, und die Virusempfindlichkeitstests sind nicht standardisiert. Die Ergebnisse der Empfindlichkeitstests, ausgedrückt als die Konzentration des Arzneimittels, die erforderlich ist, um das Wachstum des Virus in der Zellkultur um 50 % zu hemmen (EC50-Wert), variieren stark in Abhängigkeit von einer Reihe von Faktoren. Bei Verwendung von Plaquereduktionstests an Vero-Zellen reichen die EC50-Werte von Aciclovir gegen Herpes-simplex-Virusisolate von 0,09 bis 59,9 μM (0,02 bis 13,5 μg/mL) für HSV-1 und von 0.04 bis 44,0 μM (0,01 bis 9,9 μg/mL) für HSV-2.
Resistenz
In Zellkultur
Acyclovir-resistente HSV-1- und HSV-2-Stämme wurden in Zellkultur isoliert. Acyclovir-resistente HSV resultierten aus Mutationen in den viralen Genen für Thymidinkinase (TK; pUL23) und DNA-Polymerase (POL; pUL30). Frameshifts wurden häufig isoliert und führen zu einer vorzeitigen Verkürzung des HSV-TK-Produkts und damit zu einer verminderten Empfindlichkeit gegenüber Aciclovir. Mutationen im viralen TK-Gen können zu einem vollständigen Verlust der TK-Aktivität (TK-negativ), zu einer reduzierten TK-Aktivität (TK-partiell) oder zu einer Veränderung der Fähigkeit der viralen TK zur Phosphorylierung des Arzneimittels ohne einen entsprechenden Verlust der Fähigkeit zur Phosphorylierung von Thymidin (TK-verändert) führen. In der Zellkultur wurden die folgenden resistenzassoziierten Substitutionen in der TK von HSV-1 und HSV-2 beobachtet (Tabelle 1).
|
HSV-1 |
TK |
P5A, H7Q, L50V, G56V, G59A, G61A, K62N, T63A, E83K, P84S, D116N, P131S, R163H, A167V, P173L, Q185R, R216S, R220H, T245M, R281stop, T287M, M322K |
|
HSV-2 |
TK |
L69P, C172R, T288M |
|
HSV-1 |
POL |
D368A, Y557S, E597D, V621S, L702H, N815S, V817M, G841C |
|
HSV-2 |
POL |
bei HSV-infizierten Patienten
Klinische HSV-1 und HSV-2-Isolate, die von Patienten gewonnen wurden, bei denen die Behandlung ihrer α-Herpesvirus-Infektionen fehlgeschlagen war, wurden auf genotypische Veränderungen in den TK- und POL-Genen und auf phänotypische Resistenz gegen Aciclovir untersucht (Tabelle 2). Es wurden HSV-Isolate mit Frameshift-Mutationen und Resistenz-assoziierten Substitutionen in TK und POL identifiziert. Die Auflistung der Substitutionen in HSV TK und POL, die zu einer verminderten Empfindlichkeit gegenüber Acyclovir führen, ist nicht vollständig, und es werden wahrscheinlich noch weitere Veränderungen in HSV-Varianten identifiziert, die von Patienten isoliert wurden, bei denen acyclovirhaltige Therapien versagen. Die Möglichkeit einer viralen Resistenz gegen Acyclovir sollte bei Patienten in Betracht gezogen werden, die auf die Therapie nicht ansprechen oder bei denen es während der Therapie zu wiederholten Virusausscheidungen kommt.
|
HSV-1 |
TK |
G6C, R32H, R41H, R51W, Y53C/D/H, Y53stop, D55N, G56D/S, P57H, H58/N/R/Y, G59R, G61A, K62N, T63I, Q67stop, S74stop, Y80N, E83K, P84L, Y87H, W88R, R89Q/W, E95stop, T103P, Q104H, Q104stop, H105P, D116N, M121L/R, S123R, Q125H, M128L, G129D, I143V, A156V, D162A/H/N, R163G/H, L170P, Y172C, P173L, A174P, A175V, R176Q/W, R176stop, L178R, S181N, V187M, A189V, V192A, G200C/D/S, T201P, V204G, A207P, L208F/H, R216C/H, R220C/H, R221H, R222C/H, L227F, T245M/P, L249P, Q250Stop, C251G, R256W, E257K, Q261R, T287M, L288Stop, L291P/R, L297S, L315S, L327R, C336Y, Q342Stop, T354P, L364P, A365T |
|
HSV-2 |
TK |
R34C, G39E, R51W, Y53N, G59P, G61W, S66P, A72S, D78N, P85S, A94V, N100H, I101S, Q105P, T131P, D137stop, F140L, L158P, S169P, R177W, S182N, M183I, V192M, G201D, R217H, R221C/H, Q222stop, R223H, Y239stop, R271V, P272S, D273R, T287M, C337Y |
|
HSV-1 |
POL |
K532T, Q570R, L583V, A605V, A657T, D672N, V715G, A719T/V, S724N, F733C, E771Q, S775N, L778M, E798K, V813M, N815S, G841S, I890M, G901V, V958L H1228D |
|
HSV-2 |
POL |
E250Q, D307N, K533E, A606V, C625R, R628C, E678G, A724V, S725G, S729N, I731F, Q732R, M789K/T, V818A, N820S, Y823C, Q829R, T843A, M910T, D912N/V, A915V, F923L, T934A, R964H |
Anmerkung: Es können weitere Substitutionen zur Acyclovir-Resistenz existieren.
Kreuzresistenz
Kreuzresistenz wurde bei HSV-Isolaten beobachtet, die Frameshift-Mutationen und resistenzassoziierte Substitutionen tragen, die eine verminderte Empfindlichkeit gegenüber Penciclovir (PCV), Famciclovir (FCV) und Foscarnet (FOS) verleihen.
|
Kreuzresistenz gegen PCV/FCV |
HSV-1 TK |
G6C, R32H, R51W, Y53C/H, H58N, G61A, S74Stop, E83K, P84L, T103P, Q104Stop, D116N, M121R, I143V, R163H, L170P, Y172C, A174P, R176Q/W, Q185R, A189V, G200D, L208H, R216C, R220H, R222C/H, T245M, Q250Stop, R256W, R281Stop, T287M, L315S, M322K, C336Y |
|
Kreuzresistent gegen PCV/FCV |
HSV-1 POL |
A657T, D672N, V715G, A719V, S724N, E798K, N815S, G841S |
|
Kreuzresistent gegen PCV/FCV |
HSV-2 TK |
G39E, R51W, Y53N, R177W, R221H, T288M |
|
Kreuzresistent gegen PCV/FCV |
HSV-2 POL |
K533E, A606V, C625R, R628C, S729N, Q732R, M789K/T, V818A, N820S, F923L, T934A |
|
Kreuzresistent gegen FOS |
HSV-1 POL |
D368A, A605V, D672N, L702H, V715G, A719T/V, S724N, L778M, E798K, V813M, N815S, V817M, G841C/S, I890M, |
|
Kreuzresistent gegen FOS |
HSV-2 POL |
K533E, A606V, C625R, R628C, A724V, S725G, S729N, I731F, Q732R, M789K/T, V818A, Y823C, D912V, F923L, T934A, R964H |
Nichtklinische Toxikologie
Kanzerogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Die systemische Exposition nach topischer Verabreichung von Aciclovir ist minimal. Dermale Karzinogenitätsstudien wurden nicht durchgeführt. Die Ergebnisse der Studien zur Karzinogenese, Mutagenese und Fertilität sind aufgrund der minimalen Exposition von Acyclovir bei der dermalen Anwendung nicht in der vollständigen Verschreibungsinformation für Zovirax Creme enthalten. Informationen zu diesen Studien sind in der vollständigen Verschreibungsinformation für ZOVIRAX Kapseln, Tabletten und Suspension und ZOVIRAX zur Injektion enthalten.
Klinische Studien
Erwachsene Probanden
Zovirax Creme wurde in zwei doppelblinden, randomisierten, placebokontrollierten Studien zur Behandlung von wiederkehrendem Herpes labialis untersucht. Die durchschnittliche Patientin hatte in den vorangegangenen 12 Monaten fünf Episoden von Herpes labialis. In der ersten Studie lag das Durchschnittsalter der Probanden bei 37 Jahren (Spanne 18 bis 81 Jahre), 74 % waren weiblich und 94 % waren Weiße. In der zweiten Studie lag das Durchschnittsalter der Probanden bei 38 Jahren (Spanne von 18 bis 87 Jahren), 73 % waren weiblich und 94 % waren kaukasisch. Die Probanden wurden angewiesen, die Behandlung innerhalb von 1 Stunde nach dem Auftreten von Anzeichen oder Symptomen zu beginnen und die Behandlung 4 Tage lang fortzusetzen, wobei das Studienmedikament 5-mal täglich anzuwenden war. In beiden Studien war die mittlere Dauer der rezidivierenden Herpes-labialis-Episode bei den mit Zovirax-Creme behandelten Probanden (n = 682) um etwa einen halben Tag kürzer als bei den mit Placebo behandelten Probanden (n = 703), d. h. etwa 4,5 Tage bzw. 5 Tage. Es wurde kein signifikanter Unterschied zwischen Probanden, die Zovirax Creme oder Placebo erhielten, hinsichtlich der Verhinderung des Fortschreitens von Lippenherpesläsionen beobachtet.
Kinder
Eine offene, unkontrollierte Studie mit Zovirax Creme wurde an 113 Patienten im Alter von 12 bis 17 Jahren mit rezidivierendem Herpes labialis durchgeführt. In dieser Studie wurde die Therapie nach demselben Dosierungsschema wie bei Erwachsenen durchgeführt, und die Probanden wurden hinsichtlich unerwünschter Ereignisse beobachtet. Das Sicherheitsprofil war ähnlich wie bei Erwachsenen.
Lagerung und Handhabung
Jedes Gramm Zovirax Creme enthält 50 mg (entsprechend 5 Gew.-%) Aciclovir in einer wässrigen Cremegrundlage. Zovirax Creme wird wie folgt geliefert:
NDC 0187-0994-45: 5 g Tuben
Bewahren Sie die Packung bei oder unter 25°C (77°F) auf; Abweichungen von 15° bis 30°C (59° bis 86°F) sind zulässig.
Patientenberatung
Raten Sie dem Patienten, die von der FDA zugelassene Packungsbeilage (Patienteninformation) zu lesen.
Allgemein
Die Patienten sollten darüber informiert werden, dass Zovirax Creme eine verschreibungspflichtige topische Creme zur Behandlung von Lippenherpes (rezidivierende Herpes labialis) ist, die im Gesicht und an den Lippen auftreten. Zovirax Creme ist kein Heilmittel für Fieberbläschen. Die Patienten sollten darauf hingewiesen werden, dass Zovirax Creme nur zur kutanen Anwendung bei Lippenherpes und Herpes labialis im Mundbereich bestimmt ist. Die Patienten sollten darauf hingewiesen werden, dass Zovirax Creme nicht im Auge, im Mund oder in der Nase oder an den Genitalien angewendet werden darf. Die Patienten sollten angewiesen werden, während der Anwendung von Zovirax Creme keine anderen topischen Produkte auf die betroffene Stelle aufzutragen.
Nicht anwenden, wenn Sie allergisch gegen Zovirax Creme oder einen der Inhaltsstoffe von Zovirax Creme sind. Informieren Sie Ihren Arzt vor der Anwendung von Zovirax Creme, wenn Sie schwanger sind, eine Schwangerschaft planen oder stillen.
Anwendungshinweise
Die Behandlung sollte bei den ersten Anzeichen oder Symptomen eines erneuten Auftretens eingeleitet werden. Weisen Sie die Patienten an, sich vor der Anwendung die Hände zu waschen und sicherzustellen, dass das Gesicht und/oder die Lippen sauber und trocken sind. Weisen Sie die Patienten an, die Zovirax-Creme 4 Tage lang 5 Mal pro Tag topisch aufzutragen. Weisen Sie die Patienten an, eine ausreichende Menge Zovirax-Creme aufzutragen, um den betroffenen Bereich, einschließlich des äußeren Randes, zu bedecken. Weisen Sie die Patienten an, unnötiges Reiben der betroffenen Stelle zu vermeiden, um eine Verschlimmerung oder Übertragung der Infektion zu verhindern. Weisen Sie die Patienten an, sich nach der Anwendung von Zovirax Creme die Hände mit Wasser und Seife zu waschen. Außerhalb der Reichweite von Kindern aufbewahren.
Mögliche Nebenwirkungen
Zu den häufigen hautbezogenen Nebenwirkungen, die bei der Anwendung von Zovirax Creme auftraten, gehören Reaktionen an der Applikationsstelle. Zovirax Creme kann zu Reizungen und Kontaktsensibilisierung führen.
Vertrieben von: Bausch Health US, LLC
Bridgewater, NJ 08807 USA
Hergestellt von: Bausch Health Companies Inc.
Laval, Quebec H7L 4A8, Kanada
Zovirax ist ein eingetragenes Warenzeichen der GlaxoSmithKline Unternehmensgruppe und wird von Bausch Health unter Lizenz verwendet.
© 2020 Bausch Health Companies Inc. or its affiliates
9462203
PATIENTENINFORMATIONENZOVIRAX (zho-vahy-rex)(acyclovir)Creme
Wichtige Informationen: Zovirax Creme ist nur zur Anwendung bei Lippenbläschen und um den Mund herum bestimmt. Zovirax Creme sollte nicht in den Augen, im Mund, in der Nase oder auf den Genitalien angewendet werden.
Was ist Zovirax Creme?
– Zovirax Creme ist ein verschreibungspflichtiges Arzneimittel zur Behandlung von Lippenherpes (Herpes labialis), der bei Erwachsenen und Kindern ab 12 Jahren und mit normalem Immunsystem immer wieder auftritt. – Zovirax Creme ist kein Heilmittel für Fieberbläschen.
Es ist nicht bekannt, ob Zovirax Creme bei Kindern unter 12 Jahren sicher und wirksam ist.
Wenden Sie Zovirax Creme nicht an, wenn Sie auf Aciclovir, Valacyclovir oder einen der sonstigen Bestandteile von Zovirax Creme allergisch sind. Eine vollständige Liste der Inhaltsstoffe von Zovirax Creme finden Sie am Ende dieser Packungsbeilage.
Was sollte ich meinem Arzt vor der Anwendung von Zovirax Creme mitteilen?
Bevor Sie Zovirax Creme anwenden, informieren Sie Ihren Arzt über alle Ihre Beschwerden, einschließlich wenn Sie:
– sehr leicht krank werden (ein schwaches Immunsystem haben). – schwanger sind oder planen, schwanger zu werden. Es ist nicht bekannt, ob Zovirax Creme Ihrem ungeborenen Kind schaden kann. – stillen oder planen, zu stillen. Es ist nicht bekannt, ob Zovirax Creme in Ihre Muttermilch übergeht. Sprechen Sie mit Ihrem medizinischen Betreuer darüber, wie Sie Ihr Baby am besten ernähren, wenn Sie Zovirax Creme anwenden.
Informieren Sie Ihren Arzt oder Apotheker über alle Arzneimittel, die Sie einnehmen, einschließlich rezeptpflichtiger und rezeptfreier Arzneimittel, Vitamine und pflanzlicher Präparate.
Wie soll ich Zovirax Creme anwenden?
– Wenden Sie Zovirax Creme genau nach Anweisung Ihres Arztes oder Apothekers an. – Wenden Sie Zovirax Creme an, sobald Sie die ersten Symptome eines Fieberbläschen wie Juckreiz, Rötung, Brennen oder Kribbeln verspüren, oder wenn das Fieberbläschen auftritt. – Waschen Sie sich vor und nach der Anwendung von Zovirax Creme die Hände mit Wasser und Seife. – Die betroffene Stelle sollte sauber und trocken sein, bevor Sie Zovirax Creme auftragen. – Tragen Sie die Zovirax-Creme 4 Tage lang 5-mal täglich auf die betroffene Stelle auf, auch auf den äußeren Rand. – Sie sollten während der Behandlung mit Zovirax Creme keine anderen Hautprodukte auf die betroffene Stelle auftragen. – Vermeiden Sie unnötiges Reiben des Fieberbläschen, da dies dazu führen kann, dass sich das Fieberbläschen auf andere Bereiche um Ihren Mund herum ausbreitet oder Ihr Fieberbläschen verschlimmert.
Was sind die möglichen Nebenwirkungen von Zovirax Creme?
Die häufigsten Nebenwirkungen von Zovirax Creme sind Hautreaktionen an der Behandlungsstelle und können sein: trockene oder rissige Lippen, Schälen, Schuppenbildung oder Trockenheit der Haut, ein brennendes oder stechendes Gefühl und Juckreiz.
Dies sind nicht alle möglichen Nebenwirkungen von Zovirax Creme. Wenden Sie sich an Ihren Arzt, um medizinischen Rat zu Nebenwirkungen zu erhalten. Sie können Nebenwirkungen der FDA unter 1-800-FDA-1088 melden.
Wie sollte ich Zovirax Creme lagern?
– Lagern Sie Zovirax Creme bei Raumtemperatur zwischen 68° bis 77°F (20° bis 25°C).
Bewahren Sie Zovirax Creme und alle Arzneimittel für Kinder unzugänglich auf.
Allgemeine Hinweise zur sicheren und wirksamen Anwendung von Zovirax Creme.
Manchmal werden Arzneimittel für andere Zwecke verschrieben, als in der Packungsbeilage angegeben. Verwenden Sie Zovirax Creme nicht für eine Erkrankung, für die sie nicht verschrieben wurde. Geben Sie Zovirax Creme nicht an andere Personen weiter, auch wenn diese die gleichen Symptome haben wie Sie. Sie kann ihnen schaden. Sie können Ihren Apotheker oder Gesundheitsdienstleister nach Informationen über Zovirax Creme fragen, die für medizinisches Fachpersonal geschrieben wurden.
Was sind die Bestandteile von Zovirax Creme?
Wirkstoff: Acyclovir
Inaktive Bestandteile: Cetostearylalkohol, Mineralöl, Poloxamer 407, Propylenglycol, Natriumlaurylsulfat, Wasser und weiße Vaseline
Vertrieben von: Bausch Health US, LLC
Bridgewater, NJ 08807 USA
Hergestellt von: Bausch Health Companies Inc.
Laval, Quebec H7L 4A8, Kanada
Zovirax ist eine eingetragene Marke der GlaxoSmithKline Gruppe, die unter Lizenz von Bausch Health verwendet wird.
© 2020 Bausch Health Companies Inc. oder ihre Tochtergesellschaften
Für weitere Informationen rufen Sie bitte 1-800-321-4576 an.
Diese Patienteninformation wurde von der U.S. Food and Drug Administration genehmigt.
Aktualisiert: 12/2020
9462203
Hauptanzeigefeld – 5g Tube Karton
ZOVIRAX®
(ACYCLOVIR) CREAM 5%
NDC 0187-0994-45
Net Wt. 5 g
Jedes Gramm enthält:
50 mg Acyclovir, Cetostearylalkohol, Mineralöl, Poloxamer 407, Propylenglycol, Natriumlaurylsulfat, Wasser und weiße Vaseline.
Nur zur Behandlung von kalten Wunden verwenden.
Nur zur äußerlichen Anwendung geeignet.
Ortho Dermatologics
Nur Rx
| ZOVIRAX Acyclovir Creme |
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
Labeler – Bausch Health US, LLC (831922468)
| Einrichtung | |||
| Name | Adresse | ID/FEI | Betrieb |
| Bausch Health Companies Inc. | 245141858 | MANUFACTURE(0187-0994) | |
Mehr über Zovirax Creme (Acyclovir topisch)
- Nebenwirkungen
- Während der Schwangerschaft oder Stillzeit
- Dosierungshinweise
- Medikamentöse Wechselwirkungen
- Preisgestaltung & Gutscheine
- 39 Bewertungen
- Medikamentenklasse: Topische Virostatika
Ressourcen für Verbraucher
- Patienteninformationen
Ressourcen für Fachleute
- Rezeptinformationen
- Acyclovir-Salbe (FDA)
Andere Formulierungen
- Zovirax
- Zovirax-Salbe
Verwandte Behandlungsleitfäden
- Herpes Simplex
- Kaltbläschen
Medizinischer Haftungsausschluss