Ein „Mineral“ ist eine anorganische Substanz, die aus einem oder mehreren chemischen Elementen besteht. Laut Definition muss ein Mineral sein:
Die chemische Zusammensetzung eines Minerals wird als seine elementare Zusammensetzung bezeichnet. Die meisten Minerale kommen als Verbindungen (eine Kombination mehrerer verschiedener Elemente) vor. Einige Minerale kommen jedoch auch als eigenständige chemische Elemente vor. Diese werden als native Mineralien bezeichnet.
Was sind Kristalle?
Kristalle sind eine feste Substanz, die eine organisierte kristalline Struktur besitzt, die aus Atomen gebildet ist. Die innere Anordnung der Atome führt oft zu äußeren ebenen Flächen, wie man sie bei einem Quarzkristall sieht, was jedoch keine Voraussetzung für die Einstufung als Kristall ist. Kristalle können anders klassifiziert werden als Mineralien, da einige Materialien als organische Kristalle betrachtet werden können. Da Mineralien rein anorganisch sind, kann ein organischer Kristall kein Mineral sein. Proteine und Zucker sind beispielsweise Feststoffe, die Kristalle bilden können. Da es sich jedoch um organische Substanzen handelt, können sie nicht als Mineralien eingestuft werden.

Verunreinigungen in Lösungen, die Kristalle bilden, können zu Farbveränderungen sowie zu erheblichen Veränderungen der Kristallstruktur führen. Zu viele Verunreinigungen innerhalb eines Kristallgitters während der Kristallisation können Kristalle mit kleinen bis großen Einschlüssen erzeugen. Diese Einschlüsse können auch die Form des Kristalls verändern.
Mineralien, Kristalle oder Gesteine?
Die meisten Mineralien kommen in der Natur als Kristalle vor, aber nicht alle Kristalle sind Mineralien, da organische Kristalle überhaupt keine Mineralien sind. Ein Mineral mit der gleichen chemischen Formel kann mehr als eine Art von Kristall bilden. So gibt es beispielsweise drei polymorphe Formen (gleiche chemische Formel, unterschiedliche Kristallstrukturen) von Kalziumkarbonat, die als Kalzit, Aragonit und Vaterit bekannt sind. Calcitkristalle kommen im trigonalen System vor, Aragonitkristalle gehören zum orthorhombischen System und Vateritkristalle bilden sich im hexagonalen System. Diese kristallinen Strukturen können sich während der Bildung aufgrund verschiedener Faktoren verändern, darunter Verunreinigungen, die das Wachstum hemmen, die Temperatur der Umgebung während der Bildung, die Sättigung der Mineralien in der Lösung, die Geometrie der kovalenten Bindungen und Veränderungen in der Bewegung der Lösung.
Mineralien haben eine natürlich entstandene, organisierte atomare Struktur mit einer spezifischen chemischen Zusammensetzung. Kristalle weisen größtenteils die gleichen Merkmale auf, allerdings sind die Atome in einem sich wiederholenden Muster angeordnet, das ein Kristallgitter ergibt, das oft Kristallflächen aufweist.
Man hört oft, dass Mineralien oder Kristalle als Gesteine bezeichnet werden, aber ein „Gestein“ ist definiert als ein gebundenes Aggregat von Mineralien, Mineraloiden oder Fragmenten anderer Gesteine. Das Wort „gebunden“ bedeutet, dass die Ansammlung von Mineralien in gewisser Weise zusammengehalten werden muss. So gilt beispielsweise Sand nicht als Gestein, obwohl die Sandkörner in den meisten Fällen miteinander verbunden sind. Sandstein beispielsweise ist zu einem Gestein geworden, weil die Sandkörner durch feinkörnigere Minerale und/oder organisches Material zusammengekittet wurden und so eine relativ feste Masse bilden.
Die drei Hauptkategorien von Gesteinen sind Eruptivgestein, Metamorphit und Sedimentgestein.
Eruptivgestein – Gestein, das durch die Abkühlung und Kristallisation von Magma innerhalb oder oberhalb der Lithosphäre (Erdkruste) entstanden ist. Kristalle bilden sich im Magma, wenn es zu erstarren beginnt, wobei die Geschwindigkeit der Abkühlung die Größe der entstehenden Kristalle bestimmen kann.

Eine Nahaufnahme von porphyrischem Granit, einer Art von Eruptivgestein. Porphyrischer Granit entsteht, wenn sich die Temperatur des Magmas beim Abkühlen schnell ändert. In diesem Fall konnten sich bei langsamer Abkühlung große Kristalle bilden, die dann durch einen plötzlichen Temperaturabfall unterbrochen wurden, der den Kristallisationsprozess beschleunigte und zu kleineren Kristallen führte.
Sedimentäres Gestein – Gestein, das sich aus erodiertem Material früherer Gesteine gebildet hat, die sich entlang von Meeresböden, Flussbetten, Seebetten usw. abgelagert haben, zusammen mit der Ablagerung von Mineralien aus dem Wasser. Im Laufe der Jahre werden diese Ablagerungen durch natürliche Kräfte verdichtet und verfestigen sich später zu einer festen Masse (Gestein).

Dies ist eine sedimentäre Gesteinsformation, die zum Zabriskie Point im Death Valley, Kalifornien, gehört. Sie besteht aus Sedimenten des Furnace Creek Lake, der vor etwa 5 Millionen Jahren austrocknete. Millionen von Jahren der Erosion haben die Sedimentschichten freigelegt.
Metamorphes Gestein – Gestein, das entstand, als bestehendes Sediment- oder Eruptivgestein Druck und in einigen Fällen Temperaturänderungen ausgesetzt wurde, die seine ursprüngliche Mineralogie veränderten.

Metamorphes Gestein, das als „Granitgneis“ bezeichnet wird. Entsteht aus metamorphosiertem Granit.
Wie entstehen anorganische Kristalle?
Kristalle können durch eine Vielzahl verschiedener Prozesse entstehen, darunter:
Evaporitlagerstätten – Dies sind Mineralformationen, die durch Prozesse an der Erdoberfläche entstehen. Kristalle bilden sich aus mineralhaltigen Lösungen, die sich durch Dehydrierung/Verdampfung einer wässrigen Lösung konzentrieren. Während die Flüssigkeit langsam durch Verdunstung entfernt wird, sammeln sich die konzentrierten Mineralien und fallen in einem strukturierten Muster aus dem Wasser aus, das sich zu einem Kristall entwickelt. Ein Beispiel für Fällungsablagerungen sind die rosa Halitkristalle aus dem Seamless Lake in Trona, Kalifornien.
Sekundäre Mineralablagerungen – Sie bilden sich durch den Kontakt von Wasser mit primären Erzen, durch Ablagerung aus hydrothermalen Lösungen oder durch die Kristallisation von Magma.
- Kontakt mit primären Erzen – Wasser, das durch abwärts gerichtete Perkolation durch Gestein in freiliegende Erze (typischerweise in einem Hohlraum) gelangt. Dadurch können chemische Prozesse in Gang gesetzt werden, die das Erz aufspalten und die Mineralien entlang der offenen Hohlraumwände umverteilen. Azurit und Malachit sind gute Beispiele dafür, wo sich wässrige Lösungen durch Bereiche von primärem Kupfererz bewegt und diese als Azurit- und Malachitkristalle umverteilt haben, zu deren Bildung Wasser, Karbonate und Kupfer erforderlich sind.
- Hydrothermale Flüssigkeitsablagerung – tritt in den meisten Fällen auf, wenn sich hydrothermale Flüssigkeiten ihren Weg nach oben durch das Gestein bahnen und dabei Mineralien aus dem umgebenden Gestein aufnehmen. Wenn diese Fluide einen offenen Hohlraum vorfinden, können sich die Mineralien in Form von Kristallen und/oder einer festen Masse ablagern. Manchmal können die Mineralien im umgebenden Gestein ersetzt werden, was als Ersatzlagerstätte bekannt ist.
- Kristallisation von Magma – tritt auf, wenn Magma abkühlt und die Mineralien im Magma beginnen, sich in Gruppen gleichartiger und kompatibler Mineralien zu trennen. Je nach Geschwindigkeit der Abkühlung, der Zusammensetzung und der Atmosphäre kann die Größe der Kristalle erheblich variieren. Manchmal erfolgt die Abkühlung zu schnell, was dazu führt, dass keine elementare Struktur vorhanden ist; Obsidian (vulkanisches Glas) ist ein Beispiel dafür. Obsidian besteht in erster Linie aus SiO₂ (in den meisten Fällen Quarz) und hat eine chemische Formel, die das Potenzial hat, ein Kristall/Mineral zu sein; das Fehlen einer kristallinen Struktur und die Variabilität der Zusammensetzung führen jedoch dazu, dass es stattdessen als Mineraloid klassifiziert wird.

Das Mineraloid Obsidian.
Mineralklassen
Die chemische Zusammensetzung des Minerals bestimmt, wie es in der Natur vorkommt. Einige der gebräuchlichen Mineralklassen nach ihrer chemischen Zusammensetzung sind:
Native Mineralien – Elemente, die in der Natur mit einer eindeutigen Mineralstruktur und ohne Kombination mit einem anderen Element vorkommen. Einige Beispiele für Elemente, von denen bekannt ist, dass sie sich als native Minerale bilden, sind Gold (Au), Silber (Ag), Schwefel (S), Kupfer (Cu), Graphit ((C) – locker gepackter Kohlenstoff) und Diamanten ((C) – dicht gepackter Kohlenstoff – enthält normalerweise einige Verunreinigungen).

Rauer Naturdiamant

Natives Silber

Natives Kupfer
Oxide – Eine Klasse chemischer Verbindungen, bei denen sich ein Sauerstoffion (O2-) mit einem Element verbindet, in vielen Fällen ein positiv geladenes Metall. Einige Beispiele hierfür sind SiO₂ – Quarz, Fe₂O₃ – Hämatit, Cu₂O – Cuprit, usw.
Carbonate – Mineralien, die durch das Vorhandensein eines Carbonat-Ions (CO₃2-) gekennzeichnet sind. Sie sind in der Regel an Metallkationen gebunden, die in den meisten Fällen unlösliche Verbindungen bilden (nicht in Wasser auflösbar). Einige Beispiele hierfür sind CaCO₃ – Calcit/Aragonit, FeCO₃ – Siderit, ZnCO₃ – Smithsonit usw.
Silikate – Mineralien aus einer Familie von Anionen, die sowohl Silizium (Si) als auch Sauerstoff (O) enthalten. Dieses Salz bildet einen Hauptbestandteil der Gesteine in der Lithosphäre (Erdkruste). Einige Beispiele für Silikate sind SiO₂ – Quarz, AlKO₆Si₂ – Kalium-Aluminium-Silikat, (Fe,Mg)₂SiO₄ – Olivin, usw.
Sulfid (Sulfid) – Anorganisches Schwefelanion mit der chemischen Formel S^2-, das recht komplexe Reaktionen auslösen kann. Die Ausfällung von Sulfiden kann Reaktionen mit Schwermetallen einschließen, bei denen sich unlösliche Metallausfällungen bilden. Einige Beispiele für diese Schwermetalle, die sich aus Sulfidionen bilden, sind FeS₂ – Pyrit, CuFeS₂ – Chalkopyrit, PbS – Bleiglanz usw.
Sulfate (Sulfate) – Salze, die entstehen, wenn Schwefelsäure (H₂SO₄) mit einer anderen Chemikalie reagiert. Einige Beispiele für Sulfate sind (Ba,Sr)SO₄ – Baryt, CaSO₄- 2H₂O – Gips, SrSO₄ – Coelestin usw.
Phosphate – Mineralien, die durch das Vorhandensein des komplexen Anions (PO₄)^3- gekennzeichnet sind und von denen die meisten in der Natur recht selten vorkommen. Einige Beispiele für Phosphate sind Ca5(PO₄)(OH,F,CL) – Apatit, CuAl₆(PO₄)₄(OH)₈ – 4H₂O – Türkis, Fe(II)3(PO4)₂- 8H2O – Vivianit, usw.
Ökonomie der Kristalle und Mineralien
In der heutigen Zeit wird ein Mineral nur dann als wirtschaftlich abbauwürdig angesehen, wenn es in einer Konzentration von Nutzmineralien vorliegt, die mit Gewinn abgebaut werden kann. Die Konzentration muss außerdem hoch genug sein, um den Abbau lohnend zu machen. In manchen Fällen kann das Ende des Minerals in der Mine zur sofortigen Schließung der Mine führen. Aus diesem Grund kann der Bergbau aus wirtschaftlicher Sicht ein besonders riskantes Geschäft sein.
Metalle sind derzeit die wichtigsten wirtschaftlichen Mineralien, da sie für eine Vielzahl moderner Anwendungen genutzt werden. Diese Metalle werden aus metallhaltigen Lagerstätten gewonnen, die aus dem Erz (den begehrten Mineralien) und in den meisten Fällen aus den unerwünschten, weniger wirtschaftlichen Umgebungsmineralien bestehen, die als „Gangue“ bezeichnet werden.
Terminologie und Illustrationen
Chemisches Element – Ein chemisches Element ist ein Stoff, dessen Atome alle die gleiche Anzahl von Protonen enthalten, die als Ordnungszahl bezeichnet wird. Das Periodensystem ist gewissermaßen ein Schlüssel, der von Dimitri Mendelejew, einem russischen Chemiker, erstellt wurde, um diese Atome anhand ihrer Protonenzahl in Elementkategorien einzuteilen. Zum Beispiel enthält ein Wasserstoffatom (H) ein Proton, ein Heliumatom (He) zwei Protonen, ein Lithiumatom (Li) drei Protonen und so weiter und so fort.
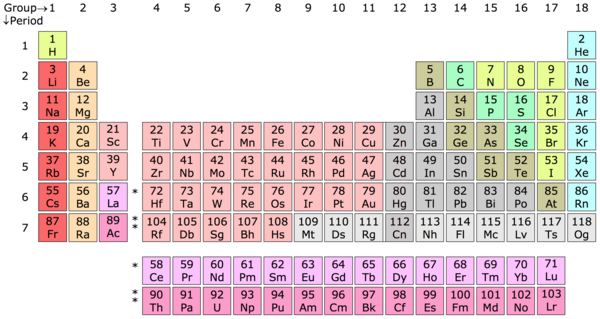
Periodensystem
Chemische Verbindung – Besteht aus Molekülen. Um als chemische Verbindung zu gelten, muss das Molekül aus bis zu zwei oder mehr verschiedenen chemischen Elementen bestehen, die miteinander verbunden sind.
Atom – Die kleinste Einheit eines chemischen Elements. Ein Atom besteht aus Proton(en), Elektron(en) und Neutron(en), die zusammen die Ladung des Atoms bestimmen. Atome können Elektronen verlieren oder gewinnen, was zu positiven und negativen Ladungen führt, die als Ionen bezeichnet werden.
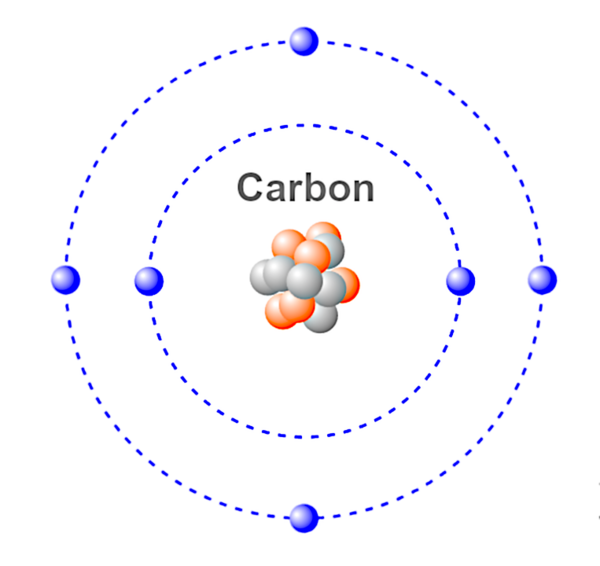
Dies ist eine Illustration eines Kohlenstoffatoms.
Blau – Elektronen.
Rot &Grau – Neutronen &Protonen.
Ion – Ein Atom oder Molekül mit einer elektrischen Ladung, die durch den Verlust oder Gewinn eines oder mehrerer Elektronen entstanden ist.
Kation – Ein positiv geladenes Ion, das von negativ geladenen Ionen angezogen wird. Beispiel – Wasserstoffion H+.
Anion – Ein negativ geladenes Ion, das von positiv geladenen Ionen angezogen wird. Beispiel – Carbonat-Ion ist CO₃2-.

Carbonat-Ion chemische Formel.
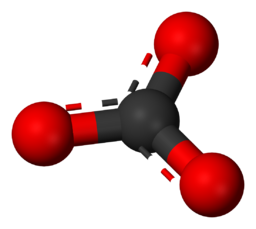
Dieses Bild zeigt die Molekularstruktur eines Carbonat-Ions (CO₃2-) auf atomarer Ebene.