INDLEDNING
Heterozygot familiær hyperkolesterolæmi (FH) er en almindelig genetisk lidelse, der er forbundet med for tidlig aterosklerotisk kardiovaskulær sygdom (ASCVD). Børn med ubehandlet FH har en øget risiko for tidlig ASCVD efter 20-årsalderen.1 Den alvorlige forhøjelse af low-density lipoproteinkolesterol (LDL-C) begynder allerede hos fosteret og fører til vedvarende eksponering af arterievæggen for LDL-C, hvilket fremskynder kolesterolaflejring og vaskulær inflammation og prædisponerer for tidlig påbegyndelse af aterosklerose, især i kranspulsårerne og aorta.
Statiner og andre lipidsænkende behandlinger (LLT) sænker effektivt LDL-C, er sikre hos børn og unge og genopretter endothelfunktionen i en tidlig alder.2-4 For nylig er der blevet foreslået universel screening af børn fra 2-årsalderen og før 8-årsalderen5,6 for at opdage personer, der kræver behandling. Denne tilgang er imidlertid baseret på teoretiske overvejelser og er ikke blevet bevist i virkeligheden.
Det er ikke desto mindre kun lidt kendt om karakteristika for FH-patienter yngre end 18 år, den LLT, der anvendes til disse patienter, og de lipidmål, der nås i virkeligheden. Informationsunderskuddet er endnu større for opfølgningsdata. Nationale registre kan anvendes til at tilvejebringe disse afgørende oplysninger, som er nødvendige for at forbedre modellerne for pleje af FH, terapeutiske protokoller og sundhedspolitik7,8 . SpAnish Familial HypErcHolEsterolaemiA CohoRt STudy (SAFEHEART) (NCT02693548) blev designet med henblik på at forbedre indsigten i de prognostiske faktorer og mekanismer, der påvirker udviklingen af ASCVD og dødelighed i en FH-population.
Vores mål var at analysere patientkarakteristika og vurdere LLT- og lipidmål ved inklusion og under opfølgning hos FH-patienter yngre end 18 år, der er indskrevet i SAFEHEART, og at bestemme de faktorer, der forudsiger sandsynligheden for opfyldelse af disse mål.
METHODSStudiedesign og population
SAFEHEART er en åben, multicenter, landsdækkende, langsigtet prospektiv kohorteundersøgelse i en molekylært defineret FH-population i Spanien. Rekrutteringen af deltagere fra FH-familier begyndte i 2004 og er stadig i gang. Inklusionskriterierne var indekstilfælde med en genetisk diagnose af FH og deres slægtninge ældre end 15 år med en genetisk diagnose af FH samt deres slægtninge uden en genetisk diagnose af FH (kontrolgruppe). Ikke desto mindre blev deltagere under 15 år også optaget, hvis deres forældre anmodede om det. Denne undersøgelse blev godkendt af de lokale etiske komitéer. Alle støtteberettigede personer og/eller mindst en af deres forældre eller værger gav skriftligt informeret samtykke. Et koordinerende center med base i Madrid, Spanien, var ansvarligt for opfølgningen af deltagerne. Patienterne og/eller deres forældre blev kontaktet årligt ved hjælp af et standardiseret telefonopkald for at registrere relevante ændringer i livsstilsvaner og medicinering og eventuelle kardiovaskulære hændelser eller andre medicinske problemer. De deltagende læger, der tilmeldte patienter og familier til dette register, modtog uddannelse, hvor retningslinjerne for bedste praksis blev styrket på årlige møder med deltagelse af læger med ekspertise på området; desuden blev der anvendt et elektronisk baseret program og telefonrådgivning, og der blev anvendt et webbaseret uddannelsesprogram til yderligere støtte for håndteringen, når det var nødvendigt. Behandlingsbeslutninger blev udelukkende truffet af den enkelte patients læge.
Kliniske og laboratoriemålinger
Demografiske og kliniske karakteristika blev registreret som beskrevet andetsteds.9 Venøse blodprøver blev taget efter 12 timers faste. Serum-, plasma- og DNA-prøver blev aliquoteret og opbevaret ved -80°C. Serum total kolesterol, triglycerider og high-density lipoproteinkolesterol (HDL-C) blev målt i et centralt laboratorium ved hjælp af enzymatiske metoder. LDL-C-koncentrationen i serum blev beregnet ved hjælp af Friedewald-formlen. DNA blev isoleret fra fuldblod ved hjælp af standardmetoder, og FH blev genetisk diagnosticeret ved hjælp af et DNA-mikroarray.10 LDL-C-målene blev defineret i overensstemmelse med de seneste anbefalinger og målsætninger. Low-density lipoproteinkolesterol
mg/dL var det primære mål.11 Et alternativt mål for patienter under 14 år bestod af LDL-C mg/dL i fravær af andre kardiovaskulære risikofaktorer (rygning, HDL-C mg/dL, lipoprotein (a) > 50mg/dL eller LDL-C > 250mg/dL) eller for tidlig kardiovaskulær sygdom hos forældrene eller bedsteforældrene.6 For tidlig kendt ASCVD blev defineret som forekomsten af en første hændelse før 55 års alderen hos mænd og før 65 års alderen hos kvinder.Klassifikation af lipidsænkende terapi
Maximal statindosis blev defineret som atorvastatin 40 til 80 mg/d eller rosuvastatin 20 til 40 mg/d, som blev betragtet som statindoser med høj intensitet. Maksimal kombineret behandling blev defineret som maksimal statindosis plus ezetimibe 10 mg/d. Maksimal LLT blev defineret som enhver LLT, der forventes at give en reduktion på mindst 50 % af LDL-C-grundniveauet: simvastatin 20, 40 eller 80 mg/d plus ezetimibe 10 mg/d; pravastatin 40 mg/d i kombination med ezetimibe 10 mg/d; fluvastatin 80 mg/d plus ezetimibe 10 mg/d; atorvastatin 40 eller 80 mg/d med eller uden ezetimibe 10 mg/d; atorvastatin 10 eller 20 mg/d plus ezetimibe 10 mg/d; rosuvastatin 20 eller 40 mg/d med eller uden ezetimibe 10 mg/d; rosuvastatin 10 mg/d plus ezetimibe 10 mg/d; og pitavastatin 4 mg/d i kombination med ezetimibe 10 mg/d.12,13
Genetisk analyse
Low-density lipoprotein cholesterolreceptor (LDLR)-mutationer blev klassificeret i henhold til deres kendte virkning på LDL-receptorproteinets funktion som nul- (receptor-negative) og defekte (receptor-defekte) mutationer som tidligere beskrevet.14 Varianter, der fører til fuldstændig fravær eller trunkering af proteinet (tab af funktion) påvist ved in vitro funktionel analyse eller computersimuleringsanalyse, blev klassificeret som receptor-negative. Disse varianter omfattede følgende: a) punktmutationer, der forårsager et for tidligt stopkodon; b) missense-mutationer, der påvirker den femte cysteinrige gentagelse i det ligandbindende domæne i LDL-C-receptorgenet (klasse 2A-mutation); c) små deletioner eller insertioner, der forårsager et frame shift og et for tidligt stopkodon; og d) store rearrangementer. Receptor-defekte mutationer var de resterende inframe-punktmutationer og små inframe-deletioner og -indsættelser. Alle mutationer uden kendt funktionalitetsanalyse ved hjælp af in vitro-undersøgelser eller computersimuleringsanalyse blev klassificeret som “ukendt funktionalitet”, fordi vi ikke kunne være sikre på, om virkningen på receptoren var negativ eller defekt; de blev imidlertid betragtet som patogene, fordi alle personer, der bar 1 af disse mutationer, havde hyperkolesterolæmi, mens slægtninge uden mutationen havde normale kolesterolniveauer.14
Statistiske analyser
Statistiske analyser blev udført ved hjælp af SPSS version 18.0 (SPSS Inc, Chicago, Illinois, USA). Normaliteten af fordelingen af variablerne blev analyseret med Kolmogorov-Smirnov-testen. Kvantitative data er udtrykt som median og interkvartilområde (IQR) og kvalitative data som absolut antal og procentdel. Der blev defineret to populationer: populationen ved indgangen (n = 241) og populationen ved opfølgningen (også kendt som kohorten), som omfattede de patienter, der havde en fuldstændig plasmalipidprofil ved opfølgningen (n = 217). Alle sammenligninger mellem indgang og opfølgning blev foretaget i kohorteundersøgelsen. Sammenligninger af frekvenser mellem kvalitative variabler blev udført ved hjælp af chi-kvadrat-testen. Ændringer i binære variabler blev analyseret ved hjælp af McNemar-testen. Medianværdier af kvantitative variabler blev sammenlignet med den ikke-parametriske Mann-Whitney-test eller den parrede Wilcoxon signed rank-test, alt efter hvad der var relevant. Der blev foretaget en fremadrettet binær logistisk regressionsanalyse i kohorteundersøgelsen for at bestemme de variabler, der var forbundet med statinbrug. Vi inkluderede variabler, der var statistisk signifikante i univariate analyser, samt a priori prædiktorer og confoundere: alder, køn og opfølgning i en primær/specialiseret indstilling. En anden fremadrettet binær logistisk regressionsanalyse blev udført i kohortestudiet med udelukkelse af de patienter, der nåede målet ved indgangen, for at bestemme de variabler, der er forbundet med opnåelse af LDL-C
mg/dL. Vi inkluderede variabler, der var statistisk signifikante i univariate analyser, samt a priori prædiktorer og confoundere: alder, køn, mutationstype (nul eller defekt), brug af ezetimibe og opfølgning i en primær/specialiseret indstilling. Forskelle blev betragtet som statistisk signifikante ved P RESULTATER
Til dato er 4141 deltagere blevet indskrevet i SAFEHEART-registret; 392 er yngre end 18 år. Af disse har 241 en molekylær bekræftelse af FH, og 217 er fulgt op med en komplet lipidprofil (90,0 %) (figur 1). Fireogtyve patienter blev udeladt fra analysen på grund af manglen på en komplet lipidprofil ved opfølgningen. Opfølgningen fandt sted i en primærplejeindstilling for 40 patienter (18,4 %). Den mediane opfølgningstid var 4,69 år (IQR, 2,48-6,38 år).
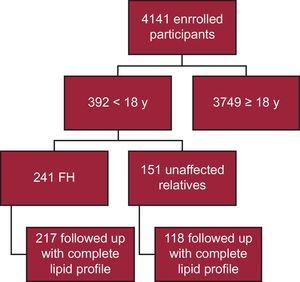
Skematisk flowdiagram over undersøgelsen. FH, familiær hyperkolesterolæmi.
Ved indskrivningen (populationen ved indskrivningen) var 129 FH-patienter (53,5 %) mænd. Medianalderen var 15,0 år (IQR, 14,0-16,0 år). De 2 yngste patienter var 8 år gamle. ASCVD-historie var ikke til stede hos nogen patienter, og for tidlig familiær ASCVD var til stede hos 40 (16,6 %). Baselinekarakteristika er afbildet i tabel 1. En sammenligning af baselinekarakteristika ved inklusion mellem kohortepatienter og de patienter, der ikke blev fulgt op, er vist i tabel 1. Der blev ikke fundet nogen signifikante forskelle mellem de 2 grupper. Ingen patienter havde en historie med ASCVD, højt blodtryk eller diabetes mellitus. En større andel af gruppen uden opfølgning blev behandlet i den primære sundhedspleje, selv om forskellen ikke var statistisk signifikant. I kohorten var der signifikante reduktioner i plasmakoncentrationerne af totalkolesterol, LDL-C, triglycerider og non-HDL-C; der blev også observeret en signifikant stigning i HDL-C ved opfølgningen (tabel 2).
Baselinekarakteristika for populationen ved indgangen
| FH-patienter med opfølgning Median (IQR)/nr. (%) |
FH-patienter uden opfølgning Median (IQR)/nr. (%) |
P | ||
|---|---|---|---|---|
| Antal | 217 | 24 | ||
| Køn (mand) | 117 (53,9 %) | 12 (50 %) | 12 (50 %) | .72 |
| Alder, y | 15,0 (14,0-16,0) | 15,0 (13,0-15,8) | .06 | |
| Premature familiar ASCVD | 36 (16,6%) | 4 (16,7%) | 1.00 | |
| Aktiv tobaksryger | 13 (6,0%) | 2 (8,3%) | .65 | |
| Xanthomer | 1 (0,5%) | 0 (0,0%) | .99 | |
| Corneal arcus | 6 (2,8 %) | 1 (4,2 %) | .53 | |
| BMI, kg/m2 | 21,09 (19,40-22,80) | 20,79 (17,80-22,70) | .64 | |
| Brystomkreds, cm | 72,0 (66,0-78,0) | 72,0 (66,0-75,8) | .94 | |
| Totalt kolesterol, mg/dL | 223,5 (194,0-262.3) | 217,5 (194,5-277,5) | .76 | |
| LDL-C, mg/dL | 162,6 (133.0-195,8) | 153,9 (13,1-209,3) | .71 | |
| HDL-C, mg/dL | 49.0 (42,8-55,0) | 48,5 (41,5-56,0) | .96 | |
| TG, mg/dL | 62,0 (49.0-80,3) | 66,0 (42,1-82,3) | .90 | |
| Non-HDL-C, mg/dL | 174.0 (145,8-210,9) | 167,0 (146,5-225,3) | .74 | |
| Lp (a), mg/dL | 18,80 (7,00-48,50) | 13,45 (9,10-28,10) | .46 | |
| Håndteres i primærsektoren | 40 (22,9 %) | 7 (46,7 %) | .06 |
ASCVD, aterosklerotisk kardiovaskulær sygdom; BMI, kropsmasseindeks; FH, familiær hyperkolesterolæmi; HDL-C, lipoproteinkolesterol med høj densitet; LDL-C, lipoproteinkolesterol med lav densitet; Lp (a), lipoprotein (a); IQR, interkvartilinterval; TG, triglycerider.
Lipid- og lipoproteinkoncentrationer i plasma (kohorte)
| Kohorte ved indtræden | Kohorte ved opfølgning-op | P | ||
|---|---|---|---|---|
| Total kolesterol, mg/dL | 221.0 (194.0-260.2) | 203.0 (183.0-233.5) | .001 | |
| LDL-C, mg/dL | 157,7 (132,8-194,5) | 138,0 (116,5-165.4) | .001 | |
| HDL-C, mg/dL | 49.0 (43.0-55.0) | 50.0 (44.0-58.0) | .002 | |
| TG, mg/dL | 62,0 (49,0-80,2) | 70,0 (54,5-91.0) | .004 | |
| Non-HDL-C, mg/dL | 171,0 (145,8-209,2) | 154.0 (132,0-182,5) | .001 |
HDL-C, lipoproteinkolesterol med høj densitet; LDL-C, lipoproteinkolesterol med lav densitet; TG, triglycerider.
Værdierne er median (interkvartilområde).
Funktionelle mutationer
Vi identificerede 212 patienter med en mutation i LDL-C-receptorgener (97,7%) og 5 patienter med en mutation i apolipoprotein B-gener (2,3%). Af mutationerne i LDL-C-receptorgener blev 95 (43,8 %) klassificeret som nulmutationer, 92 (42,4 %) som defekte mutationer og 25 (11,5 %) som mutationer med ukendt funktionalitet.
Lipidsænkende terapi og målopfyldelse
Tabel 3 viser brugen af forskellige LLT-regimer ved indgangen og opfølgningen. Resultaterne viser en signifikant stigning i brugen af statiner (44,2 % ved indgang og 68,2 % ved opfølgning), ezetimib (8,7 % ved indgang og 15,2 % ved opfølgning), maksimal statindosis (3,3 % ved indgang og 13,9 % ved opfølgning) og maksimal LLT (7,9 % ved indgang og 23,6 % ved opfølgning). Den hyppigst ordinerede statin ved indtræden (25,3 %) og opfølgning (30.5%) var atorvastatin. Ordinationen af rosuvastatin steg (fra 6,0 % ved inddragelsen til 20,3 % ved opfølgningen). Den mediane varighed af statinbehandling var 7,0 år (5,0 til 9,0 år). Alder ved menarche var 12,0 år (12,0 til 13,0 år) for piger, der blev behandlet med statiner, og 12,0 år (11,0 til 13,0 år) for piger, der ikke blev behandlet med statiner (P = 0,77). Der blev ikke observeret nogen stigning i hverken levertransaminaser eller kreatinphosphokinase. Fibrater og galdesyre-sekvestranter blev kun anvendt hos 15 patienter ved inklusion (7,0 %) og 3 patienter ved opfølgning (1,5 %). Ezetimibe monoterapi uden statin blev anvendt hos 18 patienter ved inklusion (8,3 %) og 24 patienter ved opfølgning (11,1 %). Med hensyn til overholdelse af behandlingen rapporterede 10 patienter (4,6 %), at de ikke tog medicin mindst 1 dag hver måned under opfølgningen. Ved multivariabel analyse var ingen variabel uafhængigt forbundet med statinbrug.
Lipidsænkende behandlinger og opnåelse af LDL-C-mål (kohorte)
| Ved indgangs-/følge-up- | At entry-/follow-up+ | At entry+/follow-up- | At entry+/follow-up+ | P | ||
|---|---|---|---|---|---|---|
| Patienter på statiner | 60 (27.6%) | 61 (28,1%) | 9 (4,1%) | 87 (40,1%) | .001 | |
| Patienter på maksimal statindosis | 186 (85.7%) | 24 (11,1%) | 1 (0,5%) | 6 (2,8%) | .001 | |
| Patienter på ezetimibe | 177 (81,6%) | 21 (9.7%) | 7 (3,2%) | 12 (5,5%) | .013 | |
| Patienter på maksimal kombinationsbehandling | 211 (97,2%) | 6 (2,8%) | 0 (0.0%) | 0 (0,0%) | N/A | |
| Patienter på maksimal LLT | 163 (75,1%) | 37 (17,1%) | 3 (1,4%) | 14 (6,5%) | .001 | |
| LDL-C | 111 (51,2 %) | 62 (28,6 %) | 16 (7.4%) | 28 (12,9%) | .001 | |
| LDL-C | 44 (20,3%) | 64 (29.5%) | 19 (8,8%) | 90 (41,5%) | .001 |
LDL-C, low-density lipoprotein-kolesterol; LLT, lipidsænkende behandling.
Værdierne er n (%). – = ikke til stede; + = til stede.
Se tekst for LLT-klassifikation.
Plasma LDL-C-koncentrationen faldt i gennemsnit med 12,5 % og nåede en medianværdi på 138,0 mg/dL ved opfølgningen. Målene for low-density lipoproteinkolesterol, som defineret i de seneste internationale anbefalinger om FH, blev nået hos 20,3 % ved indgangen og 41,5 % ved opfølgningen (tabel 3 og figur 2). Da et alternativt mål på LDL-C
mg/dL blev overvejet for patienter under 14 år, nåede 8 ud af 48 patienter (16,7 %) og 1 ud af 6 patienter (16,7 %) målet ved henholdsvis indskrivning og opfølgning. Den eneste variabel, der var uafhængigt forbundet med LDL-C-målopnåelse i den multivariable analyse, var statinbrug (odds ratio, 13,83; 95 % konfidensinterval, 2,98-64,15). Typen af sundhedsplejerske (specialist eller primær læge), alder, køn, lipoprotein (a)-niveau og type mutation var ikke forbundet med opnåelse af LDL-C-mål.
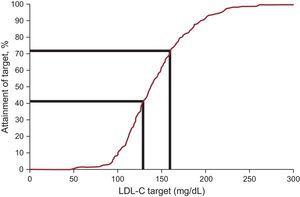
Behandlingsmål hos patienter med familiær hyperkolesterolæmi yngre end 18 år: Andel af patienter, der opnår LDL-C-målet. LDL-C, low-density lipoprotein cholesterol.
DISCUSSION
I denne undersøgelse rapporterer vi om karakteristika, LLT-anvendelse og opnåelse af LDL-C-mål i en longitudinel kohorte af molekylært definerede FH-patienter yngre end 18 år, der er indskrevet i SAFEHEART-registret. Dette unikke register over FH-patienter er baseret på data fra det virkelige liv i Spanien i både specialiserede og primære behandlingsmiljøer. Vores resultater viser, at et LDL-C-behandlingsmål
mg/dL kun blev nået af 20,3 % af patienterne ved inklusionen og i 41,5 % ved opfølgningen, med 68,2 % af patienterne på LLT. Statinbrug var den eneste faktor, der var uafhængigt forbundet med opnåelse af LDL-C-målet. Så vidt vi ved, har intet andet arbejde vist målopnåelse hos FH-patienter under 18 år, og denne undersøgelse er den første, der rapporterer det i en stor population.
For nylig analyserede et britisk register15 207 børn med FH og identificerede mutationer hos 64 % af børnene og fandt, at 48 % var på LLT; der blev opnået en 35 % reduktion i LDL-C. Forfatterne rapporterede dog ingen resultater vedrørende målopfyldelse. En anden rapport, som analyserede en lille prøve af forsøgspersoner (n = 89), viste en LDL-C-reduktion på 43 % ved langtidsopfølgningen.16 Denne større reduktion skyldes sandsynligvis en hyppigere anvendelse af kombinationsbehandling (56 %). Der blev ikke vist nogen målopfyldelsesresultater. I en anden retrospektiv artikel om 207 patienter i Nederlandene var kun 26 % af patienterne på LLT, og igen blev der ikke rapporteret nogen resultater vedrørende opnåelse af LDL-C-mål.17
Denne longitudinale undersøgelse viste, at LDL-C-niveauerne hos FH-patienter under 18 år kan ændre sig over tid som følge af LLT-modifikation og lægernes uddannelse. Andelen af patienter på statiner, den maksimale statindosis og den maksimale LLT steg signifikant i løbet af opfølgningen. Interessant nok tyder vores data på, at vores kohorte ikke er skævvredet, da der ikke var nogen statistisk signifikante forskelle mellem de patienter, der ikke blev fulgt op, og kohorten.
Førlig diagnosticering og behandling af FH er afgørende, især hos børn og unge, for at forebygge ASCVD-udvikling i voksenalderen. Screening for FH hos børn er værd at foretage og skal udføres før 8-årsalderen, fordi børn med hyperkolesterolæmi har en øget risiko for tidlig ASCVD. Desuden kan screening identificere dem, der har den højeste risiko, og fremskynde iværksættelse af LLT, som har vist sig at kunne vende den aterosklerotiske proces effektivt og reducere ASCVD-risikoen. Børn med FH har normalt ikke klinisk ASCVD. Ikke desto mindre understøtter eksistensen af fremtidig risiko brugen af LLT, idet statiner er hjørnestenen i FH-behandling.18
Sikkerheden og tolerabiliteten af LLT i pædiatrisk FH er altid kontroversiel, selv om de rapporteres at være lig dem hos voksne.5,19,20 For nylig rapporterede Ramaswami et al.15 ingen sikkerhedsproblemer, hvilket svarer til vores resultater. Ikke desto mindre anbefales streng overvågning, især hos de patienter, der modtager højere statindoser. Unge piger bør også rådes til at afbryde statinbehandling, når de overvejer at blive gravide. Ikke desto mindre, selv om der er behov for flere data om sikkerhedsspørgsmål for børn under langtidsbehandling med LLT, har nyere langtidsopfølgningsarbejde vist en fremragende sikkerhedsprofil.21 Dette resultat understøttes indirekte af vores data, fordi en høj andel af patienterne påbegyndte LLT under opfølgningen, og der var få frafald. Vores resultater viser klart en øget procentdel af patienter, der bruger statiner, en høj statindosis og maksimal LLT, med en lav andel af patienter, der opgiver medicinen. Disse data bekræfter sikkerheden, adhærensen og tolerabiliteten af statiner, selv når de anvendes i en høj dosis, hos FH-patienter yngre end 18 år.22 Desuden stemmer vores resultater overens med tidligere rapporter, der ikke viser nogen virkninger på seksuel modning.23 Alle disse resultater bekræfter på ny konceptet “jo yngre, jo bedre” med hensyn til den ideelle alder for at starte statiner hos disse unge FH-patienter.23
Vores resultater viser et stort antal FH-patienter yngre end 18 år og tyder i overensstemmelse med tidligere undersøgelser15,16 på, at voksne FH-patienter er villige til at inddrage deres nærmeste familiemedlemmer i screenings- og registeraktiviteter. Denne kendsgerning afspejler den alvor, hvormed disse patienter tager deres problem alvorligt, og den indvirkning, som deres lægers råd kan have på en ændring af deres livsstil. En sådan holdning hos voksne patienter udgør grundlaget for en sund livsstil hos deres pårørende.24
Og selv om det mest almindelige mål for FH-patienter under 18 år er et LDL-C-niveau under 130 mg/dL, kan en alternativ tilgang bestående af LDL-C mg/dL anvendes hos de patienter, der er yngre end 14 år, er ikke-rygere, har HDL-C ≥ 40 mg/dL, lipoprotein (a) mg/dL, LDL-C mg/dL og uden for tidlig hjerte-kar-sygdom hos forfædre eller bedsteforældre.6 Andre nyere retningslinjer anbefaler en reduktion af LDL-C på 50 % i forhold til niveauet før behandling, men for de børn, der er ≥ 10 år, især hvis der er yderligere kardiovaskulære risikofaktorer, herunder forhøjet lipoprotein (a), bør LDL-C-målet være mg/dL.11 Vores resultater viser også, hvor vanskeligt det er for disse patienter at nå lipidmålene.25 Desuden var LDL-C-målopfyldelsen ens, uanset om patienterne blev behandlet af specialister eller læger i primærsektoren. Det er således muligt at opnå et behandlingsniveau for pædiatriske patienter med FH i en primærplejeindstilling, som er sammenligneligt med det, der opnås ved specialistbehandling. Med henblik på dette mål er det vigtigt at fremhæve den støtte, som klinikere modtager via registre og dedikerede uddannelsesprogrammer. Registre kan optimere behandlingen af FH-patienter under 18 år ved at muliggøre integration af primær- og specialistbehandling og kan også støtte sundhedsmyndighederne i beslutningstagningen.8,26
Begrænsninger og styrker
I denne store opfølgningsundersøgelse af FH-patienter under 18 år var interventionen uændret i forhold til den, der blev leveret af patientens læge. Der mangler en pålidelig baseline lipidprofil i dette register, fordi nogle patienter allerede var i behandling, da de blev indskrevet. Desuden kan resultaterne være blevet ændret af flere forhold, såsom forskellige livsstile og en tilknytning til forskellige kardiovaskulære risikofaktorer, som kunne have ændret resultaterne.
KONKLUSIONER
SAFEHEART-registerdata viser, at en stor andel af FH-patienter yngre end 18 år har høje LDL-C-niveauer og ikke når de anbefalede LDL-C-mål. Vi fandt en stigning i LLT-intensiteten og et signifikant fald i LDL-C-niveauerne i løbet af opfølgningen. Statinbrug var den eneste uafhængige prædiktor for opnåelse af LDL-C-mål. Desuden blev der ikke påvist nogen sikkerhedsproblemer under opfølgningen. Disse resultater tyder på, at mange FH-patienter ikke er tilstrækkeligt kontrolleret, og at der stadig er plads til behandlingsforbedringer. Endvidere kan opfølgningen af denne FH-population bidrage til viden om sikkerheden ved livslang LLT og den optimale alder for behandlingsstart for at forebygge ASCVD-udvikling i voksenalderen.
FUNDING
Dette arbejde blev støttet af tilskud G03/181 fra Fundación Hipercolesterolemia Familiar, FIS PI12/01289 fra Instituto de Salud Carlos III og tilskud 08-2008 fra Centro Nacional de Investigación Cardiovascular.
Interessekonflikter
Ingen erklæret.
- –
Børn med ubehandlet heterozygot familiær hyperkolesterolæmi af familiær art har øget risiko for tidlig ASCVD efter 20 års alderen.
- –
Statiner og andre lipidsænkende behandlinger sænker effektivt LDL-C og er sikre hos børn og unge.
- –
Det vides kun lidt om karakteristika for FH-patienter under 18 år, de lipidsænkende behandlinger, der anvendes til disse patienter, og de lipidsænkende mål, der nås i det virkelige liv.
- –
Dette informationsunderskud er endnu større for opfølgningsdata.
Hvad tilføjer DENNE STUDIE?
- –
En stor andel af FH-patienter yngre end 18 år opnår ikke de anbefalede LDL-C-mål.
- –
Vi fandt en stigning i LLT-intensitet og et signifikant fald i LDL-C-niveauet i løbet af opfølgningen.
- –
Statinbrug var den eneste uafhængige prædiktor for opnåelse af LDL-C-mål, og der blev ikke påvist nogen sikkerhedsproblemer under opfølgningen.
- –
Disse resultater styrker konceptet “jo yngre, jo bedre”.