- Introduktion
- Materialer og metoder
- Deltagere
- Studieprocedurer, EEG-dataindsamling og analyse
- Resultater
- Deltagere
- Resting State EEG
- Fp1-kanalens effektspektrale tætheder (PSD’er) sammenligning
- Fp1 Channel Resting EEG Test/Retest Comparison
- Diskussion
- Author Contributions
- Funding
- Interessekonflikterklæring
- Anerkendelser
Introduktion
Neurodegenerative sygdomme udgør et enormt globalt behov, der ikke er opfyldt, og kræver udvikling af nye sygdomsændrende behandlinger. I betragtning af disse sygdommes snigende karakter og de høje omkostninger ved mange diagnostiske test er der et betydeligt behov for bredt tilgængelige, pålidelige og billige biomarkører til at spore udviklingen af neurodegenerative processer inden for tidsrammer, der er egnede til lægemiddeludvikling. I denne sammenhæng kan EEG have et bemærkelsesværdigt potentiale. Selv om EEG er følsomt over for kendte livsstilsfaktorer og medicinering, har det mange betydelige fordele. EEG afspejler synaptisk aktivitet, som er en fællesnævner for de funktionelle virkninger af neurodegenerative processer. EEG er en ikke-invasiv, bærbar, sikker og billig teknologi, som er bredt accepteret og kræver forholdsvis kort tid til registrering. Kvalitativ EEG anvendes rutinemæssigt i klinisk praksis til diagnosticering af epilepsi. For nylig er der blevet foreslået en integration af en kvantitativ EEG-biomarkør (qEEG) og klinikerens vurdering til vurdering af opmærksomhedsunderskud/hyperaktivitetsforstyrrelse (ADHD) og er blevet tildelt af FDA (Food and Drug Administration) klasse II-betegnelse til støtte for den kliniske vurdering af ADHD (Lenartowicz og Loo, 2014; Snyder et al., 2015). qEEG er på undersøgelsesstadiet til brug som endepunkt i neurodegenerative sygdomme i kliniske forsøg. Nylige fremskridt inden for dataanalyser, fortolkning og forbedret rumlig opløsning har imidlertid øget potentialet for EEG som en pålidelig, præcis biomarkør for neurodegenerativ sygdomsprogression. Mange rapporterede observationelle qEEG-analyser i hviletilstand understøtter dets potentielle værdi som en biomarkør til påvisning af neurale signaturer af neurodegeneration, der forekommer i Alzheimers sygdom (Babiloni et al., 2011; Moretti et al., 2011; Berka et al., 2014; Chen et al., 2015; Garn et al., 2015; Ruffini et al., 2016; Waninger et al., 2016), Parkinsons sygdom (Sarnthein og Jeanmonod, 2007; Babiloni et al., 2011; Soria-Frisch et al, 2014; Shani Waninger et al., 2015; Kroupi et al., 2017) og frontotemporal demens (Pijnenburg et al., 2008; Nishida et al., 2011; Caso et al., 2012; Goossens et al., 2016).
I årenes løb har EEG-hardwareteknologien også udviklet sig, og der er opstået flere trådløse multikanalsystemer, der leverer EEG og fysiologiske signaler af høj kvalitet i et enklere, mere praktisk og behageligt design end de traditionelle, besværlige systemer. Traditionelle EEG-systemer kræver lang tid til montering og anvendelse, hvilket typisk indebærer slid på patientens hovedbund. Påføringstiden og ubehaget gør disse traditionelle systemer vanskelige at anvende i befolkningsgrupper, der er ramt af demens, hvor det ofte er vanskeligt at samarbejde med langvarige kliniske procedurer. Flere af de trådløse systemer, der i øjeblikket findes på markedet, kan imidlertid anvendes på 20 minutter eller mindre uden ubehag under anvendelsen og med en behagelig pasform under optagelserne. Kombineret med fremskridt inden for signaldetektion og kvantitative analyseteknikker er trådløse systemer ideelle kandidater til relativt hurtig, tolerabel klinisk vurdering af potentielt udfordrende demenspopulationer, såsom adfærdsmæssig variant af frontotemporal demens, der er karakteriseret ved fremtrædende adfærds- og personlighedsændringer.
For nylig har der også været et voksende marked for bærbare forbrugerteknologier, der fører til systemer med begrænset kanal, der er tilgængelige til personlig brug, såsom meditation og afslapningstræning. Det er tænkeligt, at disse systemer, selv om de har en begrænset dækning, også kan anvendes i udvalgte kliniske undersøgelser. Anvendelsen af disse forbrugersystemer i kliniske forsøg er imidlertid ikke blevet udforsket i vid udstrækning, og disse systemers nøjagtighed og pålidelighed i forbindelse med gentagne målinger er ikke blevet veletableret. Endvidere er det ikke klart, om den begrænsede kanaloptagelse kan give tilstrækkelige data og anatomisk dækning til at vurdere de neurale signaturer hos patienter, der er ramt af neurodegenerative sygdomme.
Den aktuelle undersøgelse var designet til at give en indledende evaluering af potentialet af forbruger-EEG-systemer til kliniske forsøg ved at sammenligne brugervenlighed, nøjagtighed og pålidelighed af to medicinske trådløse multikanals EEG-systemer af medicinsk kvalitet, B-Alert X24 og Enobio 20, med to forbruger-systemer med begrænsede kanaler, Muse og Mindwave.
Materialer og metoder
Deltagere
Undersøgelsespopulationen omfattede fem raske deltagere, der opfyldte betingelserne for at deltage i undersøgelsen (tabel 1). Deltagerne blev udelukket, hvis de efter gennemgang af deres sygehistorie, sideløbende medicinering og livsstil (alkohol- og koffeinforbrug samt rygerstatus) ikke blev anset for at være sunde. Specifikt blev de udelukket fra undersøgelsen, hvis de havde en historie med epilepsi eller andre søvnmæssige, neurologiske eller psykiatriske lidelser eller tog medicin eller havde en livsstil, der vides at påvirke EEG-signalet, såsom rygning og et betydeligt alkohol- og koffeinforbrug.

Tabel 1. Undersøgelsespopulationens demografi og baselinekarakteristika.
Der blev indhentet skriftligt informeret samtykke fra alle undersøgelsesdeltagerne i overensstemmelse med retningslinjerne for eksperimentel undersøgelse med mennesker, som kræves af Chesapeake Institutional Review Board.
Studieprocedurer, EEG-dataindsamling og analyse
For at undgå potentiel EEG-signalvariabilitet forbundet med ernæringsindtagelse og cirkadiske variationer, fandt alle besøg sted om morgenen efter en standard morgenmad med lavt kulhydratindhold og højt proteinindhold (for at minimere postprandial døsighed) på Advanced Brain Monitoring (ABM) forskningslaboratoriernes undersøgelsessted. Desuden blev deltagerne bedt om at undgå alkoholholdige drikkevarer aftenen før undersøgelsesbesøget samt om at faste og undgå koffein om morgenen på besøgsdagen.
EEG-data blev indsamlet under to separate besøg med ~1 uges mellemrum fra to medicinske EEG-systemer med flere kanaler (20 kanaler), B-Alert (Advanced Brain Monitoring, ABM) og Enobio (Neuroelectrics) (figur 1, tabel 2) og to forbruger-systemer med begrænsede kanaler, Muse (Interaxon, 2 kanaler) og Mindwave (Neurosky, én kanal) (figur 1, tabel 2) i følgende rækkefølge: Muse, Mindwave, B-Alert, Enobio. B-Alert X24 EEG-systemet og Enobio er begge CE-medicinsk certificerede trådløse 20-kanals-systemer, der anvendes i den internationale standard 10-20 montage og optager EEG-signalet ved en samplingfrekvens på 256 Hz. Desuden er B-Alert blevet godkendt af FDA til brug som medicinsk udstyr.
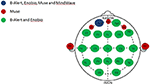
Figur 1. Anatomisk kanalfordeling af multi- og limited-channel EEG-systemer. Repræsentation af de fælles og unikke kanaler blandt de fire evaluerede EEG-systemer. Den fælles kanal for alle fire EEG-systemer, Fp1 (blå); kanaler, der er unikke for Muse-systemet (rød); kanaler, der deles mellem flerkanalsystemerne, B-Alert og Enobio (grøn).

Tabel 2. Sammenligning af EEG-systemer.
B-Alert bruger mastoiderne som referencekanal. Enobio kan anvendes med en mastoid-reference, øreklip eller ved hjælp af andre hovedbundssteder. Mindwave har også en reference på øreklipsen, og Muse har tre referencekanaler på panden. Alle systemer omfattede signalkvalitetskontrol, men i modsætning til de medicinske EEG-systemer har begge forbrugersystemer tørre elektroder og ingen impedanskontrol.
Disse teknologier blev udvalgt på grundlag af deres evne til at give slutbrugerne rå EEG-output via praktisk og ikke omkostningsforhindrende adgang.
Ten minutters EEG i hviletilstand blev optaget under åbne øjne (EO) med visuel fiksering på et kors-symbol præsenteret på en computerskærm (5 min) samt mens øjnene var lukkede (EC) i 5 min.
Da alle fire systemer kun deler FP1-kanalen (figur 1), blev EEG-mønstre (rå og dekontamineret), effektspektrale tætheder (PSD’er) og test/retest pålidelighedssammenligninger på tværs af de fire EEG-systemer, der blev evalueret i undersøgelsen, udført med fokus på Fp1-elektroden i både EO- og EC-betingelser.
EEG-dataene fra hvert system blev indlæst i MATLAB (Mathworks) ved hjælp af specialbyggede funktioner. De EEG-data, der blev optaget under pauser og instruktioner, blev kasseret før analysen. Effektspektral tæthed af EEG for hver 1 s epok blev beregnet ved hjælp af Welch’s modificerede periodogrammetode med et Hamming-vindue aftagende af 1 s længde. PSD’er blev beregnet på hvilende EEG i både åbne og lukkede perioder med åbne og lukkede øjne. For at tillade lige enheder (μV) blev der anvendt en korrektionsfaktor på 1,25 (Muse), 0,25 (MindWave) eller 1 000 (Enobio 20). Alle Fp1-kanalens PSD-data blev beregnet som gennemsnit for de fem forsøgspersoner for hvert besøg. Test-retest blev udført ved at beregne og plotte Vist1/Visit2.
Resultater
Deltagere
Deltagerne var alle sunde frivillige med en gennemsnitsalder på 27 år, de var alle højrehåndede og ikke-rygere og overvejende mænd (60%). Deres demografiske data og baselinekarakteristika er opsummeret i tabel 1.
Resting State EEG
EEG-data blev indsamlet med succes fra alle fire testede systemer. Som forventet var opsætningstiden som følge af de tørre elektroder og det begrænsede antal kanaler betydeligt kortere for forbruger-EEG-systemerne. Der blev imidlertid ikke observeret nogen forskel i forsøgspersonernes tolerance og accept på tværs af de fire systemer.
Mønstre af rå EEG-data under EO- (figur 2) og EC- (figur 3) forhold blev indsamlet og evalueret fra hvert system. Muse og Mindwave var mere tilbøjelige til artefakt på grund af øjenblink og muskelbevægelser i den frontale region ved øjenåbning (figur 2).
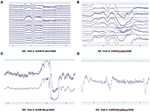
Figur 2. Uddrag af EO-rådata fra B-Alert (A) og Enobio (B) Muse (C) og MindWave (D) inden for den samme deltager under samme besøg.
Figur 3. Uddrag af EC-råddata fra B-Alert (A) og Enobio (B) Muse (C) og MindWave (D) inden for den samme deltager under samme besøg.
Fp1-kanalens effektspektrale tætheder (PSD’er) sammenligning
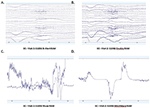
Gennemsnitlige PSD’er i Fp1-kanalen, der er fælles for alle fire EEG-systemer for besøg 1 og besøg 2, blev beregnet og plottet for både EO- (figur 4A,B) og EC- (figur 4C,D) betingelser. I EO-tilstanden var B-alert- og Enobio-spektre omtrent lige store, mens Mindwave var en smule forøget, men fulgte en lignende kurve. Der blev observeret en bredbåndsstigning i effekt for PSD’er, der blev erhvervet med Muse-systemet. På samme måde var B-alert, Enobio og Mindwave PSD’erne under EC-betingelsen (figur 4C,D) ens, men der blev observeret en øget bredbåndseffekt for Muse-spektre, som også syntes at have større variation end de andre systemer. Toppe ved 8-12 Hz (alfabåndet) var synlige i de spektrer, der blev erhvervet med B-Alert-, Enobio- og Mindwave-systemerne ved hvert besøg. Mens der var en tydelig alfa-top for Muse-effektspektrene ved besøg 2, blev der ikke observeret nogen top i spektrene fra besøg 1.
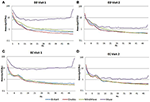
Figur 4. Fp1 Power Spectral Densities (PSD’er) fra alle fire EEG-systemer i EO-tilstanden ved Visit 1 (A) og Visit 2 (B) og EC-tilstanden ved Visit 1 (C) og Visit 2 (D).
Fp1 Channel Resting EEG Test/Retest Comparison
I EC-tilstanden var effektspektralforholdet mellem 0,975 og 1,025 for B-Alert, Enobio og Mindwave (Figur 5A). Muse-systemets PSD-forhold havde større variation end de tre andre systemer med forhold mellem 1,125 og 1,225. I EO-betingelsen syntes der at være lidt større variation for Enobio i de langsomme bølger Delta (1-3 Hz), Theta (3-7 Hz) og langsom alfa (8-10) og for B-Alert og Mindwave i de hurtigere bølger Beta (13-30 Hz) og Gamma (25-40 Hz). Forholdet var dog stadig mellem 0,975 og 1,05. I lighed med EC-betingelsen havde test/retest for Muse større variation med forholdstal på op til 1,2 (figur 5B).
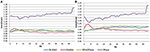
Figur 5. Test-retest-forhold for EC (A) og EO (B) tilstand.
Diskussion
Denne undersøgelse sammenlignede kvantitative EEG-signaler og test-retest-pålidelighed af medicinske og forbruger-EEG-systemer med henblik på at evaluere deres potentielle anvendelse i klinisk forskning og kliniske forsøg. Nyligt populære forbruger-EEG-systemer blev evalueret på grund af deres lave omkostninger, brede tilgængelighed og potentiale til hjemmebaserede undersøgelser i udfordrende befolkningsgrupper. Blandt de populære anvendelser af forbruger-EEG-systemer er meditations- og afslapningstræning samt håndtering af angst og smerte. I nyere undersøgelser er deres anvendelighed ud over spil blevet undersøgt: NeuroSky blev vist at være i stand til at registrere indtræden af fase 1-søvn (Van Hal et al., 2014), og der har også været interesse for at vurdere forbruger-EEG inden for hjernecomputerinterfaces (Bialas og Milanowski, 2014; Kim et al., 2015; Taherian et al., 2017). Anvendelsen af enklere EEG-systemer (f.eks. 6-kanaler) er også ved at blive undersøgt i forbindelse med nødsituationer (Jakab et al., 2014). En tidligere evaluering, selv om den anvendte et mere komplekst headset, viste, at kommercielt tilgængelige forbruger-EEG-systemer med flere ledninger, såsom Emotiv EPOC 16-elektrodehætten Emotiv EPOC, også kan have værdi til evaluering af kliniske forhold (Schiff et al., 2016).
Denne undersøgelse gav bevis for, at EEG-data af ret god kvalitet kan indsamles med succes fra forbruger-EEG’er. Der var imidlertid forskelle i effektforøgelsen, test-gennemgang og formen af alfa-toppen observeret ved 8-13 Hz. Mindwave viste generelt lignende Fp1-effektspektrer som de medicinske systemer med en lille bredbåndsforøgelse i forhold til B-Alert og Enobio. Muse viste en bredbåndsstigning i effektspektret, hvilket kan afspejle artefakt i de data, der er erhvervet af en tør elektrode.
Consumer EEG-systemer viste en betydeligt mere bekvem og hurtigere opsætning,hvilket er optimalt for deres tiltænkte anvendelse i underholdnings- og selvhjælpsapplikationer. Men deres datakvalitet var generelt negativt påvirket af artefaktfølsomhed forbundet med den tørre elektrode. Som forventet blev datakvaliteten især forringet under EO. Den manglende evne til impedansprøvning og anvendelsen i frontalområdet, som er særligt udsat for øjenblink og muskelbevægelser i forbindelse med øjenåbning, bidrog sandsynligvis også til denne relative artefakt. Desuden er den vurdering, der foretages af forbruger-EEG-systemer, i sagens natur begrænset og begrænset til det eneste anatomiske hjerneområde, der er dækket af de få kanaler, hvilket udelukker evalueringer af flere netværk.
Tørre elektroder kan også være mere tilbøjelige til at medføre ubehag over tid og udgøre en større risiko for fejlplacering på panden, hvilket fører til unøjagtig signaloptagelse og test/retest. Sammenlignet med udstyr af medicinsk kvalitet var test/retest-pålideligheden lavere i forbruger-EEG-systemer. Pålideligheden blev målt med en test/retest-opsamling for alle systemer (figur 5). Mens B-Alert, Enobio og Mindwave klarede sig rimeligt godt, havde Muse en relativt lav pålidelighed. Endvidere blev der påvist et klart alfa-top for Muse ved besøg 2 (figur 4), mens fraværet af et alfa-top ved besøg 1 tyder på manglende konsistens, som kan skyldes artefakt. Konsistente pålidelige målinger af hjerneaktivitet er afgørende i kliniske forsøg, når man overvåger sygdomsudviklingen og evaluerer effektiviteten af et eksperimentelt terapeutisk middel. Mens forbrugersystemerne kan være nyttige til en hurtig vurdering, når tiden er begrænset, kan disse begrænsninger ved forbruger-EEG hindre deres anvendelse i forsknings- og kliniske forsøgssammenhænge, og et system af medicinsk kvalitet med høj test-retest pålidelighed anbefales til brug som et farmakodynamisk endepunkt i kliniske vurderinger.
Sammenligningen af medicinske og forbruger-EEG-systemer under eksperimentelle forhold fremhævede differentiering i ydeevne og især specifikke begrænsninger i brugen, der kan hindre anvendelsen af forbrugersystemer i forsknings- og kliniske forsøgssammenhænge. På den anden side er de medicinske flerledersystemer mindre ideelle til underholdningsformål, der kræver hurtig opsætning og databehandling fra et minimalt antal elektroder. Den største begrænsning i denne undersøgelse ligger i den lille undersøgelsespopulation og den manglende randomisering af rækkefølgen af de systemer, der blev anvendt til opsamling. Data blev opsamlet i samme rækkefølge af systemer for at undgå virkningerne af opsamlingstidspunktet, som kan påvirke EEG på grund af cirkadiske rytmer. EEG-effektmålinger har imidlertid vist sig at være meget pålidelige og gentagelige for enkeltpersoner, når der anvendes standard-EEG-systemer. Derfor blev den valgte stikprøvestørrelse anset for at være informativ.
Sammenfattende kan EEG-data indsamles med succes fra alle fire testede systemer, herunder forbruger-EEG-systemer, med varierende begrænsninger med hensyn til anvendelighed, datakvalitet og pålidelighed, der styrer deres optimale anvendelse, herunder i kliniske forsøgssammenhænge. Modtagelighed for artefakt og variabilitet i test/retest pålidelighed forbundet med nuværende forbruger EEG-systemer foreslår brugen af medicinsk kvalitet EEG-system til robuste kliniske tværsnits- og langsgående EEG-dataindsamlinger.
Author Contributions
ER og AV: deltog i udformningen og designet af projektet, analysen og fortolkningen af data og manuskriptforberedelse. SW, CB og GR: deltog i udformningen og designet af projektet, dets gennemførelse, analysen og fortolkningen af data og udarbejdelsen af manuskriptet. Alle forfattere har været involveret i udarbejdelse, skrivning og revision af manuskriptet, og de har alle læst og godkendt den endelige version af manuskriptet.
Funding
Denne undersøgelse blev støttet af Biogen.
Interessekonflikterklæring
ER og AV: Biogen-ansat. SW og CB: Ansat hos Advanced Brain Monitoring, Inc. GR: Neuroelectrics medarbejder.
Anerkendelser
Vi vil gerne takke deltagerne i undersøgelsen for deres tid og bidrag til denne undersøgelse. Biogen-teamet deltog i undersøgelsens design, analyse og fortolkning af data, i skrivningen af rapporten og i beslutningen om at indsende artiklen til offentliggørelse.
Babiloni, C., De Pandis, M. F., Vecchio, F., Buffo, P., Sorpresi, F., Frisoni, G. B., et al. (2011). Cortical sources of resting state electroencephalographic rhythms in Parkinson’s disease related dementia and Alzheimer’s disease. Clin. Neurophysiol. 122, 2355-2364. doi: 10.1016/j.clinph.2011.03.029
PubMed Abstract | CrossRef Full Text | Google Scholar
Berka, C., Verma, A., Korszen, S., og Johnson, R. (2014). “Development of EEG biomarkers for Alzheimer’s disease,” in GTC Biomarkers Summit (San Diego, CA).
Bialas, P., and Milanowski, P. (2014). En højfrekvent steady-state visuelt fremkaldt potentiale baseret hjernecomputergrænseflade ved hjælp af et EEG-headset af forbrugerkvalitet. Conf. Proc. IEEE Eng. Med. Biol. Soc. 2014, 5442-5445. doi: 10.1109/EMBC.2014.6944857
PubMed Abstract | CrossRef Full Text | Google Scholar
Caso, F., Cursi, M., Magnani, G., Fanelli, G., Falautano, M., Comi, G., et al. (2012). Kvantitativ EEG og LORETA: værdifulde værktøjer til at skelne FTD fra AD? Neurobiol. Aging 33, 2343-2356. doi: 10.1016/j.neurobiolaging.2011.12.011
PubMed Abstract | CrossRef Full Text | Google Scholar
Chen, C. C., Hsu, C. Y., Chiu, H. W., Hu, C. J., and ChiehLee, T. (2015). Frekvenskraft og kohærens af elektroencefalografi er korreleret med sværhedsgraden af Alzheimers sygdom: en multicenteranalyse i Taiwan. J. Formos Med. Assoc. 114, 729-735. doi: 10.1016/j.jfma.2013.07.008
PubMed Abstract | CrossRef Full Text | Google Scholar
Garn, H., Waser, M., Deistler, M., Benke, T., Dal-Bianco, P., Ransmayr, G., et al. (2015). Kvantitative EEG-markører relaterer til Alzheimers sygdomssværhedsgrad i det prospektive demensregister Østrig (PRODEM). Clin. Neurophysiol. 126, 505-513. doi: 10.1016/j.clinph.2014.07.005
PubMed Abstract | CrossRef Full Text | Google Scholar
Goossens, J., Laton, J., Van Schependom, J., Gielen, J., Struyfs, H., Van Mossevelde, S., et al. (2016). EEG dominerende frekvenspeak differentierer mellem Alzheimers sygdom og frontotemporal lobar degeneration. J. Alzheimers Dis. 55, 53-58. doi: 10.3233/JAD-160188
PubMed Abstract | CrossRef Full Text | Google Scholar
Jakab, A., Kulkas, A., Salpavaara, T., Kauppinen, P., Verho, J., Heikkilä, H., et al. (2014). Nyt trådløst elektroencefalografisystem med en minimal forberedelsestid til brug i nødsituationer og præhospital pleje. Biomed. Eng. Online 13:60. doi: 10.1186/1475-925X-13-60
CrossRef Full Text | Google Scholar
Kim, M., Kim, B. H., og Jo, S. (2015). Kvantitativ evaluering af en billig, ikke-invasiv hybridgrænseflade baseret på EEG og øjenbevægelse. IEEE Trans. Neural. Syst. Rehabil. Eng. 23, 159-168. doi: 10.1109/TNSRE.2014.2365834
PubMed Abstract | CrossRef Full Text | Google Scholar
Kroupi, E., Castellano, M., Ibanez, D., Montplaisir, J., Gagnon, J. F., Postuma, R., et al. (2017). “Deep networks using auto-encoders for PD prodromal analysis,” in Proceedings of 1st HBP Student Conference (Vienna).
Lenartowicz, A., and Loo, S. K. (2014). Brug af EEG til at diagnosticere ADHD. Curr. Psychiatry Rep. 16:498. doi: 10.1007/s11920-014-0498-0
CrossRef Full Text | Google Scholar
Moretti, D. V., Frisoni, G. B., Binetti, G., og Zanetti, O. (2011). Anatomisk substrat og EEG-markører i hovedbunden er korreleret hos personer med kognitiv svækkelse og Alzheimers sygdom. Front Psychiatry 1:152. doi: 10.3389/fpsyt.2010.00152
PubMed Abstract | CrossRef Full Text | Google Scholar
Nishida, K., Yoshimura, M., Isotani, T., Yoshida, T., Kitaura, Y., Saito, A., et al. (2011). Forskelle i kvantitativ EEG mellem frontotemporal demens og Alzheimers sygdom som afsløret af LORET. Clin. Neurophysiol. A 122, 1718-1725. doi: 10.1016/j.clinph.2011.02.011
PubMed Abstract | CrossRef Full Text | Google Scholar
Pijnenburg, Y. A., Strijers, R. L., Made, Y. V., van der Flier, W. M., Scheltens, P., og Stam, C. J. (2008). Undersøgelse af hviletilstands EEG funktionel konnektivitet i frontotemporal lobar degeneration. Clin. Neurophysiol. 119, 1732-1738. doi: 10.1016/j.clinph.2008.02.024
PubMed Abstract | CrossRef Full Text | Google Scholar
Ruffini, G., David, I.-S., Castellano, M., og Soria-Frisch, A. (2016). “EEG-dreven RNN-klassifikation til prognose af neurodegeneration hos risikopatienter”, i Internet Corporation for Assigned Names and Numbers (ICANN) (Copenhargen).
Google Scholar
Sarnthein, J., og Jeanmonod, D. (2007). Høj thalamocortical theta-kohærens hos patienter med Parkinsons sygdom. J. Neurosci. 27, 124-131. doi: 10.1523/JNEUROSCI.2411-06.2007
PubMed Abstract | CrossRef Full Text | Google Scholar
Schiff, S., Casa, M., Di Caro, V., Aprile, D., Spinelli, G., De Rui, M., et al. (2016). Et billigt, brugervenligt elektroencefalografisk registreringssystem til vurdering af hepatisk encephalopati. Hepatology 63, 1651-1659. doi: 10.1002/hep.28477
PubMed Abstract | CrossRef Full Text | Google Scholar
Shani Waninger, S. K., Berka, C., Tan, V., og Johnson, R. (2015). “A novel portable neurocognitive biomarker assessment for Parkinson’s Disease,” in GTC Biomarkers Summit (San Diego, CA).
Snyder, S. M., Rugino, T. A., Hornig, M., and Stein, M. A. (2015). Integration af en EEG-biomarkør med en klinikers ADHD-evaluering. Brain Behav. 5:e00330. doi: 10.1002/brb3.330
PubMed Abstract | CrossRef Full Text | Google Scholar
Soria-Frisch, J. M., Ibanez, D., Dunne, S., Grau, C., Ruffini, G., Rodrigues-Brazete, J., et al. (2014). “Machine Learning for a Parkinsons prognosis and diagnosis system based on EEG,” in Proceedings International Pharmaco-EEG Society Meeting IPEG (Leipzig).
Taherian, S., Selitskiy, D., Pau, J., and Claire Davies, T. (2017). Er vi der endnu? Evaluering af hjerne-computergrænseflade af kommerciel kvalitet til kontrol af computerapplikationer af personer med cerebral parese. Disabil. Rehabil. Assist. Technol. 12, 165-174. doi: 10.3109/17483107.2015.1111943
PubMed Abstract | CrossRef Full Text | Google Scholar
Van Hal, B., Rhodes, S., Dunne, B., og Bossemeyer, R. (2014). Low-cost EEG-baseret søvndetektion. Conf. Proc. IEEE Eng. Med. Biol. Soc. 2014, 4571-4574. doi: 10.1109/EMBC.2014.6944641
PubMed Abstract | CrossRef Full Text | Google Scholar
Waninger, S., Stikic, M., Tatinada, R., Tatinada, R., and Verma, A. (2016). “Identifikation af neurofysiologiske biomarkører for MCI ved hjælp af hviletilstand, EEG,” i Alzheimer’s Association International Conference (Toronto, ON).
Google Scholar