Generický název: aciklovir
Dávkovací forma: krém
Medicínsky přezkoumáno Drugs.com. Naposledy aktualizováno 1. prosince 2020.
- Přehled
- Nežádoucí účinky
- Dávkování
- Odborné
- Interakce
- Další
- Indikace a použití přípravku Zovirax krém
- Dávkování a způsob podání přípravku Zovirax krém
- Dávkovací formy a síly
- 4. KONTRAINDIKACE
- Upozornění a opatření
- Všeobecně
- Kontaktní senzibilizace
- Nežádoucí účinky
- Zkušenosti z klinických studií
- Postmarketingové zkušenosti
- Lékové interakce
- POUŽITÍ U ZVLÁŠTNÍCH POPULACÍ
- Souhrn rizik
- Těhotenství
- Kojení
- Použití u dětí
- Geriatrické použití
- Předávkování
- Zovirax krém Popis
- Zovirax krém – klinická farmakologie
- Mechanismus účinku
- Farmakokinetika
- Mikrobiologie
- Neklinická toxikologie
- Karcinogeneze, mutageneze, poškození fertility
- Klinické studie
- Dospělé osoby
- Pediatrické subjekty
- Jak se přípravek podává/Skladování a zacházení
- Informace pro pacienta
- PATENTSKÉ INFORMACEZOVIRAX (zho-vahy-rex)(aciklovir)krém
- PŘÍBALOVÁ INFORMACE – 5g tuba Karton
- Více o přípravku Zovirax krém (aciklovir lokální)
- Zdroje pro spotřebitele
- Zdroje pro odborníky
- Jiné přípravky
- Související průvodce léčbou
Indikace a použití přípravku Zovirax krém
Zovirax. Krém je deoxynukleosidový analogový inhibitor DNA polymerázy viru herpes simplex (HSV) indikovaný k léčbě recidivujícího herpes labialis (oparu) u imunokompetentních dospělých a dospívajících od 12 let.
Dávkování a způsob podání přípravku Zovirax krém
Zovirax krém se aplikuje 5x denně po dobu 4 dnů. Léčba by měla být zahájena co nejdříve po výskytu příznaků nebo symptomů herpes labialis, tj. během prodromu nebo při objevení lézí.
U dospívajících ve věku 12 let a starších je dávkování stejné jako u dospělých.
Dávkovací formy a síly
Každý gram přípravku Zovirax krém obsahuje 50 mg (odpovídá 5 % hm.) acikloviru.
4. KONTRAINDIKACE
Zovirax krém je kontraindikován u pacientů se známou přecitlivělostí na aciklovir, valaciklovir nebo kteroukoli složku přípravku.
Upozornění a opatření
Všeobecně
Zovirax krém by měl být aplikován pouze na postižené vnější strany rtů a obličeje u pacientů s herpes labialis. Protože nejsou k dispozici žádné údaje, aplikace na lidské sliznice se nedoporučuje. Zovirax krém je určen pouze pro kožní použití a neměl by být používán do očí nebo do úst či nosu.
Kontaktní senzibilizace
Zovirax krém má potenciál pro podráždění a kontaktní senzibilizaci .
Účinek přípravku Zovirax krém nebyl u imunokompromitovaných pacientů stanoven.
Nežádoucí účinky
Zkušenosti z klinických studií
Protože klinické studie probíhají za velmi rozdílných podmínek, nelze výskyt nežádoucích účinků pozorovaných v klinických studiích léčiva přímo srovnávat s výskytem v klinických studiích jiného léčiva a nemusí odrážet výskyt pozorovaný v klinické praxi.
V pěti dvojitě zaslepených, placebem kontrolovaných studiích bylo 1124 pacientů léčeno krémem Zovirax a 1161 placebem (vehikulem). Lokální reakce v místě aplikace hlásilo 5 % pacientů dostávajících krém Zovirax a 4 % pacientů dostávajících placebo. Nejčastějšími nežádoucími reakcemi v místě lokální aplikace byly suchost rtů, deskvamace, suchost kůže, popraskané rty, pálení kůže, pruritus, šupinatost kůže a píchání na kůži; každá nežádoucí reakce se vyskytla u méně než 1 % pacientů dostávajících Zovirax krém a placebo. Tři pacienti užívající přípravek Zovirax krém a jeden pacient užívající placebo přerušili léčbu z důvodu nežádoucí příhody.
Další studie, do které bylo zařazeno 22 zdravých dospělých osob, byla provedena za účelem vyhodnocení kožní snášenlivosti přípravku Zovirax krém ve srovnání s vehikulem za použití metodiky testování náplastí s jednoduchým okluzem a polouzavřeným okluzem. Jak přípravek Zovirax krém, tak placebo vykazovaly vysoký a kumulativní potenciál podráždění. Další studie, do které bylo zařazeno 251 zdravých dospělých osob, byla provedena za účelem vyhodnocení potenciálu kontaktní senzibilizace přípravku Zovirax krém pomocí metodiky opakovaného inzultního náplasťového testování. Z 202 hodnocených subjektů byly možné kožní senzibilizační reakce pozorovány u stejných 4 (2 %) subjektů jak u přípravku Zovirax krém, tak u placeba, a tyto reakce na přípravek Zovirax krém i placebo byly potvrzeny u 3 subjektů při opakovaném kontaktu. Senzibilizující složka (složky) nebyla identifikována.
Bezpečnostní profil u pacientů ve věku 12 až 17 let byl podobný profilu pozorovanému u dospělých.
Postmarketingové zkušenosti
Kromě nežádoucích účinků hlášených z klinických studií byly během poregistračního používání acikloviru krém zjištěny následující příhody. Vzhledem k tomu, že byly hlášeny dobrovolně z populace neznámé velikosti, nelze provést odhady četnosti. Tyto události byly vybrány k zařazení na základě kombinace jejich závažnosti, četnosti hlášení nebo potenciální příčinné souvislosti s aciklovirovým krémem.
Všeobecně: Angioedém, anafylaxe.
Kůže: Kontaktní dermatitida, ekzém.
Lékové interakce
Klinické zkušenosti nezjistily žádné interakce vyplývající z lokálního nebo systémového podávání jiných léčivých přípravků současně s přípravkem Zovirax krém. Vzhledem k minimální systémové absorpci přípravku Zovirax krém jsou systémové lékové interakce nepravděpodobné.
POUŽITÍ U ZVLÁŠTNÍCH POPULACÍ
Souhrn rizik
Aciklovir se po lokální cestě podání minimálně systémově absorbuje a neočekává se, že by použití přípravku Zovirax krém u matky vedlo k expozici plodu . Zkušenosti s lokálním užíváním acikloviru u těhotných žen za několik desetiletí, založené na publikované literatuře včetně observačních studií, neidentifikovaly riziko závažných vrozených vad, potratů nebo nežádoucích výsledků u matky nebo plodu spojené s užíváním léku. Byly provedeny reprodukční studie na zvířatech se systémovou expozicí acikloviru. Další podrobnosti naleznete v informacích o předepisování acikloviru.
Odhadované základní riziko závažných vrozených vad a potratů pro uvedenou populaci není známo. Všechna těhotenství mají pozadí rizika vrozené vady, ztráty nebo jiných nežádoucích výsledků. V obecné populaci USA je odhadované riziko pozadí závažných vrozených vad a potratu u klinicky uznaných těhotenství 2 až 4 %, resp. 15 až 20 %.
Těhotenství
Souhrn rizik
Aciklovir se po lokální cestě podání systémově vstřebává minimálně a neočekává se, že by použití přípravku Zovirax krém u matky vedlo k expozici plodu . Zkušenosti s lokálním užíváním acikloviru u těhotných žen za několik desetiletí, založené na publikované literatuře včetně observačních studií, neidentifikovaly riziko závažných vrozených vad, potratů nebo nežádoucích výsledků u matky nebo plodu spojené s užíváním léku. Byly provedeny reprodukční studie na zvířatech se systémovou expozicí acikloviru. Další podrobnosti naleznete v informacích o předepisování acikloviru.
Odhadované základní riziko závažných vrozených vad a potratů pro uvedenou populaci není známo. Všechna těhotenství mají pozadí rizika vrozené vady, ztráty nebo jiných nežádoucích výsledků. V obecné populaci USA je odhadované riziko pozadí závažných vrozených vad a potratu u klinicky uznaných těhotenství 2 až 4 %, resp. 15 až 20 %.
Kojení
Souhrn rizik
Aciklovir se po lokální cestě podání systémově vstřebává minimálně a neočekává se, že by kojení vedlo k expozici dítěte přípravku Zovirax krém . Nejsou k dispozici žádné údaje o účincích přípravku ZOVIRAX na kojené dítě nebo na tvorbu mléka. Vývojový a zdravotní přínos kojení by měl být zvažován spolu s klinickou potřebou matky podávat přípravek Zovirax krém a případnými nežádoucími účinky přípravku Zovirax krém nebo základního onemocnění matky na kojené dítě.
Použití u dětí
Otevřená, nekontrolovaná studie s přípravkem Zovirax krém byla provedena u 113 pacientů ve věku 12 až 17 let s recidivujícím herpes labialis. V této studii byla léčba aplikována podle stejného dávkovacího schématu jako u dospělých a subjekty byly sledovány z hlediska nežádoucích účinků. Bezpečnostní profil byl podobný profilu pozorovanému u dospělých. Bezpečnost a účinnost u pediatrických pacientů mladších 12 let nebyla stanovena.
Geriatrické použití
Klinické studie acikloviru v krému nezahrnovaly dostatečný počet subjektů ve věku 65 let a více, aby bylo možné určit, zda reagují jinak než mladší subjekty. Další uváděné klinické zkušenosti nezjistily rozdíly v reakcích mezi staršími a mladšími pacienty. Systémová absorpce acikloviru po lokálním podání je minimální .
Předávkování
Předávkování lokální aplikací přípravku Zovirax krém je nepravděpodobné vzhledem k minimální systémové expozici . Nejsou k dispozici žádné informace o předávkování.
Zovirax krém Popis
ZOVIRAX je obchodní název pro aciklovir, syntetický deoxynukleosidový analog účinný proti herpetickým virům. Zovirax krém 5% je přípravek k lokálnímu podání.
Chemický název acikloviru je 2-amino-1,9-dihydro-9–6H-purin-6-on; má následující strukturní vzorec:
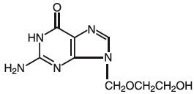
Aciklovir je bílý, krystalický prášek s molekulovým vzorcem C8H11N5O3 a molekulovou hmotností 225. Zovirax krém je určen k lokálnímu podání. Maximální rozpustnost ve vodě při 37 °C je 2,5 mg/ml. Hodnoty pKa acikloviru jsou 2,27 a 9,25.
Každý gram krému Zovirax obsahuje 50 mg (odpovídá 5 % hm.) acikloviru a následující neúčinné látky: cetostearylalkohol, minerální olej, poloxamer 407, propylenglykol, natrium-lauryl-sulfát, vodu a bílou vazelínu.
Zovirax krém – klinická farmakologie
Mechanismus účinku
Aciklovir je antivirové léčivo účinné proti α-herpesvirům .
Farmakokinetika
U dospělých dobrovolníků byla provedena klinická farmakologická studie s přípravkem Zovirax krém za účelem vyhodnocení perkutánní absorpce acikloviru. V této studii, které se zúčastnilo 6 dobrovolníků mužského pohlaví, byl krém aplikován na plochu 710 cm2 na zádech dobrovolníků 5krát denně v intervalu 2 hodin po dobu celkem 4 dnů. Denně byla měřena hmotnost naneseného krému a vylučování acikloviru močí. Plazmatická koncentrace acikloviru byla stanovena 1 hodinu po poslední aplikaci. Průměrné denní vylučování acikloviru močí bylo přibližně 0,04 % denní aplikované dávky. Plazmatické koncentrace acikloviru byly u 5 subjektů pod mezí detekce (0,01 μM) a u 1 subjektu sotva detekovatelné (0,014 μM). Systémová absorpce acikloviru z krému Zovirax je u dospělých minimální.
Systémová absorpce acikloviru po lokální aplikaci krému nebyla u pacientů <18 let hodnocena.
Mikrobiologie
Mechanismus účinku: Aciklovir je syntetický purinový deoxynukleosidový analog s inhibiční aktivitou na buněčných kulturách a in vivo proti DNA polymeráze HSV typu 1 (HSV-1) a 2 (HSV-2). Inhibuje replikaci HSV-1 a HSV-2 v buněčných kulturách a in vivo.
Inhibiční aktivita acikloviru je selektivní díky jeho afinitě k enzymu thymidinkináze (TK) kódovanému HSV. Tento virový enzym přeměňuje aciklovir na aciklovirmonofosfát, analog deoxynukleotidu. Monofosfát je dále přeměněn na difosfát buněčnou guanylátkinázou a na trifosfát řadou buněčných enzymů. V biochemických testech acyklovir trifosfát inhibuje replikaci α-herpes virové DNA. Této inhibice se dosahuje třemi způsoby: 1) kompetitivní inhibicí virové DNA polymerázy, 2) inkorporací do rostoucího řetězce virové DNA a jeho ukončením a 3) inaktivací virové DNA polymerázy.
Antivirová aktivita
Kvantitativní vztah mezi citlivostí herpetických virů na antivirotika v buněčných kulturách a klinickou odpovědí na léčbu nebyl u lidí stanoven a testování citlivosti virů nebylo standardizováno. Výsledky testování citlivosti, vyjádřené jako koncentrace léčiva potřebná k inhibici růstu viru v buněčné kultuře o 50 % (hodnota EC50), se značně liší v závislosti na řadě faktorů. Při použití testů redukce plaku na buňkách Vero se hodnoty EC50 acikloviru proti izolátům viru herpes simplex pohybují v rozmezí od 0,09 do 59,9 μM (0,02 až 13,5 μg/ml) pro HSV-1 a od 0.04 až 44,0 μM (0,01 až 9,9 μg/ml) pro HSV-2.
Rezistence
V buněčné kultuře
V buněčné kultuře byly izolovány kmeny HSV-1 a HSV-2 rezistentní vůči akloviru. HSV rezistentní k acikloviru byl výsledkem mutací v genech virové tymidinkinázy (TK; pUL23) a DNA polymerázy (POL; pUL30). Často byly izolovány frameshifty, které vedou k předčasnému zkrácení produktu HSV TK s následnou sníženou citlivostí k acikloviru. Mutace v genu pro virovou TK mohou vést k úplné ztrátě aktivity TK (TK negativní), snížené úrovni aktivity TK (TK parciální) nebo změně schopnosti virové TK fosforylovat léčivo bez ekvivalentní ztráty schopnosti fosforylovat thymidin (TK změněná). V buněčných kulturách byly pozorovány následující substituce související s rezistencí v TK HSV-1 a HSV-2 (tabulka 1).
|
HSV-1 |
TK |
P5A, H7Q, L50V, G56V, G59A, G61A, K62N, T63A, E83K, P84S, D116N, P131S, R163H, A167V, P173L, Q185R, R216S, R220H, T245M, R281stop, T287M, M322K |
|
HSV-2 |
TK |
L69P, C172R, T288M |
|
HSV-1 |
POL |
D368A, Y557S, E597D, V621S, L702H, N815S, V817M, G841C |
|
HSV-2 |
POL |
U pacientů infikovaných HSV
Klinický HSV-1 a HSV-.2 získané od pacientů, u nichž selhala léčba α-herpesvirové infekce, byly hodnoceny na genotypové změny v genech TK a POL a na fenotypovou rezistenci k acikloviru (tabulka 2). Byly identifikovány izoláty HSV s mutacemi typu frameshift a substitucemi souvisejícími s rezistencí v TK a POL. Výčet substitucí v HSV TK a POL vedoucích ke snížené citlivosti k acikloviru není úplný a u variant HSV izolovaných od pacientů, u nichž selhávají režimy obsahující aciklovir, budou pravděpodobně identifikovány další změny. Možnost virové rezistence k acikloviru by měla být zvážena u pacientů, kteří nereagují na léčbu nebo u nichž dochází k opakovanému vylučování viru během léčby.
|
HSV-1 |
TK |
G6C, R32H, R41H, R51W, Y53C/D/H, Y53stop, D55N, G56D/S, P57H, H58/N/R/Y, G59R, G61A, K62N, T63I, Q67stop, S74stop, Y80N, E83K, P84L, Y87H, W88R, R89Q/W, E95stop, T103P, Q104H, Q104stop, H105P, D116N, M121L/R, S123R, Q125H, M128L, G129D, I143V, A156V, D162A/H/N, R163G/H, L170P, Y172C, P173L, A174P, A175V, R176Q/W, R176stop, L178R, S181N, V187M, A189V, V192A, G200C/D/S, T201P, V204G, A207P, L208F/H, R216C/H, R220C/H, R221H, R222C/H, L227F, T245M/P, L249P, Q250Stop, C251G, R256W, E257K, Q261R, T287M, L288Stop, L291P/R, L297S, L315S, L327R, C336Y, Q342Stop, T354P, L364P, A365T |
|
HSV-2 |
TK |
R34C, G39E, R51W, Y53N, G59P, G61W, S66P, A72S, D78N, P85S, A94V, N100H, I101S, Q105P, T131P, D137stop, F140L, L158P, S169P, R177W, S182N, M183I, V192M, G201D, R217H, R221C/H, Q222stop, R223H, Y239stop, R271V, P272S, D273R, T287M, C337Y |
|
HSV-1 |
POL |
K532T, Q570R, L583V, A605V, A657T, D672N, V715G, A719T/V, S724N, F733C, E771Q, S775N, L778M, E798K, V813M, N815S, G841S, I890M, G901V, V958L H1228D |
|
HSV-2 |
POL |
E250Q, D307N, K533E, A606V, C625R, R628C, E678G, A724V, S725G, S729N, I731F, Q732R, M789K/T, V818A, N820S, Y823C, Q829R, T843A, M910T, D912N/V, A915V, F923L, T934A, R964H |
Not: Mohou existovat další substituce vedoucí k rezistenci k acikloviru.
Křížová rezistence
Křížová rezistence byla pozorována u izolátů HSV nesoucích frameshift mutace a substituce spojené s rezistencí, které propůjčují sníženou citlivost na penciklovir (PCV), famciklovir (FCV) a foskarnet (FOS) .
|
Zkřížená rezistence k PCV/FCV |
HSV-1 TK |
G6C, R32H, R51W, Y53C/H, H58N, G61A, S74Stop, E83K, P84L, T103P, Q104Stop, D116N, M121R, I143V, R163H, L170P, Y172C, A174P, R176Q/W, Q185R, A189V, G200D, L208H, R216C, R220H, R222C/H, T245M, Q250Stop, R256W, R281Stop, T287M, L315S, M322K, C336Y |
|
Křížově odolný vůči PCV/FCV |
HSV-1 POL |
A657T, D672N, V715G, A719V, S724N, E798K, N815S, G841S |
|
Křížově odolný vůči PCV/FCV |
HSV-2 TK |
G39E, R51W, Y53N, R177W, R221H, T288M |
|
Křížově rezistentní k PCV/FCV |
HSV-2 POL |
K533E, A606V, C625R, R628C, S729N, Q732R, M789K/T, V818A, N820S, F923L, T934A |
|
Křížově rezistentní k FOS |
HSV-1 POL |
D368A, A605V, D672N, L702H, V715G, A719T/V, S724N, L778M, E798K, V813M, N815S, V817M, G841C/S, I890M, |
|
Křížově odolný vůči FOS |
HSV-2 POL |
K533E, A606V, C625R, R628C, A724V, S725G, S729N, I731F, Q732R, M789K/T, V818A, Y823C, D912V, F923L, T934A, R964H |
Neklinická toxikologie
Karcinogeneze, mutageneze, poškození fertility
Systémová expozice po lokálním podání acikloviru je minimální. Studie dermální karcinogenity nebyly provedeny. Výsledky studií karcinogeneze, mutageneze a fertility nejsou zahrnuty v úplných preskripčních informacích pro přípravek Zovirax krém vzhledem k minimální expozici acikloviru, která je výsledkem dermální aplikace. Informace o těchto studiích jsou k dispozici v úplných preskripčních informacích pro přípravek ZOVIRAX tobolky, tablety a suspenze a ZOVIRAX na injekce.
Klinické studie
Dospělé osoby
Zovirax krém byl hodnocen ve dvou dvojitě zaslepených, randomizovaných, placebem (vehikulem) kontrolovaných studiích pro léčbu recidivujícího herpes labialis. Průměrný pacient měl v předchozích 12 měsících pět epizod herpes labialis. V první studii byl průměrný věk subjektů 37 let (rozmezí 18 až 81 let), 74 % tvořily ženy a 94 % běloši. Ve druhé studii byl medián věku subjektů 38 let (rozmezí 18 až 87 let), 73 % tvořily ženy a 94 % běloši. Subjekty byly poučeny, aby zahájily léčbu do 1 hodiny od zaznamenání příznaků nebo symptomů a pokračovaly v léčbě po dobu 4 dnů s aplikací studijního léku 5krát denně. V obou studiích byla průměrná doba trvání rekurentní epizody herpes labialis přibližně o půl dne kratší u subjektů léčených krémem Zovirax (n = 682) ve srovnání se subjekty léčenými placebem (n = 703), a to přibližně 4,5 dne oproti 5 dnům. Nebyl pozorován žádný významný rozdíl mezi subjekty, které dostávaly přípravek Zovirax krém nebo placebo, v prevenci progrese lézí oparu.
Pediatrické subjekty
Otevřená, nekontrolovaná studie s přípravkem Zovirax krém byla provedena u 113 pacientů ve věku 12 až 17 let s recidivujícím herpes labialis. V této studii byla léčba aplikována podle stejného dávkovacího schématu jako u dospělých a subjekty byly sledovány z hlediska nežádoucích účinků. Bezpečnostní profil byl podobný profilu pozorovanému u dospělých.
Jak se přípravek podává/Skladování a zacházení
Každý gram přípravku Zovirax krém obsahuje 50 mg (odpovídá 5 % hm.) acikloviru ve vodném krémovém základu. Zovirax krém se dodává takto:
NDC 0187-0994-45: 5 g tuby
Uchovávejte při teplotě do 25 °C; exkurze jsou povoleny při teplotě od 15 °C do 30 °C .
Informace pro pacienta
Poručte pacientovi, aby si přečetl označení schválené FDA (Informace pro pacienta).
Všeobecné informace
Pacienti by měli být informováni, že Zovirax krém je lokální krém na lékařský předpis k léčbě oparů (recidivující herpes labialis), které se vyskytují na obličeji a rtech. Zovirax krém není lékem na opary. Pacienti by měli být poučeni, že Zovirax krém je určen pouze ke kožnímu použití na herpes labialis rtů a okolí úst. Pacienti by měli být poučeni, že Zovirax krém se nesmí používat do očí, uvnitř úst nebo nosu a na genitálie. Pacienti by měli být poučeni, aby se během používání přípravku Zovirax krém vyhnuli aplikaci jiných lokálních přípravků na postižené místo.
Přípravek Zovirax krém nepoužívejte, pokud jste alergičtí na přípravek Zovirax krém nebo na kteroukoli složku přípravku Zovirax krém. Před použitím přípravku Zovirax krém informujte svého lékaře, pokud jste těhotná, plánujete otěhotnět nebo kojíte.
Návod k použití
Léčba by měla být zahájena při prvních známkách nebo příznacích recidivy. Poučte pacienty, aby si před aplikací umyli ruce a zajistili, že obličej a/nebo rty budou čisté a suché. Doporučte pacientům aplikovat Zovirax krém lokálně 5krát denně po dobu 4 dnů. Poučte pacienty, aby lokálně aplikovali takové množství krému Zovirax, které pokryje postiženou oblast včetně vnějšího okraje. Doporučte pacientům, aby se vyhnuli zbytečnému tření postižené oblasti, aby nedošlo ke zhoršení nebo přenosu infekce. Poučte pacienty, aby si po použití přípravku Zovirax krém umyli ruce vodou a mýdlem. Uchovávejte mimo dosah dětí.
Možné nežádoucí účinky
Mezi časté nežádoucí účinky související s kůží, které se vyskytly při aplikaci přípravku Zovirax krém, patří reakce v místě aplikace. Zovirax krém má potenciální možnost podráždění a kontaktní senzibilizace.
Distribuováno:
Laval, Quebec H7L 4A8, Kanada
Zovirax je registrovaná ochranná známka skupiny společností GlaxoSmithKline a společnost Bausch Health ji používá na základě licence.
© 2020 Bausch Health Companies Inc. nebo její pobočky
9462203
PATENTSKÉ INFORMACEZOVIRAX (zho-vahy-rex)(aciklovir)krém
Důležité informace: Zovirax krém je určen pouze k použití na opary na rtech a v okolí úst. Zovirax krém se nesmí používat v oblasti očí, úst, nosu ani na genitáliích.
Co je přípravek Zovirax krém?
– Zovirax krém je léčivý přípravek na lékařský předpis, který se používá k léčbě oparu (herpes labialis), který se opakuje u dospělých a dětí ve věku 12 let a starších a kteří mají normální imunitní systém. – Zovirax krém není lékem na opary.
Není známo, zda je přípravek Zovirax krém bezpečný a účinný u dětí mladších 12 let.
Nepoužívejte přípravek Zovirax krém, pokud jste alergický(á) na aciklovir, valaciklovir nebo na kteroukoli složku přípravku Zovirax krém. Úplný seznam složek přípravku Zovirax krém naleznete na konci této příbalové informace.
Co mám říci svému lékaři před použitím přípravku Zovirax krém?
Před použitím přípravku Zovirax krém informujte svého lékaře o všech svých zdravotních potížích, včetně případů, kdy:
– velmi snadno onemocníte (máte oslabený imunitní systém). – Jste těhotná nebo plánujete otěhotnět. Není známo, zda přípravek Zovirax krém poškodí Vaše nenarozené dítě. – kojíte nebo plánujete kojit. Není známo, zda Zovirax krém přechází do Vašeho mateřského mléka. Pokud používáte přípravek Zovirax krém, poraďte se se svým lékařem o nejlepším způsobu krmení Vašeho dítěte.
Informujte svého lékaře o všech lécích, které užíváte, včetně léků na předpis a volně prodejných léků, vitamínů a bylinných doplňků.
Jak mám používat přípravek Zovirax krém?
– Používejte přípravek Zovirax krém přesně tak, jak Vám řekl Váš lékař. – Zovirax krém použijte, jakmile se u Vás objeví první příznaky oparu, jako je svědění, zarudnutí, pálení nebo mravenčení, nebo jakmile se opar objeví. – Před použitím přípravku Zovirax krém a po něm si umyjte ruce vodou a mýdlem. – Postižené místo by mělo být před aplikací přípravku Zovirax krém čisté a suché. – Aplikujte Zovirax krém na postižené místo 5krát denně po dobu 4 dnů, včetně vnějšího okraje. – Během léčby přípravkem Zovirax Cream byste na postižené místo neměli nanášet jiné kožní přípravky. – Vyvarujte se zbytečného tření oparu, protože to může způsobit rozšíření oparu do dalších oblastí kolem úst nebo zhoršení oparu.
Jaké jsou možné nežádoucí účinky přípravku Zovirax krém?
Nejčastějšími nežádoucími účinky přípravku Zovirax krém jsou kožní reakce v místě léčby a mohou zahrnovat: suché nebo popraskané rty, olupování, odlupování nebo suchost kůže, pocit pálení nebo píchání a svědění.
To nejsou všechny možné nežádoucí účinky přípravku Zovirax krém. O nežádoucích účincích se poraďte se svým lékařem. Nežádoucí účinky můžete hlásit FDA na telefonním čísle 1-800-FDA-1088.
Jak mám přípravek Zovirax krém uchovávat?
– Přípravek Zovirax krém uchovávejte při pokojové teplotě od 20° do 25°C (68° až 77°F).
Udržujte přípravek Zovirax krém a všechny léky mimo dosah dětí.
Všeobecné informace o bezpečném a účinném používání přípravku Zovirax krém.
Léky jsou někdy předepisovány pro jiné účely, než jsou uvedeny v příbalové informaci pro pacienta. Nepoužívejte přípravek Zovirax krém na stav, pro který nebyl předepsán. Nedávejte přípravek Zovirax krém jiným lidem, i když mají stejné příznaky jako Vy. Mohl by jim ublížit. Informace o přípravku Zovirax krém, které jsou určeny pro zdravotnické pracovníky, si můžete vyžádat od svého lékárníka nebo zdravotnického pracovníka.
Jaké složky obsahuje přípravek Zovirax krém?
Léčivá látka: aciklovir
Neúčinné látky: cetostearylalkohol, minerální olej, poloxamer 407, propylenglykol, natrium-lauryl-sulfát, voda a bílá vazelína
Distributor: MUDr: Bausch Health US, LLC
Bridgewater, NJ 08807 USA
Vyrobeno: Bausch Health US, LLC
:
Laval, Quebec H7L 4A8, Kanada
Zovirax je registrovaná ochranná známka skupiny GlaxoSmithKline používaná na základě licence společnosti Bausch Health.
© 2020 Bausch Health Companies Inc. nebo jejích přidružených společností
Pro více informací volejte 1-800-321-4576.
Tato informace pro pacienty byla schválena Úřadem pro kontrolu potravin a léčiv v USA.
Revize: 12/2020
9462203
PŘÍBALOVÁ INFORMACE – 5g tuba Karton
ZOVIRAX®
(ACYCLOVIR) KRÉM 5%
NDC 0187-0994-45
Čistá hmotnost. 5 g
Každý gram obsahuje:
50 mg acikloviru, cetostearylalkohol, minerální olej, poloxamer 407, propylenglykol, natrium-lauryl-sulfát, vodu a bílou vazelínu.
POUŽÍVÁ SE POUZE NA STUDENÉ BOLESTI.
POUZE PRO KUTÁNNÍ POUŽITÍ.
Ortho Dermatologics
Pouze na lékařský předpis
| ZOVIRAX acyclovir krém |
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
Označovatel -. Bausch Health US, LLC (831922468)
| Zařízení | |||
| Název | Adresa | ID/FEI | Provoz |
| Bausch Health Companies Inc. | 245141858 | MANUFACTURE(0187-0994) | |
Více o přípravku Zovirax krém (aciklovir lokální)
- Nežádoucí účinky
- Během těhotenství nebo kojení
- Informace o dávkování
- Lékové interakce
- Cenové &Kupóny
- 39 recenzí
- Třída léků: lokální antivirotika
Zdroje pro spotřebitele
- Informace pro pacienty
Zdroje pro odborníky
- Předpisová informace
- Acyclovir mast (FDA)
Jiné přípravky
- Zovirax
- Zovirax mast
Související průvodce léčbou
- Herpes simplex
- Studené vředy
Zřeknutí se lékařské odpovědnosti
.