![]()
Voda má důležité účinky na všechny biologické systémy. To, co dělá vodu tak jedinečnou, jsou dvě velmi důležité vlastnosti.
Voda je polární molekula
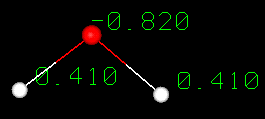 Molekula vody vzniká kovalentní vazbou dvou atomů vodíku s atomem kyslíku. V kovalentní vazbě jsou elektrony sdíleny mezi atomy. Ve vodě není toto sdílení rovnoměrné. Atom kyslíku přitahuje elektrony silněji než vodík, což dává vodě asymetrické rozložení náboje. Molekuly, které mají konce s částečným záporným a kladným nábojem, se nazývají polární molekuly. Právě tato polární vlastnost umožňuje vodě oddělovat polární molekuly rozpuštěných látek a vysvětluje, proč voda dokáže rozpouštět tolik látek.
Molekula vody vzniká kovalentní vazbou dvou atomů vodíku s atomem kyslíku. V kovalentní vazbě jsou elektrony sdíleny mezi atomy. Ve vodě není toto sdílení rovnoměrné. Atom kyslíku přitahuje elektrony silněji než vodík, což dává vodě asymetrické rozložení náboje. Molekuly, které mají konce s částečným záporným a kladným nábojem, se nazývají polární molekuly. Právě tato polární vlastnost umožňuje vodě oddělovat polární molekuly rozpuštěných látek a vysvětluje, proč voda dokáže rozpouštět tolik látek.
Voda je vysoce soudržná .
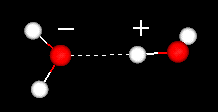 Kladné oblasti v jedné vodě budou přitahovat záporně nabité oblasti v jiných vodách. Čárky znázorňují vodíkovou vazbu. Ve vodíkové vazbě je atom vodíku sdílen dvěma dalšími atomy. Donorem je atom, ke kterému je vodík pevněji vázán. Akceptor (s částečným záporným nábojem) je atom, který přitahuje atom vodíku. Kliknutím sem nebo na obrázek vlevo zobrazíte film dvou molekul vody.
Kladné oblasti v jedné vodě budou přitahovat záporně nabité oblasti v jiných vodách. Čárky znázorňují vodíkovou vazbu. Ve vodíkové vazbě je atom vodíku sdílen dvěma dalšími atomy. Donorem je atom, ke kterému je vodík pevněji vázán. Akceptor (s částečným záporným nábojem) je atom, který přitahuje atom vodíku. Kliknutím sem nebo na obrázek vlevo zobrazíte film dvou molekul vody.
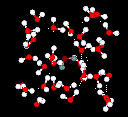 Vodíkové vazby jsou mnohem slabší než kovalentní vazby. Pokud však velký počet vodíkových vazeb působí ve shodě, vytvoří silný přispívající účinek. To je právě případ vody.
Vodíkové vazby jsou mnohem slabší než kovalentní vazby. Pokud však velký počet vodíkových vazeb působí ve shodě, vytvoří silný přispívající účinek. To je právě případ vody.
Viz: Vodíkové vazby ve vodě a ledu — Vodíkové vazby ve vodě a ledu pomocí Jsmol
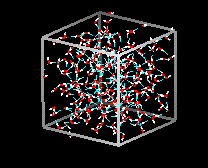
Tekutá voda má částečně uspořádanou strukturu, ve které se neustále vytvářejí a rozpadají vodíkové vazby.
Podívejte se na bleskový film molekul vody v akci.
Naopak led má pevnou mřížkovou strukturu.
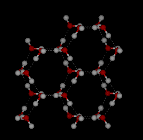
V kapalné vodě je každá molekula vodíkově vázána s přibližně 3,4 dalšími molekulami vody. V ledu je každá každá molekula vodíkově vázána na 4 další molekuly.
Porovnejte obě níže uvedené struktury. Všimněte si prázdných míst ve struktuře ledu.
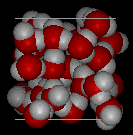
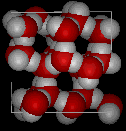
V ledu Ih tvoří každá molekula vody čtyři vodíkové vazby se vzdáleností O—O 2,76 angströmů k nejbližšímu sousednímu kyslíku. Úhly O-O-O jsou 109 stupňů, což je typické pro tetraedricky koordinovanou mřížkovou strukturu. Hustota ledu Ih je 0,931 gm/kubický cm. Pro srovnání, hustota vody je 1,00 gm/kubický cm.
Známe jedenáct různých forem krystalického ledu. Šestihranná forma známá jako led Ih je jediná, která se vyskytuje v přírodě. Mřížková struktura ledu 1h je znázorněna zde.
 Obrázek
Obrázek
.