Thomas A. Oetting, MS, MD
La conversión a la extracción extracapsular de cataratas (ECCE) suele llegar en un momento difícil. El cristalino está a punto de caer al sur, el vítreo ha prolapsado y el cirujano está estresado. Entender los pasos y el proceso de conversión a ECCE es esencial y el estudio antes de la crisis ayudará a calmar el estrés cuando se produzca este proceso inevitable. Cubriremos varias áreas: la identificación de los pacientes con riesgo de necesitar una conversión a ECCE, las indicaciones para la conversión, la conversión de tópica a sub-Tenon’s, la preparación de la herida, la expresión del material de la lente, el cierre de la herida, la colocación de la LIO, las cuestiones postoperatorias y una breve sección sobre la vitrectomía anterior.
Pacientes con riesgo de conversión a ECCE: Una de las partes más importantes del proceso preoperatorio de los pacientes con cataratas es evaluar los factores que aumentan la dificultad quirúrgica y que pueden llevar a la conversión a ECCE o complicar de otro modo el procedimiento.Es posible que desee añadir tiempo operativo a su programa o pedir equipo adicional. Es posible que desee cambiar a una herida limbal superior que facilite la conversión a una ECCE en lugar de una incisión corneal transparente temporal. Es posible que desee realizar un bloqueo retrobulbar en lugar de anestesia tópica, ya que el caso puede durar más tiempo o es más probable que se complique. En algunas situaciones, los factores de riesgo preoperatorios le hacen considerar la posibilidad de invitar a alguien más experimentado para hacer el caso.
Factores de dificultad (en orden decreciente de importancia)1
- Laxitud zonular (pseudoexfoliación-PXF, historia de traumatismo, síndrome de Marfan, etc.)
- Lente dura (lente roja o negra)
- Tamaño de la pupila (¿por qué es pequeña? PXF, diabetes s/p láser, sinequias posteriores centrales – CPS, floppy de tamsulosin/Flomax)
- No puede estar plana durante mucho tiempo (eg. Enfermedad pulmonar obstructiva crónica – EPOC, claustrofobia, temblor, obesidad severa)
- Grandes cejas que limitan el acceso superior
- Ángulo estrecho que limita el espacio de la cámara anterior (CA)
- Predisposición a la descompensación corneal: (por ejemplo Distrofia de Fuch o guttata corneal, PPMD, núcleo duro)
- Catara blanca/negra con reflejo rojo pobre que dificulta la capsulorrexis curvilínea continua (CCC)
- Cirugía pasada como trab existente o vitrectomía pars plana pasada (PPVx)
- Predisposición a la exposición: p. ej.: botox, traumatismo del párpado pasado, diabetes mellitus (DM)
- Anticoagulantes (e.g., warfarina/Coumadin, asparina)
- Paciente monocular
| Factor | Tiempo | Equipo/Anestesia |
|---|---|---|
| Laxitud zonular | Doble |
|
| Lente dura como una roca | Añadir 50% |
|
| Pupila pequeña | Añadir 50% |
|
| Flomax | Añadir 50% |
|
| Reflejo rojo pobre | Añadir 50% |
|
| Grandes cejas | Añadir 25% |
|
| Ángulo estrecho | Añadir 25% |
|
| Predisposición a la descompensación corneal | 0% |
|
| Sangrado de trabeculectomía existente | 0% |
|
| Vitrectomía previa (PPVx) | 0% |
|
| No se puede poner en posición horizontal | 0% |
|
| Anticoagulante usar | 0% |
|
| Paciente monocular | 0% |
|
| (modificado de Oetting, Cataract Surgery for Greenhorns, http://medrounds.org/cataract-surgery-greenhorns) | ||
Indicciones para la conversión: La conversión a ECCE está indicada cuando la facoemulsificación está fallando. A veces esto se debe a un cristalino muy duro que no se somete a los ultrasonidos o a un cristalino lo suficientemente duro como para que al cirujano le preocupe que la energía ultrasónica requerida dañe una córnea tentativa (por ejemplo, distrofia endotelial de Fuchs o distrofia polimorfa posterior). A veces se convierte a ECCE cuando una capsulorrexis errante se vuelve radial, especialmente con un cristalino duro, cuando al cirujano le preocupa que el riesgo de caída del cristalino sea demasiado grande con una facoemulsificación continuada. Un cirujano puede optar por convertir a la ECCE cuando la cápsula anterior es difícil de ver y la capsulorrexis debe completarse con la técnica del abrelatas (sin embargo, con el uso de la tinción con azul tripán esto está menos indicado). Más a menudo la conversión está indicada cuando el cristalino está suelto por zónulas débiles o por un desgarro de la cápsula posterior que hace que la facoemulsificación sea menos segura que la extensión de la herida y la eliminación del material del cristalino residual. Las indicaciones para la conversión a ECCE incluyen:
- Lente cristalino duro o endotelio inestable
- Desgarro radial en cápsula anterior con lente duro
- Mala visualización a pesar del colorante Trypan
- Desgarro capsular posterior
- Diálisis zonular
Conversión a anestesia sub-Tenon. A menudo convertimos los casos de córnea transparente tópica a ECCE. Mientras que el ECCE puede ser hecho bajo tópico es generalmente más cómodo y más seguro dar el anestésico adicional que es típicamente una inyección de sub tenon de bupivicaine y lidocaine. Esto proporcionará algo de acinesia y anestesia adicional. Suele haber una hemorragia subconjuntival y si la inyección se hace demasiado anterior puede causar quimiosis y abombamiento de la conjuntiva. Los pasos de la inyección subtenoniana se describen a continuación:1
- Preparar una jeringa de 3 cc con partes iguales de lidocaína al 2%/0.75% de bupivacaína
- Colocar la cánula lagrimal (o la cánula de Masket) con una curva suave que se aproxime a la del globo terráqueo
- Elegir un cuadrante para el bloqueo (mejor optar por un cuadrante lateral para evitar los músculos oblicuos)
- Hacer que el paciente mire hacia otro lado del cuadrante elegido para aumentar la exposición
- Utilizar unas pinzas .12 fórceps para retraer la conjuntiva
- Hacer una pequeña incisión hasta la esclerótica con las tijeras de Wescott
- Dirigir las tijeras de Wescott con la curva hacia abajo y diseccionar de forma contundente a través del cuadrante
- Diseccionar más allá del ecuador (similar al uso de las tijeras de tenotomía de Stevens en peds/retina)
- Utilizar .12 Fórceps para la contra tracción
- Colocar la cánula a través de la incisión y dirigirla más allá del ecuador antes de inyectar
- El anestésico local debe fluir fácilmente y causar poca quemosis — Si no, volver a disecar con las tijeras de Wescott para conseguir más posterior
- Utilizar 2-3 cc de la mezcla local
Forzar manteniendo abierto el colgajo posterior de la disección en el espacio subtenoniano. Cánula lagrimal con una curva suave que se aproxima a la curva del globo terráqueo, lista para introducir el anestésico local.
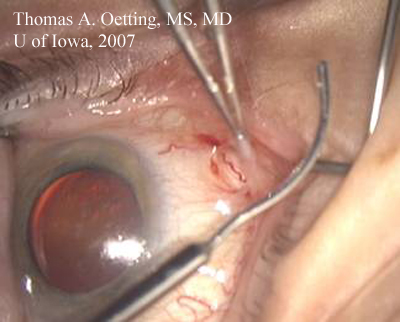
Conversión de la herida: El paso principal para convertir a la ECCE es ampliar la herida existente o cerrar y hacer otra. El ECCE requerirá una gran incisión de 9-12 mm que se cierra con sutura. La decisión de ampliar la herida existente o hacer una nueva depende de varios factores: la ubicación de la herida original, el tamaño de la ceja, los antecedentes quirúrgicos y la posible necesidad de una futura cirugía.
| Herida original | Ventajas de hacer una nueva herida para la AEPI | Ventajas de ampliar la herida existente para la AEPI |
|---|---|---|
| Temporal |
|
|
| Supero-temporal (ojo izquierdo) |
|
|
| Infero-temporal (ojo derecho) |
|
|
| Superior |
|
|
La realización de una nueva incisión durante la conversión es idéntica a la de un ECCE planificado. La incisión original se cierra con una sutura de nylon 10-O. El cirujano y el microscopio se giran, ya que el cirujano debe sentarse en posición superior. Los pasos para realizar una nueva incisión superior son:
- Peritomía conjuntival de unos 170 grados
- Utilizar cuchilla del 64 o de media luna para hacer el surco limbal con una longitud de cuerda de 11mm
- Cauterio bipolar para la hemostasia
- Utilizar queratomo para hacer la incisión inicial comenzando en el surco hacia el CA
- Extender la incisión inicial a toda la longitud del surco (con tijeras o cuchillo)
- Se colocan previamente suturas de seguridad (normalmente 7-0 Vicryl)
.
Extender una incisión existente puede ser complicado y la técnica es diferente para los túneles esclerales en comparación con las incisiones corneales claras. Sin embargo, en ambos casos la extensión original se lleva al limbo. En el caso de una incisión escleral original, la incisión se lleva a la parte anterior para unirse al limbo en cualquiera de sus extremos antes de extenderse a lo largo del limbo durante una longitud de cuerda de unos 11 mm. En el caso de una incisión corneal existente, la incisión corneal se lleva posteriormente hacia el limbo antes de extender la herida a lo largo del limbo para una longitud de cuerda de unos 11 mm. Cuando se utilizan ganchos de iris en configuración de diamante, la herida puede extenderse para preservar el gancho subincisional y la pupila grande.2
- Peritomía conjuntival de unos 170 grados
- Utilizar cuchilla 64 o de media luna a cada lado de la herida existente para hacer un surco limbal con una longitud de cuerda de 11mm
- Cauterización bipolar para la hemostasia
- Utilizar hoja de media luna para llevar la herida escleral existente por delante o la herida corneal existente por detrás para unir el limbo
- Extender la incisión inicial a toda la longitud del surco (con tijeras o cuchillo)
- Se colocan previamente suturas de seguridad (normalmente 7-0 Vicryl)
Retirar el cristalino: Hay que tener mucho más cuidado a la hora de retirar el núcleo durante la típica conversión a ECCE que viene acompañada de la pérdida de vítreo. Primero la cápsula anterior debe ser bastante grande para permitir que el núcleo exprese que puede requerir incisiones que relajan en algunos casos. Cuando las zónulas son débiles o la cápsula posterior está desgarrada, el cristalino no puede expresarse con líquido o presión externa, como suele hacerse en una ECCE planificada con cápsula/zónulas intactas. Después de retirar el vítreo (véase más adelante), el cristalino debe sacarse cuidadosamente de la cámara anterior con una presión mínima sobre el globo. Si la cápsula posterior y las zónulas están intactas, el cristalino puede extraerse como se ha descrito con un ECCE planificado.
Extrayendo el cristalino con el complejo capsular intacto:
- Mobilizar el cristalino (físicamente con cistótomo o con hidrodisección–tener cuidado)
- Extraer el cristalino con bucle de cristalino o con técnica de contrapresión
- Se cierra la herida con suturas de seguridad y una sutura central adicional de Vicryl
- Se retira el material cortical con un dispositivo I/A (automatizado o manual)
- Se mantiene el dispositivo viscoelástico oftálmico (OVD)
- Se coloca la lente en la cámara posterior
- Se cierra la herida con nylon 10-O y se retiran las suturas de Vicryl.
- Se retira el OVD
.técnica de contrapresión
Se retira la lente con el vítreo presente:
- Mobilizar el cristalino con la cánula de Viscoat (inclinar el cristalino de manera que el lado de la herida sea anterior)
- Deslizar el lazo del cristalino por debajo del cristalino, «levantar» el instrumento, retirar la lente
- Se cierra la herida con suturas de seguridad y una sutura central adicional de vicryl
- Vitrectomía anterior (ver más abajo)
- Se retira el material cortical utilizando la técnica seca o vitrector anterior
- Se coloca el dispositivo viscoelástico oftálmico (OVD)
- Se coloca la lente en el surco o en el canal anterior
- Se cierra la herida con suturas de nylon 10-O y se retiran las suturas de Vicryl
- Se retira el OVD
Colocación de la LIO: La selección de la LIO con conversión a ECCE depende del complejo capsular residual.3,4 La clave para el centrado de la LIO es conseguir que los dos hápticos estén en el mismo sitio: los dos en el saco o los dos en el surco.
- Cuando la cápsula posterior está intacta tras una conversión a ECCE, la apertura capsular anterior suele estar mal definida, lo que puede dificultar la colocación del saco. Si la cápsula anterior y por lo tanto la bolsa está bien definida, entonces coloque una LIO acrílica de una sola pieza sin doblarla directamente y suavemente en la bolsa utilizando pinzas Kelman.
- Cuando la cápsula posterior está intacta y la cápsula anterior está mal definida, entonces coloque una LIO de 3 piezas en el sulcus, como una LIO de silicona grande o la MA50 acrílica, colocándolas directamente y desplegadas en el sulcus con las pinzas Kelman. Asegúrese de que ambos hápticos están en el sulcus.
- Cuando la cápsula posterior está dañada, si queda suficiente cápsula anterior y posterior para soportar la LIO, defina el sulcus con viscoat y coloque la LIO directamente en el sulcus. Asegúrese de que ambos hápticos están en el surco. Si la LIO no parece estable, coloque suturas de McCannel para asegurar la LIO al iris o retírela y sustitúyala por una LIO AC (no olvide colocar una iridectomía posterior con el vitrector).
- Cuando la cápsula está severamente dañada y no puede soportar una LIO entonces coloque la LIO en la cámara anterior. Utilice las pinzas Kelman para colocar la LIO, luego asegure la cámara y utilice un gancho Sinskey para colocar la LIO AC en su posición final. (no olvide colocar una iridectomía periférica con el vitrector).
Cuestiones postoperatorias: Los cuidados postoperatorios de los pacientes tras la conversión de faco a ECCE son un poco más complicados y se centran en la prevención del edema macular cistoide (EMC) y la limitación del astigmatismo inducido. A menudo, los cuidados son muy similares a los de una ECCE planificada, con unas 3 visitas postoperatorias (una el mismo día o al día siguiente, otra una semana después y otra unas 5-6 semanas después). Dependiendo de la cantidad de astigmatismo el paciente puede requerir varias visitas para retirar secuencialmente las suturas mientras se elimina el astigmatismo inducido.
Primera visita postoperatoria: Esta visita suele realizarse la misma tarde (4-6 horas después de la cirugía) o a la mañana siguiente, con el objetivo principal de comprobar la PIO, buscar fugas en la herida y buscar material residual del cristalino o vítreo en la cámara anterior. Ciertamente, la mayoría de las fugas de la herida deben suturarse, pero si la CA no está formada, es obligatorio cerrarlas. El material nuclear residual debe eliminarse en los días siguientes si está presente, pero el material cortical residual suele disolverse con poca inflamación. Es de esperar una mala visión en el rango 20/200 debido al astigmatismo y al edema. La cámara anterior debería estar formada y suele tener una célula moderada (10-20 células/hpf con un haz de 0,2 mm). Si la PIO es inferior a 10 mmHg, busque cuidadosamente con un alto índice de sospecha de una fuga utilizando la prueba de Seidel. Si la PIO está en el rango de 10-29, entonces todo está probablemente bien, a menos que el paciente sea un vasculópata, en cuyo caso su límite superior de tolerancia de la PIO debería reducirse. Si la PIO está en el rango de 30-39, considere la supresión acuosa. Si la PIO es >40 entonces considere la supresión acuosa y «eructar» o «sangrar» la PIO a través de la paracentesis o una punción de la cámara anterior. La PIO debe volver a comprobarse 60-90 minutos después para asegurar el éxito del tratamiento. Observar el fondo de ojo para descartar desprendimiento de retina (DR) y derrame o hemorragia coroidea. Típicamente los pacientes son colocados en acetato de prednisolona 1% 1 gota 4 veces al día (QID), cyclogyl 1% 1 gota 2 veces al día (BID), y un antibiótico 1 gota QID para la semana siguiente.
Visita postoperatoria de la semana 1: La visión y la presión deben mejorar drásticamente en los pacientes durante la siguiente semana después de un caso que se convirtió en ECCE. La visión debe estar en el rango de 20/100 con una mejoría de los agujeros de alfiler a alrededor de 20/50. La visión suele estar limitada por el edema residual y el astigmatismo. En un estudio de nuestros casos de ECCE, encontramos alrededor de 7,0 dioptrías de cilindro en la visita de una semana. Se debe esperar muy poca inflamación y documentar que no existe RD. Busque material de lente residual en el segmento anterior y en el polo posterior. Puede suspender el ciclogilo y el antibiótico. Disminuir lentamente el acetato de prednisolona (por ejemplo, 1 gtt QID durante 7 días más, luego 1 gtt tres veces al día durante 7 días, luego 1 gtt BID durante 7 días, luego 1 gtt QD durante 7 días), y luego suspenderlo. Si el paciente está en el riesgo para el edema macular cistoide (CME), como es posible con la pérdida vítrea, entonces usted debe mantener en la prednisolona en la frecuencia más alta (por ejemplo, QID) y comenzar un no esteroide (como ketorolac tópico o equivalente 1 gtt QID) hasta la próxima visita 4 -6 semanas más tarde.
Visita postoperatoria de la semana 5: La visión debe seguir mejorando a medida que el astigmatismo se asienta y la córnea se aclara más. El ojo debe estar cómodo. La visión debe estar en el rango de 20/80, mejorando a 20/40 con estenopeica. En nuestro estudio, el astigmatismo inducido por las suturas ECCE fue de unas 5,0 dioptrías en la incisión. El segmento anterior debe estar tranquilo y la PIO normal (a menos que el paciente sea un «respondedor a los esteroides»). Considere la posibilidad de una CME en los pacientes en los que se requirió una conversión, ya que estos casos suelen ser largos y pueden implicar una pérdida de vítreo. Evaluar según lo indicado clínicamente por el examen o la historia con tomografía de coherencia óptica (OCT) o angiografía con flouresceína (FFA).
A estas alturas de la recuperación, la cuestión principal es el control astigmático con la retirada de la sutura. Utilice la queratometría, la refracción, la retinoscopia de rayas o la topografía para guiar la retirada de la sutura. Si la queratometría es 45.00 @ 90, y 40.00 @ 180, entonces busque suturas apretadas alrededor de los 90 grados (12 en punto) que están causando 5 dioptrías de cilindro. Puede quitar una sola sutura a las 5 semanas, pero para la evaluación de las 8 semanas, podría considerar quitar 2 suturas a la vez. El plan es quitar una sutura y ver cómo se asienta la córnea. Cuando el astigmatismo sea menor de 1,0 a 1,5 dioptrías, deberá dejar de retirar las suturas y corregir cualquier astigmatismo residual con refracción. Utilice gotas antibióticas de forma profiláctica durante unos días después de cada retirada de sutura. Después de esta visita debe considerar las siguientes opciones en cada visita (no pierda demasiado tiempo pensando en otras posibilidades y recuerde que no todo el mundo va a ser 20/20):
- retirar un punto (es decir el cilindro en el eje del punto es mayor de 1,0 a 1,5 dioptrías en la refracción manifiesta )
- dar gafas (es decir, no hay punto del que tirar o el cilindro es menor de 1 en la RM)
- obtener FFA u OCT porque se sospecha de CME
Vitrectomía anterior. La conversión a ECCE se acompaña casi siempre de vítreo. A veces la conversión se produce cuando el cristalino es demasiado duro y la cápsula está intacta, pero la mayoría de las veces parece que la conversión se produce cuando las zónulas o la cápsula liberan el vítreo en las reticentes manos del cirujano del segmento anterior. Cubriremos las causas y las muestras del prolapso vítreo y los principios de la vitrectomía anterior en varias situaciones.
Causas del prolapso vítreo. El vítreo sale alrededor de las zónulas o a través de un desgarro en la cápsula posterior. Los desgarros capsulares posteriores son causados comúnmente por 1) un desgarro anterior que se extiende posteriormente – lo más común, 2) un desgarro posterior – secundario a que la aguja de faco o el picador sean demasiado profundos, 3) durante la manipulación con el instrumento de I/A, o 4) una lesión preexistente (por ejemplo, catarata polar posterior, iatrogénica por PPVx, o por traumatismo penetrante del cristalino). Los problemas zonulares suelen ser preexistentes (por ejemplo, por un traumatismo, PXF o síndrome de Marfan), pero también pueden ser iatrogénicos por la rotación forzada del cristalino o por la tracción de la cápsula durante la I/A.
Signos de prolapso vítreo. El primer signo de prolapso vítreo es la negación. Algo parece mal pero usted no puede precisar el problema. Al principio usted niega que exista un problema, pero pronto se hace evidente. Otros signos reveladores del prolapso vítreo son: 1) profundización de la cámara, 2) ampliación de la pupila, 3) el material de la lente ya no está centrado, 4) las partículas de la lente ya no llegan a la faco o a la I/A, y 5) la lente ya no gira libremente. Cuando se sospecha de un prolapso vítreo se debe colocar OVD dispersivo en el ojo antes de retirar la aguja de faco o I/A y se puede comprobar la herida con un Weck-Cel (o una esponja de flecha similar) en busca de vítreo.
Principios básicos de la vitrectomía anterior. La clave de una vitrectomía anterior exitosa es controlar la fluidez del ojo. El primer paso es cerrar la cámara. Esto es a menudo difícil cuando usted ha convertido a un ECCE como la herida es grande. Sin embargo, hay que cerrar la herida para que el único punto de salida del líquido sea el dispositivo de aspiración/corte. Separe el dispositivo de irrigación del dispositivo de aspiración/corte para poder crear un diferencial de presión tal que el vítreo se vea estimulado a ir al dispositivo de aspiración/corte. El último punto importante es cortar bajo e irrigar alto. Si usted puede colocar el dispositivo de la irrigación en la cámara anterior sobre la aspiración/el cortador abajo cerca del plano de la cápsula posterior que el vítreo dejará la cámara anterior.
|
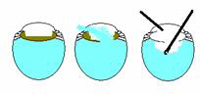 |
En general, la altura de la botella debe ser baja – lo suficientemente alta para mantener la CA formada y no tan alta para empujar el líquido y posiblemente el vítreo fuera del ojo. La velocidad de corte debe ser lo más alta posible cuando se corta el vítreo y baja cuando se corta el material del cristalino cortical. Discutiremos por separado la pérdida vítrea temprana, media y tardía del caso a continuación.
Vítreo Presente temprano en el caso – mientras la mayoría de la lente cristalina está en el ojo: Éste es el peor momento para el prolapso del vítreo y uno debe considerar fuertemente la conversión a ECCE. Los pasos a considerar se describen a continuación:1
- Si es tópico hacer inyección subtenoniana (como se ha descrito anteriormente)
- Considerar el cierre de la incisión temporal con 10-0 y hacer incisión separada con peritomía superior especialmente (como se ha comentado anteriormente)
- Utilizar viscoelástico dispersivo para levantar el cristalino cerca de la herida y desplazar el vítreo más posteriormente.
- Puede ser necesaria la vitrectomía Weck-Cel para limpiar si el vítreo está muy prolapsado
- Utilizar el lazo del cristalino para extraerlo (como se ha descrito anteriormente)
- Tener preparadas las tijeras Wescott cuando se saque el lazo del cristalino para cortar el vítreo
- Cerrar con 3 suturas de seguridad de Vicryl 7-0 cada una (una en el centro y otra a cada lado a 3 mm, permitiendo la retirada de la sutura central para colocar la LIO de 6 mm)
- Puede ser necesario añadir algo de nylon 10-0 en los bordes de la herida para asegurarse de que es estanca
- Vitrectomía anterior (como se ha comentado anteriormente, separar el aspirador/cortador del irrigador)
- Extracción en seco del material cortical residual con jeringa en cánula de calibre 27
- Utilizar cánula J-cánula o paracentesis si es necesario para el material subincisional
- Considerar la tinción con Kenalog (ver más adelante)
- Colocar la LIO si es posible en el sulcus (ajustar la potencia) o utilizar una LIO AC (no olvidar la iridotomía periférica)
- Miochol para bajar la pupila-asienta la LIO del sulcus, La pupila alta ayuda a detectar el vítreo
Vítreo Presentar el caso a mitad de camino – mientras se retira el material cortical: Esto parece ser el tiempo más común para la pérdida vítrea. A menudo uno conseguirá la cápsula posterior apenas mientras que se toma el último fragmento nuclear. Por supuesto, no hay ninguna razón para cambiar a ECCE en este caso. Los pasos siguientes son útiles:1
- Colocar viscoat en el área del desgarro o de la diálisis antes de quitar los instrumentos
- Hacer una incisión separada de 1 o 1.5 mm para la vitrectomía anterior
- Irrigar por separado (a través de la paracentesis) y aspirar/cortar (a través de la paracenetesis más grande)
- Puede ser necesario suturar la herida original para mantener la cámara formada
- Irrigar alto y cortar/chupar bajo – crea un gradiente de presión para empujar el vítreo hacia atrás
- Configuración de vacío bajo 100 rango, altura de botella baja 50 rango, máxima tasa de corte
- Intentar obtener algo del material cortical residual
- Extracción en seco del material cortical residual con jeringa en cánula de calibre 27
- Utilizar cánula J-o paracentesis si es necesario para el material subincisional
- Considerar la tinción con kenalog (ver más abajo)
- Colocar la LIO si es posible en el surco o en la CA (si es en la CA no olvidar la iridotomía periférica)
- Miochol para bajar la pupila
Cómo tratar el vítreo que se presenta tarde en el caso – mientras se coloca la LIO: Este es el momento menos problemático y menos común para perder vítreo. La cuestión principal es asegurarse de que la LIO es estable mientras se atiende al vítreo y luego asegurar una LIO adecuada en la CA, el surco o la bolsa:1
- Colocar viscoat en la zona de desgarro o diálisis antes de retirar los instrumentos
- Hacer una incisión separada de 1 o 1.5 mm para la vitrectomía anterior
- Irrigar por separado (a través de la paracentesis) y aspirar/cortar (a través de la paracenetesis más grande)
- Puede ser necesario suturar la herida original para mantener la cámara formada
- Irrigar alto y cortar/chupar bajo – crea un gradiente de presión para empujar la V hacia atrás
- Configuración de vacío bajo 100 rango, altura de botella baja 50 rango, tasa de corte máxima
- Si el surco puede soportar una LIO, entonces
- Mover la LIO de 3 piezas existente en el surco
- Reemplazar una LIO de una pieza existente conLIO de 3 piezas en el sulcus
- Considere la captura de la cápsula anterior de la óptica si el CCC es redondo y centrado
- Si el desgarro en la cápsula posterior es redondo y seguro
- Coloque el viscoat en el agujero
- Coloque suavemente la LIO de una pieza en la bolsa (tenga mucho cuidado con la lente de 3pieza en la bolsa)
- Miochol para bajar la pupila
Tinción del vítreo con Kenalog: Scott Burk en Cincinatti Eye describió el uso de Kenalog fuera de etiqueta para teñir el vítreo que había prolapsado en la cámara anterior5 (siga el enlace al vídeo de Facebook). Como el Kenalog no está aprobado por la FDA para esta indicación y como algunos cirujanos de retina han tenido endoftalmitis estériles (e incluso infecciosas) por usar el Kenalog, su uso es controvertido. Sin embargo, es un complemento muy útil para la vitrectomía anterior. El método para mezclar la triamcinolona (Kenalog) para diluir 10:1 y para lavar el conservante es el siguiente:
- Jeringa TB para retirar 0.2 ml de triamcinolona bien agitada (40mg/ml)
- Retire la aguja y sustitúyala por un filtro de jeringa de 5 (o 22) micras (Sherwood Medical)
- Fuerce la suspensión a través del filtro y deseche el vehículo lleno de conservante
- El Kenalog quedará atrapado en el lado de la jeringa del filtro
- Transfiera el filtro a una jeringa de 5 ml llena de solución salina equilibrada (BSS)
- Fuerce suavemente la BSS a través del filtro para enjuagar aún más el conservante
- Repita el enjuague unas cuantas veces
- Coloque una aguja de calibre 22 en el extremo distal del filtro
- Atraiga 2 ml de BSS en la jeringa a través del filtro para resuspender el Kenalog
- El Kenalog (ahora sin conservante y diluido 10:1) teñirá los filamentos vítreos de blanco
- Oetting, TA, Cataract Surgery for Greenhorns, Disponible en http://medrounds.org/cataract-surgery-greenhorns. consultado el 9 de septiembre de 2007
- Dupps WJ Oetting TA, Diamond iris retractor configuration for small-pupil extracapsular or intracapsular cataract surgery. J Cataract Refract Surg Vol 30(12):2473-2475.
- Chang DF, Oetting TA, Kim T, Curbside Consultations in Anterior Segment Surgery, Slack Inc, Thorofare NJ, 2007.
- Henderson BA, Essentials of Cataract Surgery, Slack Inc, Thorofare NJ, 2007.
- Burk SE, Da Mata AP, Snyder ME, Schneider S, Osher RH, Cionni RJ. Visualizing vitreous using Kenalog suspension J Cataract Refract Surg. 2003 Apr;29(4):645-51.