¿Qué es una ANOMALÍA CONGÉNITA DE LA ARTERIA CORONARIA?
Existe un debate permanente sobre lo que debe considerarse normal y lo que debe considerarse una anomalía de la arteria coronaria (AAC). Según Angelini,1 las AAC se diagnostican por exclusión, lo que significa que, en aquellos casos en los que la morfología de las arterias coronarias no es normal, se define la normalidad según un criterio estadístico (intervalo entre más o menos 2 desviaciones estándar del valor medio). Así, una AAC sería aquella morfología arterial coronaria observada en menos del uno por ciento de la población general.1,2 Las AAC pueden producirse durante la cardiogénesis normal o patológica: en el primer caso, el resultado sería una AAC aislada, en la que nos centramos en este artículo, mientras que, en el segundo, estarían asociadas a otras malformaciones cardíacas.
CLASIFICACIÓN
Existen varias clasificaciones.1-3 Recientemente se ha propuesto una nueva que intenta estandarizar los criterios diagnósticos y agrupa las AAC según 7 categorías4 (Tabla 1).


Los grupos internacionales reclaman registros que incluyan al menos las anomalías que causan la mayoría de los eventos clínicos (muerte súbita e isquemia miocárdica) atribuidos a las AAC,5-7 constituidas por las que se originan en el seno de Valsalva contralateral o «equivocado». En este grupo se incluyen las arterias coronarias de un solo vaso («hiperdominancia» en la clasificación de Rigatelli et al4), ya que tienen que suministrar sangre al miocardio surgiendo de un único ostium coronario y estableciendo rutas que en ocasiones son similares a las de las AAC con origen en el seno de Valsalva equivocado (Figura 1).

Figura 1. Arteriografía coronaria en proyección oblicua anterior izquierda que muestra una arteria coronaria derecha de un solo vaso.
INCIDENCIA
Las diferentes definiciones o clasificaciones y el análisis tanto de las series angiográficas8,9 como de las autopsias10 y, en los últimos años, de las series ecocardiográficas11 dan como resultado una incidencia comunicada de AAC que oscila entre el 0,1% y el 8,4%,1,8,11 lo que hace difícil establecer la magnitud exacta del problema que representan. En general, la incidencia puede ser bastante similar a la de otras enfermedades que hemos podido definir con mayor precisión, como
la miocardiopatía hipertrófica (0,2%)12 o el síndrome de Wolff-Parkinson-White (0,1% a 0,3%).13
La incidencia de arterias coronarias anómalas con origen en el seno equivocado y de arterias coronarias de un solo vaso en los estudios angiográficos coronarios oscila entre el 0.28% y 1,74%.2,3,8,9,14-16 Dada su importancia clínica, vamos a centrar nuestra revisión en estas anomalías.
PRESENTACIONES CLÍNICAS
Inicialmente, estas anomalías se diagnosticaban durante la angiografía coronaria realizada en pacientes con valvulopatía o cardiopatía isquémica, y se consideraba que no tenían importancia clínica. Posteriormente, se empezaron a notificar casos de muerte súbita en deportistas jóvenes en los que el único signo de enfermedad era una anomalía con origen en las arterias coronarias.8,17
El espectro clínico en el momento de la presentación es variable: mientras que algunos pacientes son asintomáticos, otros presentan angina, disnea, síncope, infarto agudo de miocardio, insuficiencia cardíaca y muerte súbita.1,2,5,8,17-20 Actualmente, se considera que los AAC son la segunda causa más común de muerte súbita en los deportistas en los Estados Unidos.21
¿Significa esto que todos los AAC deben considerarse como indicadores de alto riesgo? Absolutamente no, pero desde un punto de vista estratégico, deben considerarse «potencialmente malignas» hasta que se realicen pruebas adicionales para descartar una isquemia miocárdica provocada por la anomalía.
La mayor preocupación radica en determinar qué AAC pueden presentarse con muerte súbita. Hoy sabemos que aquellas que siguen un curso interarterial (o intramural), aquellas en las que la arteria coronaria anómala es la dominante y las que producen signos clínicos en pacientes de menos de 30 o 35 años son aquellas en las que la incidencia de muerte súbita es mayor.22-26
Por este motivo, nuestra aproximación a una AAC debe ser diferente según la edad del paciente. En los jóvenes, menores de 35 años, nos «centraremos» en la prevención de la muerte súbita, mientras que en los mayores de 35 años, el objetivo principal será tratar la isquemia miocárdica (Figura 2).
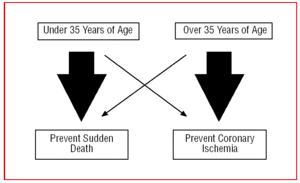
Figura 2. Diferente abordaje según la edad del paciente.
Ocasionalmente, debido a su origen y curso anómalo, los CAA pueden resultar dañados durante la cirugía de sustitución valvular, pero esto también puede ocurrir durante el cierre percutáneo del foramen oval. Por este motivo, debe descartarse la presencia de AAC antes de realizar intervenciones de este tipo.27-30
PATOGRAFÍA DE LA ISQUEMIA EN LAS ANOMALÍAS CORONARIAS
Existen varias teorías31 para explicar los mecanismos que producen la isquemia en las AAC, pero ninguna de ellas ha sido claramente demostrada. En una de ellas, se considera que la causa es la marcada angulación de la arteria anómala en el lugar donde emerge de la aorta. A diferencia de una arteria coronaria normal, que es perpendicular a la aorta en su origen, la arteria coronaria anómala tiene que doblarse sobre sí misma para alcanzar, desde el seno de Valsalva opuesto, su territorio de suministro normal. Por ello, el ostium de la arteria coronaria anómala sería más pequeño, con crestas en forma de válvula, en comparación con el ostium circular normal, y podría llegar a comprimirse en caso de una expansión marcada de la aorta, como la que se observa durante el ejercicio extenuante.32
Otra teoría se refiere al curso inicial de la AAC. Cuando es interarterial, entre la aorta y la arteria pulmonar, el aumento de la presión en los 2 vasos, que se produce durante el esfuerzo, produciría una compresión de la arteria coronaria anómala.33 Además, si el trayecto inicial es intramural, la obstrucción puede verse potenciada ya que la arteria coronaria puede deformarse dentro de la pared aórtica durante los períodos de hipertensión.34
Algunos autores consideran que el mecanismo que conduce a la isquemia implica la producción de un espasmo en la arteria coronaria anómala como consecuencia del daño endotelial producido por la vía anómala,35 y otros, que se produciría una invaginación de la porción proximal de la AAC en la pared aórtica.31
Por último, todos los mecanismos comentados pueden producir isquemia aguda o crónica (eventos isquémicos menores) que provoquen fibrosis miocárdica que, a su vez, podría ser la causa de la generación de arritmias letales.36
¿Cómo se diagnostica una anomalía coronaria?
El diagnóstico requiere un alto índice de sospecha y la valoración de su presencia en determinadas circunstancias. Como hemos comentado anteriormente, la mayoría de las AAC se descubren de forma incidental durante las angiografías coronarias realizadas en pacientes con cardiopatía isquémica o valvulopatía que se someten a este estudio antes de la cirugía de sustitución valvular.
Los jóvenes que no presentan factores de riesgo coronario ni valvulopatía asociada representan el mayor reto diagnóstico. Debemos sospechar un AAC ante la presencia de síncope de esfuerzo, disnea o dolor torácico indicativo de angina.24,26,35 Evidentemente, la primera prueba diagnóstica que todos realizamos es la ergometría estándar. Sin embargo, ésta no ha demostrado ser muy útil en este tipo de pacientes ya que suele ser negativa, hecho que indica que la isquemia por AAC se presenta sólo ocasionalmente.35,36
Por tanto, dado que las pruebas «funcionales» no son de gran ayuda, debemos optar por un estudio de imagen que nos permita examinar la anatomía coronaria. La prueba no invasiva recomendada inicialmente es la ecocardiografía transtorácica (ETT).7,26,37-40 En la mayoría de estos pacientes, la realización de una ETT simple en la proyección paraesternal de eje corto en el plano de la raíz aórtica permite distinguir los dos ostia coronarios e incluso determinar el curso inicial de la AAC. Pellicia et al estudiaron 1360 deportistas de élite mediante ecocardiografía, visualizando el ostium y la porción proximal de la coronaria principal izquierda en el 97% de los casos y la coronaria principal derecha en el 80%.41
Recientemente, Frommelt et al34 realizaron una ecocardiografía a todos los niños y adolescentes (rango de edad, 3 meses a 20 años) remitidos a su hospital (1997-2002) con síntomas de isquemia miocárdica, sospecha de cardiopatía congénita o dolor musculoesquelético. Todos ellos se sometieron a una ETT convencional con ayuda de un mapa de flujo Doppler en color para determinar la dirección del flujo sanguíneo. Identificaron a 10 pacientes con origen anómalo de una arteria coronaria en el seno equivocado (6 pacientes con arteria coronaria izquierda originada en el seno de Valsalva derecho y 4 con arteria coronaria derecha originada en el seno de Valsalva izquierdo). Utilizando la ETT con técnicas de Doppler color, observaron un curso intramural dentro de la pared aórtica en nueve de los pacientes y un curso intramiocárdico en el paciente restante. Cuando el curso de una AAC originada en el seno equivocado es intramural, puede parecer que emerge de su ostium normal. Por ello, los autores recomiendan la utilización del Doppler color para determinar la dirección del flujo cuando sea necesario descartar la presencia de una anomalía.
Los avances en las técnicas de imagen ecocardiográfica permiten determinar el origen y seguir el curso inicial de una AAC en determinados grupos de pacientes. Se han realizado estudios en niños, adolescentes y deportistas de élite, pero aún no se han estudiado grandes series que incluyan a la población adulta normal. Por ello, la identificación de los ostia coronarios en pacientes jóvenes con esta sintomatología debe realizarse de forma sistemática en la exploración ETT.7,26
En pacientes con una mala ventana ecocardiográfica, o cuando persiste la duda diagnóstica a pesar de las indicaciones clínicas, para permitir la visualización del origen y el curso inicial de la AAC, se puede realizar una ecocardiografía transesofágica (ETE)7,26,42,43 tomografía computarizada (TC)26,44-46–con haz de electrones o multicorte–(Figura 3) o una resonancia magnética cardiaca (RMC)26,47,48 (Figura 4).

Figura 3. Imagen de tomografía computarizada multidetector que muestra la arteria coronaria circunfleja (Cx) originada en la arteria coronaria derecha (CD), siguiendo un curso retroaórtico para llegar a su territorio de distribución normal. Ao indica aorta; AP, arteria pulmonar. Cortesía del Dr. Gabriel C. Fernández, Servicio de Radiología, Hospital Povisa, Vigo, España.
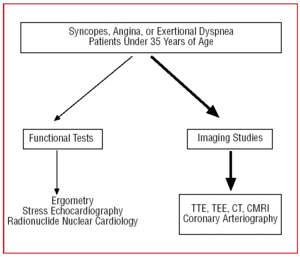
Figura 4. Protocolo diagnóstico propuesto en pacientes menores de 35 años con sospecha de anomalía coronaria. RMC: resonancia magnética cardiaca; TC: tomografía computarizada; ETE: ecocardiografía transesofágica; ETT: ecocardiografía transtorácica.
¿Qué técnica debemos utilizar y en qué orden? Cada equipo médico debe responder a esta pregunta de acuerdo con las técnicas disponibles y su experiencia. Lo que debemos hacer es identificar la AAC y su curso inicial mediante la técnica menos invasiva de que dispongamos. Aunque la ETE se ha utilizado en el diagnóstico e identificación del curso inicial de algunas AAC, consideramos que, dado su carácter semiinvasivo, debe emplearse sólo tras el fracaso de otras técnicas. Hoy en día, debido a la creciente disponibilidad y a las excelentes imágenes tridimensionales que se pueden obtener, parece prudente optar por la TC multidetector (figura 5) o por la RMC49,50. La arteriografía coronaria estándar estaría indicada si las otras pruebas no dan lugar a un diagnóstico definitivo. En este sentido, la 36ª Conferencia de Bethesda51 para la selección de deportistas de competición con anomalías cardiovasculares, publicada en abril de 2005, recomendaba «Las anomalías coronarias deben considerarse en los atletas con síncope de esfuerzo o arritmia ventricular sintomática y deben investigarse mediante estudios apropiados como la ecocardiografía, la RMC o la tomografía computarizada ultrarrápida. La angiografía coronaria está indicada si otros estudios no son diagnósticos». En resumen, no se decantan por un estudio diagnóstico u otro.
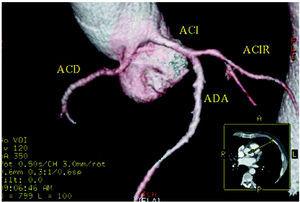
Figura 5. Tomografía computarizada multicorte (16 cortes); reconstrucción tridimensional renderizada que muestra la arteria coronaria derecha (ACD) originada en el seno de Valsalva izquierdo. ACI indica la arteria coronaria izquierda; ACIR, arteria coronaria circunfleja; ADA, arteria coronaria descendente anterior. Cortesía del Dr. Joaquín Alonso, Servicio de Cardiología y Servicio de Diagnóstico por Imagen, Hospital de Fuenlabrada, Madrid, España.
En los pacientes mayores de 35 años que presentan signos clínicos de angina o síncopes repetidos, tras la prueba funcional (ergometría, ecocardiografía de ejercicio, etc.), se suele realizar un cateterismo, ya que la mayor incidencia de aterosclerosis hace sospechar la existencia de enfermedad coronaria. En determinados centros equipados con esta tecnología, los pacientes con un cuadro clínico atípico pueden someterse a un cribado inicial con TC multidetector o CRMI. En cualquiera de las dos circunstancias, la AAC sería un hallazgo (Figura 6).
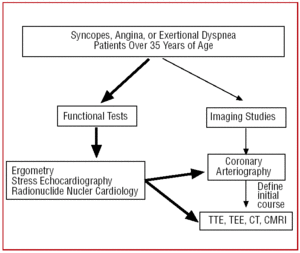
Figura 6. Protocolo diagnóstico propuesto en pacientes mayores de 35 años con sospecha de anomalía arterial coronaria. CRM: resonancia magnética cardiaca; TC: tomografía computarizada; ETE: ecocardiografía transesofágica; ETT: ecocardiografía transtorácica.
¿Cómo se identifica el curso inicial de una anomalía coronaria?
Este es uno de los puntos más complejos del estudio de las AAC y constituye un aspecto fundamental en la identificación del riesgo.
Para empezar, hay que tener en cuenta que el nombre y la naturaleza de una arteria coronaria se definen por el territorio que irrigan, no por su origen. Así, una coronaria que nace del seno de Valsalva derecho y se ramifica para irrigar los territorios de las arterias descendente anterior y circunfleja (Cx), no es una arteria coronaria derecha sino una arteria coronaria principal izquierda con origen en el seno equivocado. Cuando una arteria coronaria surge del seno equivocado, el nombre, la naturaleza e incluso la función siguen siendo los mismos; sólo su origen y su curso inicial son anómalos.2
Después de emerger del seno de Valsalva equivocado, una arteria coronaria anómala puede alcanzar su territorio de suministro normal a través de al menos cinco rutas diferentes2,52:
1. Retrocardíaca, por detrás de las válvulas mitral y tricúspide.
2. 2. Retroaórtica, generalmente seguida de la Cx con origen en el seno de Valsalva derecho o en la arteria coronaria derecha, adyacente a la pared aórtica posterior, en el surco entre la aurícula y la aorta (seno transverso) (Figura 3).
3. Preaórtico o interarterial (entre la aorta y la arteria pulmonar), en el que la coronaria derecha anómala, la descendente anterior izquierda o la coronaria principal izquierda atraviesan el septo o el espacio aortopulmonar. Este es el curso que más frecuentemente se ha relacionado con signos de isquemia y/o muerte súbita (Figuras 7 y 8).
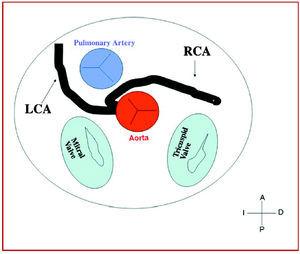
Figura 7. Diagrama que muestra el curso interarterial de una arteria coronaria derecha (ACD) que se origina en el seno contralateral.
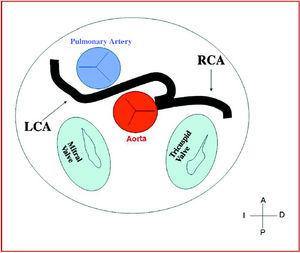
Figura 8. Diagrama que muestra el curso interarterial de una arteria coronaria izquierda (ACL) que se origina en el seno contralateral.
4. Intraseptal, a través de la porción superior del tabique intraventricular. Es intramiocárdica en la mayoría de los casos y se reconoce en la angiografía por el estrechamiento sistólico, similar a un puente miocárdico, y porque suele haber 1 o 2 ramas perforantes septales en esta zona (Figura 9).

Figura 9. Diagrama que muestra el curso intraseptal de una arteria coronaria izquierda (CI) originada en el seno de Valsalva derecho.
5. Precardíaca o prepulmonar, caracterizada por su localización subepicárdica, en la pared anterior del tracto de salida del ventrículo derecho o infundíbulo. Este paso suele ir seguido de una coronaria derecha anómala, del tronco principal izquierdo o de la arteria coronaria descendente anterior.
Se han descrito otros cursos posibles o incluso varios cursos en un mismo paciente.2
¿Cómo se pueden identificar estos cursos iniciales mediante la angiografía coronaria? Inicialmente, se consideró que la introducción de un alambre guía en la arteria pulmonar seguida de una arteriografía coronaria en proyección lateral sería suficiente para determinar la relación entre la anomalía y los grandes vasos. Sin embargo, esta técnica tiene un valor limitado ya que, por ejemplo, en una proyección lateral, tanto el curso septal como el interarterial parecerían estar situados posteriormente a la arteria pulmonar y anteriormente a la aorta cuando, en realidad, el curso septal está situado caudalmente a ambos vasos.53
También se han descrito diferentes características angiográficas coronarias para el reconocimiento de la anomalía y su curso inicial, incluso antes de su visualización. En este sentido, Page et al54 proponen dos signos que permiten reconocer un origen anómalo de la Cx y su curso inicial:
1. El signo del «miocardio no perfundido». Durante la opacificación selectiva de la arteria coronaria izquierda, podemos observar un área avascular en la zona posterolateral del ventrículo izquierdo que indica el origen anómalo de la Cx. En primer lugar es necesario inyectar un medio de contraste en el seno coronario izquierdo para descartar la afectación de los ostia independientes de las arterias descendente anterior y Cx. Sin embargo, si la identificación de la Cx no es clara, debemos recordar que es más frecuente observar la Cx originada en el seno coronario derecho o en la arteria coronaria derecha que la presencia de ostia independiente en el seno coronario izquierdo.55
2. El signo de la «raíz aórtica». En la ventriculografía, la proyección oblicua anterior derecha muestra el contorno de la Cx anómala y sigue su curso al pasar por detrás del seno coronario derecho (figura 10).
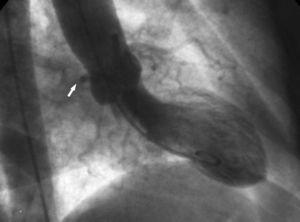
Figura 10. Ventriculografía en proyección oblicua anterior derecha que muestra el contorno de la arteria circunfleja anómala (flecha) que pasa por detrás del seno coronario derecho; esto se conoce como signo de la raíz aórtica o signo de Page.
En 1985, Ishikawa et al,56 seguidos por Serota et al en 1990,57 propusieron una serie de criterios arteriográficos coronarios destinados a definir la relación, a lo largo del curso inicial, entre el vaso anómalo y la aorta y la arteria pulmonar (figura 11). Estos autores intentaron identificar los diferentes cursos en base a la orientación del «bucle» que forma la arteria coronaria anómala con el resto del árbol coronario56 o aplicando el concepto de «punto» (visualización de la columna de contraste de la AAC que, por el giro que realiza, adopta la morfología de un punto57).
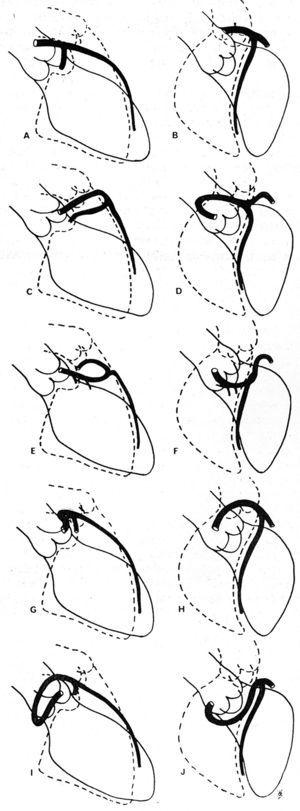
Figura 11. Ilustraciones de imágenes de angiografía coronariac de las arterias coronarias descendente anterior izquierda y circunfleja proximal en proyección oblicua anterior derecha (A, C, E, G, I) y en proyección oblicua anterior izquierda (B, D, F, H, J), que muestran los diferentes cursos iniciales posibles de una arteria coronaria izquierda originada en el seno de Valsalva derecho. A y B representan una arteria coronaria normal; C y D muestran el «loop» anterocraneal, descrito en el curso anterior; E y F: «loop» anterocaudal, curso septal; G y H: «loop» posterocraneal, curso interarterial; I y J: «loop» posterocaudal, curso retroaórtico. Tomado de Ishikawa et al.56
En muchos casos, la identificación del curso inicial de la AAC mediante angiografía coronaria es difícil, ya que esta técnica proporciona una visión bidimensional del árbol coronario, que es una estructura tridimensional compleja. Para un cardiólogo intervencionista con experiencia en el diagnóstico de AAC, la angiografía coronaria puede ser suficiente para la correcta identificación del curso. Sin embargo, dada su baja incidencia, la mayoría de los cardiólogos intervencionistas tienen una experiencia limitada en el estudio de las AAC. Por ello, en la gran mayoría de los casos, no se describen adecuadamente. En un registro reciente en el que participaron 13 hospitales españoles, en la mayoría de los casos no se identificó el curso inicial de la AAC comunicada.16
Por ello, en muchas ocasiones, la identificación del curso inicial de una AAC con origen en el seno equivocado requiere una técnica de imagen adicional. Como mencionamos anteriormente, tanto la ETT como la ETE pueden ser empleadas para este fin pero, dada la creciente disponibilidad en nuestros hospitales de técnicas no invasivas que proporcionan una definición más correcta y exacta de la anatomía coronaria y su relación con las estructuras adyacentes en pacientes que pueden ser candidatos a cirugía, nos decantamos por la RMC o la TC multidetector.35,37,47,49
¿CUÁL ES EL MEJOR ENFOQUE TERAPÉUTICO?
Este es uno de los aspectos más controvertidos de esta patología ya que no se han establecido pautas oficiales al respecto.
Una vez diagnosticada y caracterizada la AAC, parece lógico intentar determinar si está provocando o no isquemia miocárdica. Si el paciente ha tenido un infarto de miocardio (sin relación demostrable con la aterosclerosis) o ha sido sometido a una reanimación por muerte súbita atribuible a la anomalía y es menor de 35 años, la mayoría de los autores recomiendan la revascularización.24,26,35
Una prueba de esfuerzo con talio o una ecocardiografía bajo estrés farmacológico o inducido por el ejercicio que demuestre isquemia reversible en el territorio de la anomalía ayudará en el proceso de toma de decisiones.36
¿Qué se debe hacer en el caso de individuos jóvenes y asintomáticos en los que se descubre incidentalmente una AAC si se cumplen los criterios de riesgo, pero la prueba de esfuerzo no produce evidencia de isquemia? En primer lugar, el paciente debe adoptar un estilo de vida sedentario.26,35
Corrado et al compararon la muerte súbita en jóvenes deportistas y no deportistas y sólo las atribuidas a AAC o a displasia arritmogénica del ventrículo derecho se asociaron al esfuerzo.58 Respecto al tratamiento, la revascularización es controvertida, pero hay autores que optan por este enfoque ya que, en estos pacientes, la muerte súbita es imprevisible y puede ser el primer signo de AAC.24,26,34,35 Algunos autores apoyan las visitas de seguimiento anuales en estos casos, con ecocardiogramas o pruebas de esfuerzo con talio, y basan sus decisiones en los resultados.7,36 Tras el tratamiento quirúrgico, los pacientes disfrutan de un estilo de vida normal, incluyendo la participación en deportes.25,34,49
En los pacientes mayores de 35 años, las decisiones deben tomarse de forma individual. El riesgo de muerte súbita es menor pero, dado que la AAC puede provocar isquemia miocárdica sintomática, en algunos casos se realiza una revascularización (Figura 12).24,26
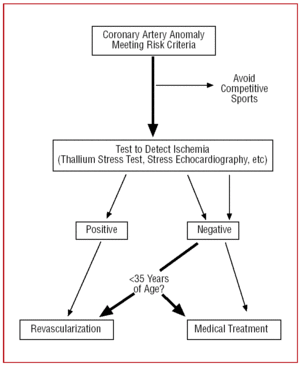
Figura 12. Protocolo terapéutico propuesto para las anomalías coronarias con origen en el seno de Valsalva contralateral en presencia de factores de riesgo.
Algunos grupos están investigando la utilización de determinados protocolos diagnósticos (ecocardiografía intracoronaria para evaluar el ostium coronario anómalo en reposo y tras infusión de dobutamina o sobrecarga de líquidos)59 o la utilización de cables de presión intracoronaria para detectar isquemia.60
Como puede observarse, hasta que no se establezcan directrices oficiales en esta materia, la aproximación más razonable parece ser, en primer lugar, confirmar si la edad del paciente y la anatomía de la AAC se asocian con el riesgo y, en segundo lugar, verificar que la isquemia coronaria (presentada por el paciente o demostrada) está claramente provocada por la anomalía.
¿CÓMO SE DEBE REALIZAR LA REVASCULARIZACIÓN?
Lógicamente, hay que tratar cada caso de forma individualizada según la anatomía coronaria; así, la revascularización puede ser quirúrgica o percutánea.
La revascularización quirúrgica implica el bypass aortocoronario, el reimplante ostial o la técnica de unroofing, que libera el segmento intramural de la AAC mediante una incisión en la pared que comparten la AAC y la aorta, creando así un nuevo orificio de mayor tamaño en el seno apropiado.61,62 Existe una gran controversia sobre la revascularización quirúrgica en estos pacientes, especialmente en los jóvenes. El injerto de bypass aortocoronario ha sido muy criticado7,63 debido a su permeabilidad «limitada» y al inevitable flujo competitivo entre el bypass y la AAC. Por ello, se está adoptando cada vez más la técnica de unroofing, que parece ser más fisiológica62.
La intervención percutánea, con implantación de stents en la región de la compresión entre los grandes vasos y en el ostium anómalo, se ha realizado en varios casos, en adultos, con éxito a corto plazo64. Hasta la fecha, la revascularización quirúrgica se prefiere en pacientes jóvenes y el procedimiento percutáneo se realiza sólo en adultos.26,62-64 Evidentemente, en ambos casos, es necesario un seguimiento a largo plazo.
¿Es el tratamiento médico una opción?
La falta de series y estudios controlados hace difícil responder a esta pregunta. Hay informes que incluyen el seguimiento a los 2 y 5 años en pacientes que o rechazaron la cirugía, en los que el enfoque fue el manejo expectante o el tratamiento con betabloqueantes, y entre los que no hubo casos de muerte súbita.65-68 Sin embargo, algunos autores argumentan en contra de la decisión de iniciar un tratamiento «de por vida» en niños y adolescentes.7
PROBLEMAS MAYORES NO RESUELTOS
El verdadero riesgo de muerte súbita asociado a cada anomalía es desconocido.5 Esto se debe a que el riesgo se calcula sobre la base de estudios de autopsia, que no indican el riesgo real de que una persona muera como consecuencia de una AAC, sino que sugieren la posibilidad de que una persona que ha experimentado una muerte súbita tenga una AAC.7 Además, los riesgos calculados pueden estar sobreestimados con respecto a la población general, ya que se obtienen a partir de series de deportistas de competición que, como se ha informado, tienen un riesgo de muerte súbita dos veces superior al de una persona sedentaria.69 Sabemos que el riesgo de muerte súbita por una AAC es mayor en los jóvenes; de hecho, se recomienda un enfoque terapéutico u otro según el paciente tenga menos de 30 o 35 años. Estos puntos de corte se basan en los escasos estudios que abordan esta cuestión23,25 y, por tanto, deben considerarse meramente orientativos. Por esta razón, el enfoque terapéutico debe decidirse siempre de forma individual.
Si se adopta la solución quirúrgica descrita anteriormente, hay que tener en cuenta que no existen series en las que se haya estudiado la evolución de los pacientes durante más de dos años. A la incertidumbre sobre la permeabilidad del bypass se añade el posible daño a la válvula aórtica que puede producir el procedimiento de desobstrucción. En este sentido, se han descrito casos de insuficiencia aórtica o incluso de sustitución valvular tras este procedimiento.7,70 Hay que recordar que la cirugía cardíaca siempre conlleva el riesgo de complicaciones neurológicas, cuya incidencia en jóvenes se ha estimado en torno al 2,3%.71
Por último, las guías de selección de deportistas de competición con anomalías cardiovasculares recomiendan excluir a los pacientes con AAC de todos los deportes de competición.51 Una vez más, se han extrapolado los datos de una población de deportistas a la población general. En un adolescente, el término «competitivo» puede ser difícil de definir. Además, prohibir a un adolescente o a un adulto joven que participe en clases de gimnasia o en el deporte que le gusta puede causar más daños que beneficios. Tal vez deban evitarse los deportes extenuantes, pero no un deporte menos exigente.7
CONCLUSIÓN
Las arterias coronarias que se originan en el seno de Valsalva incorrecto constituyen el grupo de AAC más comúnmente asociado a la isquemia miocárdica y, en particular, a la muerte súbita.
El índice de sospecha de esta anomalía debe ser alto en los pacientes jóvenes que presentan signos clínicos de angina, disnea o síncope de esfuerzo. En estos casos, debe realizarse una ETT para intentar identificar los ostia y el curso inicial de ambas arterias coronarias.
Deberíamos definir claramente el curso inicial de cada arteria coronaria anómala, utilizando técnicas de imagen como la ETT, la ETE o, preferiblemente, la TC multidetector o la RMC, según las características de nuestro hospital.
Debemos dar prioridad a la creación de registros nacionales e internacionales que nos permitan determinar la incidencia de estas anomalías, así como las tasas de morbilidad y mortalidad asociadas, el pronóstico, el tratamiento, las posibles influencias genéticas o ambientales y, en definitiva, conocer todo lo que podamos al respecto.
Es necesario realizar un seguimiento a largo plazo de los pacientes intervenidos de AAC, especialmente de los jóvenes. En cualquier caso, la revascularización (quirúrgica o percutánea) puede ser una opción válida para los pacientes con este tipo de enfermedad.
Agradecimientos
Agradecemos al Dr. Joaquín Alonso y al Dr. Gabriel C. Fernández su ayuda en la obtención de las imágenes de tomografía computarizada multidetector.